Le Informazioni Presenti Sul Sito Non Costituiscono Consulenza Medica. Non Vendiamo Nulla. L'Accuratezza Della Traduzione Non È Garantita. Disclaimer
Fattori di coagulazioneEsperoct
Riepilogo della droga
Cos'è Esperoct?
Esperoct [fattore anti-emofilo (ricombinante) glicopegylated-exei] è un coagulazione Concentrati del fattore VIII indicato per l'uso in adulti e bambini con emofilia A per il trattamento su richiesta e il controllo degli episodi di sanguinamento perioperatoria di gestione del sanguinamento e della profilassi di routine per ridurre la frequenza degli episodi di sanguinamento. L'esperoct non è indicato per il trattamento della malattia di von Willebrand.
Quali sono gli effetti collaterali di Esperoct?
Topper esperoct
- orticaria
- Difficoltà a respirare
- gonfiore della lingua o della gola
- prurito
- eruzione cutanea
- intorpidimento
- formicolio
- febbre
- vertigini
- nausea
- battiti cardiaci veloci
- tenuta toracica
- sibilante
- pelle pallida
- sudore freddo
- Accendino
- svenimento
- aumento degli episodi di sanguinamento
- qualsiasi sanguinamento che non si fermerà e
- dolore al petto
Ottieni subito assistenza medica se hai uno qualsiasi dei sintomi sopra elencati.
Gli effetti collaterali comuni di Esperoct includono:
- eruzione cutanea
- arrossamento
- prurito E
- Reazioni del sito di iniezione
Cerca cure mediche o chiama il 911 contemporaneamente se hai i seguenti gravi effetti collaterali:
- Sintomi di occhiali gravi come la perdita di visione improvvisa del tunnel della visione sfocata Dolore alla visione o gonfiore o vedere aloni attorno alle luci;
- Sintomi cardiaci gravi come battiti cardiaci irregolari o martellanti veloci; svolazzando nel petto; fiato corto; e improvviso vertigini giuria o svenuta;
- Grave mal di testa confusione Il braccio del linguaggio bloccato o la debolezza delle gambe problemi perdite perdita di coordinamento sentendoti instabili muscoli molto rigidi ad alta febbre abbondante sudorazione o tremori.
Questo documento non contiene tutti i possibili effetti collaterali e altri possono verificarsi. Verificare con il tuo medico ulteriori informazioni sugli effetti collaterali.
Dosaggio per esperoct
La dose di Esperoct dipende dall'uso.
Quali sostanze o integratori di farmaci interagiscono con l'esperoct?
Esperoct può interagire con altri farmaci. Dì al medico tutti i farmaci e gli integratori che usi.
Esperoct durante la gravidanza o l'allattamento
Di 'al medico se sei incinta o hai intenzione di rimanere incinta prima di usare Esperoct; Non è noto come influirebbe su un feto. Non è noto se l'esperoct passi nel latte materno o se influisse su un bambino infermieristico. Consulta il medico prima dell'allattamento al seno.
Ulteriori informazioni
La nostra polvere liofilizzata da ESPEROCT [fattore antiemofilo (ricombinante) glicopegopegylated-exei] per soluzione per gli effetti collaterali per endovenosi offre una visione completa delle informazioni disponibili sui farmaci sui potenziali effetti collaterali quando si assume questo farmaco.
Informazioni sui farmaci FDA
- Descrizione del farmaco
- Indicazioni
- Effetti collaterali
- Avvertimenti
- Overdose
- Farmacologia clinica
- Guida ai farmaci
Descrizione per esperoct
L'esperoct è una polvere liofilizzata non pirogenica senza conservante sterile per iniezione endovenosa dopo la ricostituzione con il diluente salino fornito. L'ingrediente attivo in Esperoct è un analogo ricombinante del fattore VIII di coagulazione umana (FVIII) coniugato con una molecola di glicole polietilenico (PEG) da 40 kDa. L'esperoct è formulato con i seguenti eccipienti: cloruro di sodio l-istidina saccarosio polisorbato 80 l- metionina e cloruro di calcio.
L'attività di FVIII in Esperoct è determinata usando il test cromogenico descritto nella farmacopea europea. L'assegnazione delle attività impiega un materiale di riferimento FVIII che è rintracciabile all'attuale standard internazionale dell'Organizzazione mondiale della sanità (OMS) per il concentrato di FVIII e valutato con metodologie appropriate per garantire l'accuratezza dei risultati. Esperoct è disponibile in fiale monodose che contengono nominalmente 500 1000 1500 2000 o 3000 UI di FVIII. Ogni fiala di Esperoct è etichettata con l'attività FVIII effettiva. Dopo la ricostituzione con il diluente fornito (NULL,9% salino) ogni ml della soluzione contiene rispettivamente circa 125 250 375 500 o 750 UI di FVIII.
La proteina FVIII in Esperoct è prodotta nelle cellule di ovaio del criceto cinese (CHO) usando la tecnologia del DNA ricombinante e contiene un dominio B troncato che è O-glicosilato. La parte polipeptidica della molecola ha una massa molecolare di 166 kDa (calcolata esclusa le modifiche post-traduzionali) e rappresenta un eterodimero di una catena pesante e una catena leggera che sono tenute insieme da interazioni non covalenti. La proteina FVIII ricombinante viene purificata usando una serie di passaggi cromatografici, una delle quali è la cromatografia di affinità con l'uso di un anticorpo monoclonale per isolare selettivamente l'RFVIII dal terreno di coltura cellulare. La molecola PEG a 40 kDa è coniugata alla porzione di O-glicano del dominio B usando una reazione enzimatica per produrre un FVIII glicopegica (FVIII-PEG). Il processo di purificazione include due fasi di clearance virale, vale a dire il trattamento di detergente (Triton X-100) per l'inattivazione di virus avvolti e filtrazione a 20 nm per la rimozione di virus avvolti e non avvolti. Non sono usati additivi di origine umana o animale durante il processo di produzione e la formulazione di Esperoct.
Nella circolazione sanguigna quando FVIII-PEG è attivato dalla trombina, la porzione di dominio B con la porzione di PEG attaccata viene scissa e il FVIII attivato risultante (FVIIIa) è simile nella struttura e nella funzione a FVIIIa nativa.
Usi per esperoct
Esperoct ® [fattore antiemofilico (ricombinante) glicopegylated- exei] è un concentrato di coagulazione VIII ricombinante derivato dal DNA indicato per l'uso in adulti e bambini con emofilia A per:
- Trattamento su richiesta e controllo degli episodi di sanguinamento
- Gestione perioperatoria del sanguinamento
- Profilassi di routine per ridurre la frequenza degli episodi di sanguinamento
Limitazione dell'uso
Esperoct ® non è indicato per il trattamento della malattia di von Willebrand. (1)
Dosaggio per esperoct
Per infusione endovenosa solo dopo la ricostituzione.
Dose
- Il dosaggio e la durata del trattamento dipendono dalla gravità della carenza del fattore VIII dalla posizione e dall'estensione del sanguinamento e dalla condizione clinica del paziente. È necessario un attento monitoraggio della terapia sostitutiva in caso di chirurgia grave o episodi di sanguinamento potenzialmente letale.
- Ogni fiala di esperoct ® Contiene la quantità etichettata di fattore VIII ricombinante nelle unità internazionali (IU). Una IU dell'attività del fattore VIII corrisponde alla quantità di fattore VIII in un millilitro di plasma umano normale. Il calcolo del dosaggio richiesto del fattore VIII si basa sulla scoperta empirica che una IU del fattore VIII per kg di peso corporeo aumenta l'attività del fattore VIII plasmatico di due UI/DL.
Trattamento on -demand e controllo degli episodi di sanguinamento
La tabella 1 può essere utilizzata per guidare il dosaggio di Esperoct ® Per il trattamento degli episodi di sanguinamento.
Tabella 1: dosaggio di esperoct ® Per controllare gli episodi di sanguinamento
| Tipo di sanguinamento | Adolescenti/ adulti ≥12 anni Dose (IU/kg) | Bambini <12 years Dose (IU/kg) | Dosi aggiuntive |
| Minore | |||
| Emartrosi precoce Sanguinamento muscolare lieve o sanguinamento orale | 40 | 65 | Una dose dovrebbe essere sufficiente |
| Moderare | |||
| Emartrosi più estesa sanguinamento muscolare o ematoma | 40 | 65 | Una dose aggiuntiva può essere somministrata dopo 24 ore |
| Maggiore | |||
| Emorragia per la vita o per le letali | 50 | 65 | Dose aggiuntive possono essere somministrate circa ogni 24 ore |
Gestione perioperatoria
Il livello di dose e gli intervalli di dosaggio per la chirurgia dipendono dalla procedura e dalla pratica locale. Una guida per il dosaggio con Esperoct ® Durante l'intervento chirurgico (gestione perioperatoria) è fornita nella Tabella 2 di seguito.
Tabella 2: dosaggio per la gestione perioperatoria con Esperoct ®
| Tipo di chirurgia | Adolescenti/ adulti ≥12 anni Pre-operative Dose (IU/kg) | Bambini <12 years Pre-operative Dose (IU/kg) | Dosi aggiuntive |
| Minore | |||
| Compresa l'estrazione dei denti | 50 | 65 | Dose aggiuntive possono essere somministrate dopo 24 ore, se necessario |
| Maggiore | |||
| Chirurgia intra-addominale intra-addominale intracranica | 50 | 65 | Dosi aggiuntive can be administered approximately every 24 hours for the first week E then approximately every 48 hours until wound healing has occurred |
Profilassi di routine
Adulti e adolescenti (≥ 12 anni): la dose di partenza raccomandata è 50 UI di Esperoct ® per kg di peso corporeo ogni 4 giorni.
Questo regime può essere regolato individualmente a un dosaggio inferiore o più frequente in base a episodi di sanguinamento.
Bambini ( <12 years): A dose of 65 IU of Esperoct ® per kg di peso corporeo due volte alla settimana. Questo regime può essere regolato individualmente a un dosaggio inferiore o più frequente in base a episodi di sanguinamento.
Dosaggio (IU) = peso corporeo (kg) × fattore VIII desiderato (IU/dl o % normale) × 0,5
- Esperoct ® Possono anche essere dosato per raggiungere un livello di attività target VIII specifico a seconda della gravità dell'emofilia per il trattamento/controllo su richiesta degli episodi di sanguinamento o della gestione perioperatoria. Per ottenere un livello di attività target VIII specifico, utilizzare la seguente formula:
- Basare la dose e la frequenza di esperoct ® Sulla risposta clinica individuale. I pazienti possono variare nelle loro risposte farmacocinetiche e cliniche.
- Se viene eseguito il monitoraggio dell'attività del fattore VIII, utilizzare un test di coagulazione cromogenica o a una fase appropriata per l'uso con ESPEROCT ® [Vedere Avvertimenti e precauzioni ].
Preparazione e ricostituzione
- Lavare sempre le mani e assicurarsi che l'area sia pulita prima di eseguire le procedure di ricostituzione.
- Utilizzare la tecnica asettica durante le procedure di ricostituzione.
- Se la dose richiede più di una fiala di esperoct ® per infusione ricostituire ogni fiala secondo le seguenti istruzioni.
Panoramica di Esperoct ® Pacchetto
Panoramica
Fial con Esperoct ® polvere
| ® powder - Illustration' src='//pharmacie-hoffer.eu/img/coagulation-factors/92/esperoct.webp' > |
Ricostituzione
| ® vial and the pre-filled diluent syringe to room temperature. - Illustration' src='//pharmacie-hoffer.eu/img/coagulation-factors/92/esperoct-1.webp' > |
| ® vial. - Illustration' src='//pharmacie-hoffer.eu/img/coagulation-factors/92/esperoct-2.webp' > |
 |
| ® Fial su una superficie piana e solida. Mentre si tiene in mano il cappuccio protettivo posizionare l'adattatore della fiala sopra l'Esperoct ® vial and press down firmly on the protective cap until the vial adapter spike penetrates the rubber stopper. - Illustration' src='//pharmacie-hoffer.eu/img/coagulation-factors/92/esperoct-4.webp' > |
 |
 |
 |
 |
 |
| ® vial until all of the powder is dissolved. Avoid shaking the vial and foaming the solution. - Illustration' src='//pharmacie-hoffer.eu/img/coagulation-factors/92/esperoct-10.webp' > |
- Porta l'Esperoct ® Fial e la siringa diluente pre-riempita a temperatura ambiente.
- Rimuovere il tappo di plastica dall'esperoct ® Fial.
- Pulisci il tappo di gomma sulla fiala con un tampone di alcol sterile e lascialo asciugare prima dell'uso.
- Rimuovere la carta protettiva dall'adattatore della fiala. Non rimuovere l'adattatore della fiala dal cappuccio protettivo.
- Posizionare l'Esperoct ® Fial su una superficie piana e solida. Mentre si tiene in mano il cappuccio protettivo posizionare l'adattatore della fiala sopra l'Esperoct ® Fial e premere saldamente verso il basso sul tappo protettivo fino a quando l'adattatore di fiala picchi non penetra nel tappo di gomma.
- Rimuovere con cura il cappuccio protettivo dall'adattatore della fiala.
- Afferrare l'asta dello stantuffo come mostrato nel diagramma. Collegare l'asta dello stantuffo alla siringa tenendo l'asta dello stantuffo dall'estremità superiore. Trasforma l'asta dello stantuffo in senso orario nello stantuffo di gomma all'interno della siringa di diluente pre-riempita fino a quando non viene avvertita la resistenza.
- Rompere il cappuccio della siringa dalla siringa diluente pre-riempita scattando la perforazione del cappuccio.
- Collegare la siringa di diluente pre-riempita all'adattatore Fial ruotandola in senso orario fino a quando non è fissata.
- Spingere l'asta dello stantuffo per iniettare lentamente tutto il diluente nella fiala.
- Senza rimuovere la siringa di rotazione delicatamente ® Fial fino a quando tutta la polvere non viene sciolta. Evita di scuotere la fiala e schivare la soluzione.
Amministrazione
Solo per infusione endovenosa
- I prodotti farmaceutici parenterali devono essere ispezionati visivamente per il particolato e lo scolorimento prima della somministrazione ogni volta che la soluzione e il permesso del contenitore. La soluzione dovrebbe essere chiara e non avere particelle. Non utilizzare se si osserva il particolato o lo scolorimento.
- Non somministrare Esperoct ® nello stesso tubo o contenitore con altri prodotti medicinali.
- Amministrare l'esperoct ® soluzione immediatamente. Se non conservare la soluzione nella fiala con l'adattatore di fiala e la siringa attaccata. Usa Esperoct ® Entro 4 ore se conservato a ≤86 ° F (30 ° C) o entro 24 ore se conservato in frigorifero da 36 ° F a 46 ° F (da 2 ° C a 8 ° C).
| ® vial and slowly draw the solution into the syringe. - Illustration' src='//pharmacie-hoffer.eu/img/coagulation-factors/92/esperoct-11.webp' > |
- Invertire l'esperoct ® Fial e disegnare lentamente la soluzione nella siringa.
- Staccare la siringa dall'adattatore della fiala ruotando la siringa in senso antiorario.
- Attaccare la siringa all'estremità luer di un set di ago per infusione.
- Infondere l'esperoct ricostituito ® endovenoso lentamente per circa 2 minuti.
- Dopo l'infusione smaltire in modo sicuro la siringa con l'infusione imposta la fiala con l'adattatore di fiala qualsiasi esperoct inutilizzato ® e altri materiali di scarto.
Attenzione
La siringa di diluente pre-riempita è realizzata in vetro con un diametro della punta interno di 0,037 pollici ed è compatibile con un connettore Luer-Lock standard.
Alcuni connettori senza bisogni per cateteri endovenosi sono incompatibili con le siringhe diluenti di vetro (ad esempio alcuni connettori con un picco interno come la clave ® /Microclave ® Invision-plus ® Invision-plus CS ® Invision-plus junior ® Bionector ® ) e il loro uso può danneggiare il connettore e influire sulla somministrazione. Per somministrare Esperoct ® Attraverso i connettori incompatibili senza nemico, ritirano il prodotto ricostituito in una siringa di plastica Luer-Lock sterile standard da 10 ml.
Come fornito
Forme di dosaggio e punti di forza
Esperoct ® è disponibile come bianco sterile a polvere liofilizzata off-bianca fornita in fiale monodosi contenenti nominalmente 500 1000 1500 2000 o 3000 UI. L'attività FVIII effettiva è stampata su ciascun esperoct ® Fial e cartone.
Dopo la ricostituzione con 4 ml di diluente salino, la soluzione ricostituita contiene circa 125 250 375 500 o 750 UI per ml di Esperoct ® rispettivamente.
- Esperoct ® è fornito in pacchetti composti da una fiala monodose contenente nominalmente 500 1000 1500 2000 o 3000 UI dell'attività del fattore VIII; un mixpro ® Siringa di diluente pre-riempita contenente soluzione salina allo 0,9%; e un adattatore di fiala sterili con un filtro da 25 micrometri che funge da dispositivo di ricostituzione senza bisogno.
- L'attività effettiva del fattore VIII in IU è indicata su ciascun esperoct ® cartone e etichetta della fiala.
Tabella 9: Esperoct ® Presentazioni
| Forza di dosaggio nominale | Indicatore di colore del cappuccio | Cartone Ndc Numero | Componenti |
| 500 UI | Rosso | Ndc 0169 8500 01 |
|
| 1000 UI | Verde | Ndc 0169 8100 01 |
|
| 1500 UI | Grigio | Ndc 0169 8150 01 |
|
| 2000 UI | Giallo | Ndc 0169 8200 01 |
|
| 3000 IU | Nero | Ndc 0169 8300 01 |
|
| Iu = unità internazionali |
- L'esperoct ® Le fiale sono realizzate in vetro chiuso con un tappo di gomma clorobutilico (non realizzato con lattice di gomma naturale) e sigillate con un cappuccio di alluminio.
- Le siringhe di diluenti pre-riempite sono realizzate in vetro con uno stantuffo di gomma bromobutil siliconizzato (non fatto con lattice in gomma).
- Le fiale chiuse e le siringhe di diluenti pre-riempite sono dotate di un tappo a snap-off evidente di manomissione che è realizzato in polipropilene.
Archiviazione e maneggevolezza
- STORING ESPEROCT ® Nel pacchetto originale per proteggere l'esperoct ® Fial dalla luce.
- STORING ESPEROCT ® In una polvere a forma di refrigerazione da 36 ° F a 46 ° F (da 2 ° C a 8 ° C) per un massimo di 30 mesi dalla data di produzione fino alla data di scadenza dichiarata sull'etichetta. Durante la durata di 30 mesi Esperoct ® può essere mantenuto a temperatura ambiente:
- fino a 86 ° F (30 ° C) per non più di 12 mesi o
- fino a 104 ° F (40 ° C) per non più di 3 mesi
- Registra la data sul cartone quando il prodotto è stato rimosso dal frigorifero. Non restituire il prodotto al frigorifero.
- Non congelare Esperoct ® .
- Usa l'attesa ® Entro 4 ore dalla ricostituzione se conservato a ≤86 ° F (30 ° C) o entro 24 ore quando conservato in frigorifero. Conservare il prodotto ricostituito nella fiala.
- Scartare qualsiasi prodotto ricostituito inutilizzato.
Prodotto da: Novo Nordisk A/S DK-2880 Bagsvaerd Danimarca. Revisionato: settembre 2022
quanto wellbutrin è in contrasto
Effetti collaterali per Esperoct
Le reazioni avverse più frequentemente riportate (incidenza ≥1%) negli studi clinici sono state il prurito di arrossamento (prurito) e le reazioni del sito di iniezione.
Esperienza di studi clinici
Poiché gli studi clinici sono condotti in condizioni di reazione avverse ampiamente variabili osservate negli studi clinici di un farmaco non possono essere confrontati direttamente ai tassi negli studi clinici di un altro farmaco e potrebbero non riflettere i tassi osservati nella pratica clinica.
La sicurezza di Esperoct ® è stato valutato in 270 soggetti (202 adolescenti/adulti e 68 bambini) in cinque studi clinici multicentrici prospettici in pazienti precedentemente trattati (PTP) con grave emofilia A ( <1% endogenous FacAr VIII activity) E no hisAry of inhibiArs. All subjects received at least one dose of Esperoct ® . Un paziente precedentemente trattato è stato definito come soggetto con una storia di almeno 150 giorni di esposizione ad altri prodotti del fattore VIII (soggetti adolescenti/adulti) o 50 giorni di esposizione ad altri prodotti del fattore VIII (soggetti pediatrici). Esposizione totale a Esperoct ® era 80425 giorni di esposizione corrispondenti a 889 anni di trattamento.
Durante gli studi clinici nelle reazioni avverse PTP si sono verificate ad un tasso di 0,10 eventi per anno di esposizione al paziente. Le reazioni avverse più frequentemente riportate sono state la reazione del sito di iniezione eruzione (NULL,2%) (NULL,6%) arrossamento (NULL,9%) e prurito (prurito) (NULL,5%).
Immunogenicità
I soggetti sono stati monitorati per gli anticorpi neutralizzanti e non neutralizzanti ai fattori VIII polietilenglicole (PEG) e alla proteina delle cellule ospiti CHO. Un soggetto precedentemente trattato ha sviluppato anticorpi neutralizzanti confermati ai fattori VIII (NULL,5 unità Bethesda). Inoltre, due soggetti avevano anticorpo FVIII a bassa titolo transitorio ( <5 Bethesda Units) test results at a single occasion. Anti-PEG antibodies of no clinical consequence were detected in 45 subjects 32 of whom had pre-existing anti-PEG antibodies. Nine subjects developed anti-CHO host cell protein antibodies of no clinical consequence.
Il rilevamento di anticorpi dipende fortemente dalla sensibilità e dalla specificità del test. Inoltre, l'incidenza osservata dell'anticorpo (compresa l'anticorpo neutralizzante) in un test può essere influenzata da diversi fattori tra cui la metodologia del test, i tempi di gestione dei campioni dei farmaci concomitanti di raccolta del campione e la malattia sottostante.
Esperienza post -marketing
Le seguenti reazioni avverse sono state identificate durante la post-approvazione di Esperoct ® . Poiché queste reazioni sono riportate volontariamente da una popolazione di dimensioni incerte, non è sempre possibile stimare in modo affidabile la loro frequenza o stabilire una relazione causale con l'esposizione ai farmaci.
Diminuzione dell'attività del fattore VIII: sono state segnalate una ridotta attività del fattore VIII in assenza di inibitori del fattore VIII rilevabili nei pazienti precedentemente trattati (PTP) al passaggio all'esperoct ® da altri prodotti di fattore VIII.
Interazioni farmacologiche per esperoct
Nessuna informazione fornita
Avvertimenti per Esperoct
Incluso come parte del 'PRECAUZIONI' Sezione
Precauzioni per Esperoct
Reazioni di ipersensibilità
Sono possibili reazioni di ipersensibilità di tipo allergico con anafilassi con esperoct ® . Il prodotto contiene tracce di proteine del criceto che in alcuni pazienti possono causare reazioni allergiche [vedi DESCRIZIONE ]. Early signs of allergic reactions which can progress A anaphylaxis may include angioedema tenuta toracica Difficoltà a respirare sibilante eruzione cutanea orticaria E prurito. Observe patients for signs E sympAms of acute hypersensitivity reactions particularly during the early phases of exposure A the product. Discontinue use of Esperoct ® Se si verificano reazioni di tipo allergico o anafilattico e iniziano un trattamento adeguato.
Anticorpi neutralizzanti
La formazione di anticorpi neutralizzanti (inibitori) al fattore VIII si è verificata dopo la somministrazione di esperoct ® . Monitorare i pazienti per lo sviluppo di inibitori del fattore VIII da parte di appropriate osservazioni cliniche e test di laboratorio. Se il fattore VIII previsto i livelli plasmatici non vengono raggiunti o se il sanguinamento non è controllato dopo l'esperoct ® la somministrazione sospetta la presenza di un inibitore (anticorpo neutralizzante) [vedi Monitoraggio dei test di laboratorio ].
Monitoraggio dei test di laboratorio
Se viene eseguito il monitoraggio del fattore VIII, utilizzare un test di coagulazione cromogenica o uno stadio appropriato per l'uso con ESPEROCT ® [Vedere Dosaggio e amministrazione ].
I livelli di attività del fattore VIII possono essere influenzati dal tipo di reagente di tempo di tromboplastina parziale attivato (APTT) utilizzato nel test. Alcuni reagenti APTT a base di silice possono sottovalutare l'attività di Esperoct ® fino al 60%; Altri reagenti possono sopravvalutare l'attività del 20%. Se un coagulazione a una fase appropriata o un test cromogenico non è disponibile localmente, utilizzare un laboratorio di riferimento.
Se il sanguinamento non è controllato con la dose raccomandata di Esperoct ® o se i livelli di attività del fattore VIII previsto nel plasma non vengono raggiunti, eseguire un test BETHESDA per determinare se sono presenti inibitori del fattore VIII.
Informazioni sulla consulenza del paziente
Consigli sui pazienti:
- Per leggere l'etichettatura dei pazienti approvata dalla FDA ( Informazioni sul paziente E Istruzioni per l'uso ).
- Quelle reazioni di ipersensibilità di tipo allergico o anafilassi sono possibili con l'uso di esperoct ® . Informare i pazienti dei primi segni di reazioni di ipersensibilità, tra cui orticaria erutta che proseguono la tenuta del gonfiore del viso e si respirano. Consiglia ai pazienti di interrompere l'uso di esperoct ® immediatamente e contattare il proprio medico e/o cercare tempestivamente le cure di emergenza se si verificano questi sintomi.
- Contattare il proprio operatore sanitario o struttura di trattamento per ulteriori cure e/o valutazioni se subiscono una mancanza di una risposta clinica alla terapia sostitutiva del fattore VIII in quanto questa può essere una manifestazione di un inibitore.
Tossicologia non clinica
Mutagenesi della carcinogenesi compromissione della fertilità
La mutagenesi della carcinogenesi e la compromissione degli studi sulla fertilità negli animali non sono stati eseguiti.
Utilizzare in popolazioni specifiche
Gravidanza
Riepilogo del rischio
Non ci sono dati con Esperoct ® Uso nelle donne in gravidanza per determinare se esiste un rischio associato al farmaco. Studi di riproduzione degli animali non sono stati condotti con Esperoct ® . Non è noto se esperoct ® può causare danni fetali quando somministrato a una donna incinta o può influire sulla fertilità.
Nella popolazione generale degli Stati Uniti il rischio di background stimato di maggiore Difetto alla nascita E miscarriage in clinically recognized pregnancies is 2–4% E 15–20% rispettivamente.
Lattazione
Riepilogo del rischio
Non ci sono informazioni sulla presenza di Esperoct ® Nel latte umano l'effetto sul bambino allattato al seno e sugli effetti sulla produzione di latte. I benefici per lo sviluppo e la salute dell'allattamento dovrebbero essere considerati insieme alla necessità clinica della madre di Esperoct ® E any potential adverse effects on the breastfed infant from Esperoct ® o dalla condizione materna sottostante.
Uso pediatrico
La sicurezza e l'efficacia sono state valutate in 93 pazienti pediatrici precedentemente trattati <18 years of age who received at least one dose of Esperoct; all received routine prophylaxis [Vedere Studi clinici ]. Thirty-four (34) of these subjects (36.6%) were 1 a <6 years of age; 34 subjects (36.6%) were 6 a <12 years of age; E 25 subjects (27%) were 12 a <18 years of age. Pharmacokinetic parameters were evaluated for 27 of these subjects who were treated with Esperoct ® [Vedere Farmacologia clinica ].
Nessuna differenza nel profilo di sicurezza di Esperoct ® è stato osservato tra soggetti pediatrici precedentemente trattati e soggetti adulti. Studi di farmacocinetica nei bambini <12 years of age demonstrated higher clearance a shorter half-life E lower incremental recovery of FacAr VIII compared A adults but the pharmacokinetic parameters are comparable between young children (1– <6 years) E older children (6- <12 years). Because clearance (per kg body weight) is higher in children ( <12 years) a higher dose E more frequent dosing may be needed in this population [Vedere Farmacologia clinica ].
Uso geriatrico
Studi clinici su esperoct ® non includeva un numero sufficiente di soggetti di età pari o superiore a 65 anni per determinare se rispondono o meno in modo diverso rispetto ai soggetti più giovani. Altra esperienza clinica segnalata non ha identificato differenze nelle risposte tra i pazienti anziani e più giovani. In generale, la selezione della dose per un paziente anziano dovrebbe essere cauta di solito a partire dalla fascia bassa dell'intervallo di dosaggio che riflette la maggiore frequenza della ridotta funzione renale e cardiaca epatica e di malattia concomitante e altre terapia farmacologica.
Informazioni per overdose per Esperoct
Nessuna informazione fornita
Controindicazioni per Esperoct
Esperoct ® è controindicato nei pazienti che hanno conosciuto ipersensibilità all'esperoct ® o i suoi componenti (comprese le proteine del criceto) [vedi Avvertimenti e precauzioni E DESCRIZIONE ].
Farmacologia clinica for Esperoct
Meccanismo d'azione
Esperoct ® Una forma glicopegopica di fattore anti-emofilo ricombinante sostituisce temporaneamente il fattore VIII di coagulazione mancante necessario per l'efficacia efficace nell'emofilia congenita A. Il fattore VIII in Esperoct ® è coniugata con una molecola di glicole polietilenico da 40 kDa che aumenta l'emivita e riduce la clearance rispetto alla molecola non pegilata.
Farmacodinamica
La somministrazione di esperoct ® Aumenta i livelli plasmatici del fattore VIII e può temporaneamente correggere il difetto di coagulazione nell'emofilia A dei pazienti come riflessi da una diminuzione del tempo di tromboplastina parziale attivato (APTT).
Farmacocinetica
Tutti gli studi farmacocinetici con Esperoct ® sono stati condotti in soggetti precedentemente trattati con grave emofilia A (fattore VIII <1%). In Atal 129 single-dose pharmacokinetic profiles of Esperoct ® sono stati valutati in 86 soggetti (inclusi 24 soggetti pediatrici 1– <12 years).
La tabella 3 mostra i dati per i soggetti che hanno ricevuto ciascuno una singola dose di 50 UI/kg. I campioni di plasma sono stati analizzati utilizzando il test di coagulazione a una fase. Vi è stata una tendenza all'aumento del recupero incrementale e all'AUC e alla riduzione della clearance con l'età.
Tabella 3: parametri PK monodose di Esperoct ® 50 UI/kg per età usando un test di coagulazione a uno stadio (media geometrica (CV%))
| Parametro PK | 1 a <6 years | 6 a <12 years | 12 a <18 years | > 18 anni |
| No. di soggetti | N = 12 | N = 10 | N = 3 | N = 42 |
| No. di profili | 12 | 10 | 5 | 78 |
| Ir (iu / d d d di) per i / kg) a | 1.82 (32) | 1.67 (22) | 2.45 (16) | 2,53 (24) |
| FVIII Recovery (IU/DL) a | 103.2 (27) | 98.7 (18) | 117.7 (14) | 130.4 (26) |
| t 1/2 (ore) | 14.7 (27) | 13,8 (32) | 17.4 (39) | 21.7 (33) |
| Aucinf (iu*hour/dl) | 2305 (42) | 2197 (38) | 3063 (40) | 4110 (38) |
| CL (ml/ora/kg) | 2.4 (42) | 2.7 (42) | 1.6 (39) | 1.2 (34) |
| VSS (ml/kg) | 44.2 (25) | 47.3 (28) | 36.4 (12) | 37,3 (26) |
| MRT (ore) | 18.1 (27) | 17,8 (35) | 23.4 (43) | 27.4 (28) b |
| I parametri PK sono presentati in media geometrica. Abbreviazioni: IR = recupero incrementale; T 1/2 = emivita terminale; AUC = area sotto il profilo del tempo di attività FVIII; Cl = clearance; VSS = volume di distribuzione allo stato stazionario; MRT = tempo di permanenza medio; CV% = coefficiente di variazione a Il recupero IR e FVIII è stato valutato 30 minuti post-dosaggio 50 UI/kg per pazienti ≥12 anni e 60 minuti dopo la dosaggio 50 UI/kg (primo campione) per bambini <12 years. bCalculation based on 64 profiles. |
Nella valutazione di PK monodose in soggetti adulti il cui indice di massa corporea (BMI) variava da 17-35 kg/m 2 Sono state notate differenze per le persone in sovrappeso (BMI 25 - <30 kg/m 2 ) e obesi (BMI 30 - <35 kg/m 2 ). Incremental recovery was increased by approximately 17% E 41% AUC was increased by approximately 10% E 27% E clearance was decreased by approximately 8% E 23% respectively all in comparison A those subjects with BMI <25 kg/m 2 . Non ci sono dati sufficienti per raccomandare adeguamenti di dose specifici per i pazienti in sovrappeso e obesi. La dose può essere regolata se necessario per discrezione del prescrittore.
I livelli di attività del fattore plasmatico pre-dosi (depressione) e post-dose (picco) livelli di attività allo stato stazionario durante il trattamento profilattico con ESPEROCT ® sono presentati nella Tabella 4 per regime di dose e fascia d'età.
Tabella 4: Attività FVIII di depressione allo stato stazionario e di picco mediante test cromogenico per età e dose (media geometrica [IC 95% IC])
può essere tagliato a metà Belsomra
| Dose Regimen | 60 UI/kg due volte alla settimana ** (50–75 UI/kg) | 50 UI/kg Q4d* | 75 IU/kg Q7D* | |||
| Fascia d'età | <6 years | 6- <12 years | 12- <18 years | ≥18 anni | 12- <18 years | ≥18 anni |
| No. pazienti | N = 31 | N = 34 | N = 23 | N = 143 | N = 6 | N = 29 |
| Trough iu/dl | 1.2 (NULL,8; 1,6) | 2.0 (1.5; 2.7) | 2.7 (1.8; 4.0) | 3.0 (2.6; 3.5) | 0.6 (NULL,2; 1,6) | 1.3 (0.9; 2.0) |
| Picco iu/dl | 125.0 (118.7; 131.6) | 143.3 (136.8; 150.2) | 125.1 (116.0; 135.0) | 137.9 (NULL,9; 142.2) | 198.0 (166.8; 235.2) | 197.9 (184.9; 212.7) |
| *Dati inclusi nell'analisi: adolescenti/adulti Fase principale fino alla visita 8 (fine della fase principale) 50 UI/kg Q4d ed estensione 1 per 75 UI/kg Q7D. Nelle analisi sono incluse solo le misurazioni raccolte allo stato stazionario per il trattamento di profilassi dato. ** Dati inclusi nell'analisi: fase principale pediatrica 60 UI/kg (50–75 UI/kg) due volte a settimana. Nelle analisi sono incluse solo le misurazioni raccolte allo stato stazionario per il trattamento di profilassi dato. |
Tempo del fattore VIII Attività superiore al 5%
I profili di attività del fattore VIII a stato stazionario sono stati stimati utilizzando un modello a un compartimento con eliminazione del primo ordine con parametri PK di clearance (CL) e volume di distribuzione (Tabella 5). Le previsioni farmacocinetiche hanno mostrato che in tutte le fasce di età i pazienti dosati due volte a settimana (intervallo di dosaggio alternato tra 3 e 4 giorni) o Q4d sarà superiore al 5% di attività del fattore VIII (cioè nell'intervallo di emofilia lieve) per la maggior parte del tempo (72-95% di tempo). I pazienti dosati con 50 UI/kg ogni 4 giorni saranno superiori all'attività del fattore VIII al di sopra dell'1% del 100% dell'intervallo di dosaggio. Si prevede che i pazienti dosati con 75 UI/kg ogni 7 giorni siano superiori al 5% per il 57% del tempo e superiore all'1% per l'83% del tempo.
Tabella 5: stima del picco di stato stazionario e dell'attività FVIII e del tempo al 5% di attività FVIII per esperoct ®
| Dose regimen | 60 UI/kg (50–75 UI/kg) due volte alla settimana | 50 UI/kg due volte alla settimana | 50 UI/kg Q4D | 75 IU/kg Q7D |
| Fascia d'età | <12 years | ≥12 anni | ≥12 anni | ≥12 anni |
| Attività di picco FVIII (%) | 110/112* | 133/138* | 132 | 194 |
| Trough FVIII Activity (%) | 2,8/0,8* | 8.6/3.6* | 3.5 | 0.3 |
| Tempo al 5% di attività FVIII (giorni) | 2,5/2,5* | 3.6/3.6* | 3.6 | 4.0 |
| % del tempo nell'intervallo di dosaggio superiore al 5% di attività FVIII | 72 | 95 | 90 | 57 |
| *I valori due volte settimanali sono mostrati come 3 giorni/4 giorni. Per l'analisi vengono utilizzati solo 50 dati UI/kg. |
Tossicologia animale e/o farmacologia
Non sono stati osservati effetti avversi nei ratti carenti immuno iniettati per via endovenosa con esperoct ® (50-1200 UI/ kg/ iniezione) una volta ogni 4 ° giorno per 52 settimane. Non è stata rilevata alcuna evidenza di accumulo di polietilenglicole mediante colorazione immunoistochimica del tessuto cerebrale incluso il plesso coroideo.
Studi clinici
La sicurezza e l'efficacia di Esperoct ® sono stati valutati in cinque studi multinazionali in aperto su soggetti maschili con grave emofilia A ( <1% endogenous FacAr VIII activity). One trial was subsequently partially rEomized A evaluate two different prophylaxis regimens. All subjects were previously treated which was defined as having received other FacAr VIII products for ≥150 exposure days for adolescents E adults E ≥50 exposure days for pediatric subjects. The key exclusion criteria across trials included known or suspected hypersensitivity A trial or related products E known hisAry of FacAr VIII inhibiArs or current inhibiAr ≥0.6 Bethesda units (BU).
La valutazione dell'efficacia includeva 254 soggetti che hanno ricevuto almeno una dose di Esperoct ® Nelle seguenti prove:
- Prova adolescenziale/adulto: questo studio includeva 186 soggetti 161 adulti (dai 18 ai 65 anni) e 25 adolescenti (da 12 a <18 years old); it consisted of a Main Phase E optional Extension Phase. During the Main Phase 175 subjects received the prophylaxis regimen which consisted of 50 UI/kg every 4 days (Q4D) while 12 adults chose A be treated on-demE. (One subject changed from on-demE A prophylaxis E is counted in both groups.) Thirteen (7%) of 175 adults in the prophylaxis arm modified their dosing regimen A Q3-4D dosing for ease of use. All subjects received at least one dose of Esperoct ® E are evaluable for safety E efficacy. A Atal of 165 subjects (91%) completed the Main Phase of this trial.
- Estensione: questa estensione ha confrontato due regimi di dose: 75 UI/kg ogni 7 giorni (Q7D) e 50 UI/kg Q4D. La randomizzazione è stata aperta a soggetti che hanno subito 2 o meno sanguinamenti negli ultimi 6 mesi nella fase principale.
- Prova pediatrica: questo studio includeva 68 soggetti che erano uniformemente divisi con 34 in ogni fascia di età 0– <6 E 6- <12 years of age. All subjects received the same prophylaxis regimen of approximately 65 IU/kg (50–75 UI/kg) due volte alla settimana. A Atal of 63 subjects (93%) completed the Main Phase.
- Studio chirurgico: nella sperimentazione chirurgica 33 adolescenti/adulti precedentemente trattati hanno subito 45 gravi interventi chirurgici. Il livello di dose di esperoct ® è stato scelto in modo tale che l'attività FVIII sia stata mirata almeno come raccomandata dalle linee guida della Federazione mondiale della Emofilia (WFH). Tutti i soggetti sono tornati alla sperimentazione adolescenziale/adulta dopo il completamento delle valutazioni della sperimentazione chirurgica.
Trattamento su richiesta e controllo degli episodi di sanguinamento
Sono stati riportati 1506 sanguinamenti in 171 su 254 soggetti negli studi clinici completati e i tipi di spurgo più comuni erano muscoli articolari (NULL,2%) (NULL,5%) e sottocutanei (NULL,9%). La tabella 6 riassume l'efficacia nel controllo degli episodi di sanguinamento per età.
Doses used for treatment of bleeding episodes depended on age treatment regimen E the severity of the bleed.
Degli episodi di sanguinamento lievi e moderati del 1407 in tutti i soggetti nello studio adolescenziale/adulto, la dose mediana utilizzata era di 42 UI/kg. Per i soggetti che erano sul braccio on-demand la dose iniziale mediana era di 28 UI/kg e l'88,4% delle sanguinamenti venivano trattate con successo con una singola dose. Nei soggetti che ricevevano profilassi di routine la dose iniziale mediana era di 52 UI/kg e il 76,4% delle sanguinamenti sono stati trattati con successo con una singola dose. Dei 15 gravi sanguinamenti 12 (80%) hanno richiesto più di una dose con una dose mediana totale di 111 UI/kg.
Nello studio pediatrico 70 sanguinamenti lievi/moderati nei bambini <12 years old receiving routine prophylaxis were treated with a median initial dose of 64 IU/kg per injection with 63% treated with a single injection. When needed additional median doses of 62 IU/kg were used at approximately 24 hour intervals. The median Atal dose was 70 IU/kg per bleed.
Tabella 6: Riepilogo dell'efficacia nel controllo degli episodi sanguinanti per età
| Fascia d'età | <6 years N = 34 | 6 - <12 years N = 34 | 12 - <18 years N = 25 | ≥ 18 anni N = 161 | Totale N = 254 | |
| 30 | 40 | 112 | 1324 | 1506 | ||
| 1-2 | 76,7% | 82,5% | 88,4% | 95,5% | 94,3% | |
| > 2 | 23,3% | 17,5% | 11,6% | 4,5% | 5,7% | |
| Risposta al primo trattamento | Eccellente/ buono | 80,0% | 77,5% | 75,0% | 88,7% | 87,3% |
| Moderare | 13,3% | 17,5% | 17,9% | 10,3% | 11,1 % | |
| Definizione di risposta emostatica: Eccellente: brusco sollievo dal dolore e/o inequivocabile miglioramento dei segni oggettivi di sanguinamento entro circa 8 ore dopo una singola iniezione. Bene: sollievo dal dolore definito e/o miglioramento nei segni di sanguinamento entro circa 8 ore dopo un'iniezione, ma eventualmente richiede più di un'iniezione per una risoluzione completa. Moderare: Probable or slight beneficial effect within approximately 8 hours after the first injection; usually requiring more than one injection. |
Gestione perioperatoria
L'analisi di efficacia di Esperoct ® Nella gestione perioperatoria includeva 45 principali procedure chirurgiche eseguite in 33 soggetti adolescenti e adulti. Le procedure includevano 15 sostituzioni articolari 9 interventi ortopedici artroscopici 17 altri interventi ortopedici e 4 interventi chirurgici non ortopedi.
La valutazione clinica della risposta emostatica durante la chirurgia maggiore è stata valutata utilizzando una scala a 4 punti di eccellente buon moderato o nessuno. L'effetto emostatico di Esperoct ® è stato valutato come eccellente o buono in 43 su 45 interventi chirurgici (NULL,6%) mentre l'effetto è stato valutato come moderato in 2 interventi chirurgici (NULL,4%). Nessun intervento chirurgico ha ottenuto un risultato classificato come nessuno o mancante.
La dose pre-operatoria mediana per adulti e adolescenti sottoposti a gravi interventi chirurgici era di 52 UI/ kg e la dose totale mediana era di 702 UI/ kg. Durante i giorni post-operatori 1-6 la dose mediana era di 32 UI/kg a intervalli di circa 24 ore. Durante i giorni post-operatori 7-14 la dose mediana era di 36 UI/kg a intervalli di circa 28 ore. Il numero di dosi e la durata del trattamento variavano in base alla procedura.
Profilassi di routine In Adolescents/Adults
L'efficacia di Esperoct ® Nella profilassi di routine con dosaggio Q4D è stata dimostrata per la popolazione adulta/ adolescenziale (vedere la Tabella 7). Nella parte dell'estensione del trattamento del trattamento dello studio il successo del braccio Q7D non è stato stabilito. Durante la fase principale della sperimentazione adolescenziale/adulta, 186 soggetti hanno avuto un totale di 159 anni di esposizione. La velocità di sanguinamento annualizzata mediana (ABR) per le sanguinamenti trattati negli adulti e negli adolescenti trattati ogni 4 giorni era 1,2 (IQR: 0,0: 4.3) e la media ABR era 3,0 (DS: 4.7). Quando includevano tutti i sanguinamenti (trattati e non trattati), l'ABR mediano era 1,2 (IQR: 0,0; 4,7) e l'ABR medio era 3,3 (DS: 4,9).
Tabella 7: Efficacia nella profilassi adolescenziale/adulta mediana e ABR media per regime di trattamento dell'età e tipo di sanguinamento
| Fascia d'età | Profilassi | On demand | ||
| 12-17 years | 18–70 anni | 12-70 years | 18–70 anni | |
| 25 | 150 | 175 | 12 | |
| Durata media del trattamento (anni) | 0.85 | 0.81 | 0.82 | 1.33 |
| Bleeds trattati | ||||
| with bleeds (%) | 19 (76) | 86 (57) | 105 (60) | 12 (100) |
| without bleeds (%) | 6 (24) | 64 (43) | 70 (40) | 0 |
| 67 | 369 | 436 | 532 | |
| Mediana ABR (IQR) | 2,2 (NULL,9; 4.7) | 1.2 (NULL,0; 3,7) | 1.2 (NULL,0; 4.3) | 30.9 (18.6; 38.5) |
| Mean ABR (SD) | 3.5 (3.9) | 2.9 (4.8) | 3.0 (4.7) | 31.9 (19.1) |
| Tutti i sanguinamenti (trattati e non trattati) | ||||
| with bleeds (%) | 19 (76) | 88 (59) | 107 (61) | 12 (100) |
| without bleeds (%) | 6 (24) | 62 (41) | 68 (39) | 0 |
| * | 72 | 386 | 458 | 536 |
| Mediana ABR (IQR) | 2,2 (NULL,9; 6,0) | 1.2 (NULL,0; 4.3) | 1.2 (NULL,0; 4.7) | 31.3 (18.6; 38.9) |
| Mean ABR (SD) | 3.7 (4.1) | 3.2 (5.1) | 3.3 (4.9) | 32.2 (19.1) |
| Bleed spontanei trattati | ||||
| with bleeds (%) | 11 (44) | 65 (43) | 76 (43) | 12 (100) |
| without bleeds (%) | 14 (56) | 85 (57) | 99 (57) | 0 |
| 30 | 221 | 251 | 415 | |
| Median ASBR (IQR) | 0,0 (NULL,0; 1,5) | 0,0 (NULL,0; 1,9) | 0,0 (NULL,0; 1,8) | 19.4 (12.1; 31.0) |
| Mean ASBR (SD) | 1.4 (2.4) | 1.8 (3.7) | 1.7 (3.5) | 24.5 (17.3) |
| Blesi traumatiche trattate | ||||
| with bleeds (%) | 16 (64) | 57 (38) | 73 (42) | 10 (83) |
| without bleeds (%) | 9 (36) | 93 (62) | 102 (58) | 2 (17) |
| 37 | 146 | 183 | 110 | |
| Mediana ATBR (IQR) | 1.3 (NULL,0; 2,6) | 0,0 (NULL,0; 1,4) | 0,0 (NULL,0; 1,7) | 4.3 (NULL,8; 9,9) |
| Media ATBR (SD) | 2.1 (2.9) | 1.1 (2.2) | 1.2 (2.3) | 6.1 (6.2) |
| Blesi articolari trattati | ||||
| with bleeds (%) | 16 (64) | 74 (49) | 90 (51) | 12 (100) |
| without bleeds (%) | 9 (36) | 76 (51) | 85 (49) | 0 |
| 37 | 288 | 325 | 309 | |
| AJBR mediana (IQR) | 1.2 (NULL,0; 2,8) | 0,0 (NULL,0; 2,8) | 0,9 (NULL,0; 2,8) | 19.4 (4.5; 28.8) |
| Mean AJBR (SD) | 1.8 (2.2) | 2.3 (4.3) | 2.2 (4.1) | 19.7 (15.1) |
| ABR = tasso di sanguinamento annualizzato; IQR = intervallo interquartile 25 ° percentile al 75 ° percentile; SD = deviazione standard; ASBR = velocità di sanguinamento spontaneo annuale; ATBR = velocità di sanguinamento traumatico annuale; AJBR = velocità di sanguinamento articolare annualizzato. *Riflette tutti i sanguinamenti riportati da pazienti, compresi quelli in cui non è stato somministrato alcun esperoct |
Profilassi di routine In Bambini <12 Years Of Age
Complessivamente 68 bambini sotto i 12 anni hanno ricevuto un trattamento profilattico con ESPEROCT ad una dose media di circa 65 UI/kg due volte a settimana. L'effetto profilattico di ESPEROCT è stato dimostrato con una velocità ABR mediana di 2,0 (IQR: 0,0; 2,8) e 2,0 (IQR: 0,0; 4.2) per sanguinamenti trattati e tutti i sanguinamenti rispettivamente (vedere la Tabella 8). La media ABR (SD) per le sanguinamenti trattati e tutte le sanguinamenti erano rispettivamente 3,1 (NULL,1) e 4,4 (NULL,7). Dei 68 bambini 22 (32%) non hanno sperimentato episodi di sanguinamento e 29 (43%) non hanno sperimentato episodi di sanguinamento che richiedevano il trattamento durante la fase principale della sperimentazione. Dei 13 soggetti con 17 giunti target documentati ai soggetti di base 10 (77%) e 14 giunti target (82%) non hanno avuto sanguinamenti durante la fase principale della sperimentazione.
Tabella 8: efficacia nella profilassi pediatrica mediana e media media per età e tipo di sanguinamento
| Fascia d'età | Median ASBR (IQR)Profilassi Regimen | ||
| <6 years** | 6 a <12 years | 0 a <12 years | |
| N = 34 | N = 34 | N = 68 | |
| Durata media del trattamento (anni) | 0.46 | 0.51 | 0.48 |
| Bleeds trattati | |||
| with bleeds (%) | 19 (56) | 20 (59) | 39 (57) |
| without bleeds (%) | 15 (44) | 14 (41) | 29 (43) |
| 30 | 40 | 70 | |
| Mediana ABR (IQR) | 1.9 (NULL,0; 2.1) | 2,0 (NULL,0; 3,9) | 2,0 (NULL,0; 2,8) |
| Mean ABR (SD) | 3.9 (9.7) | 2.3 (2.9) | 3.1 (7.1) |
| Tutti i sanguinamenti (trattati e non trattati) | |||
| with bleeds (%) | 20 (59) | 26 (77) | 46 (68) |
| without bleeds (%) | 14 (41) | 8 (24) | 22 (32) |
| * | 41 | 65 | 106 |
| Mediana ABR (IQR) | 2,0 (NULL,0; 4.0) | 2.0 (1.9; 6.0) | 2,0 (NULL,0; 4.2) |
| Mean ABR (SD) | 5.0 (11.9) | 3.8 (3.6) | 4.4 (8.7) |
| Bleed spontanei trattati | |||
| with bleeds (%) | 6 (18) | 7 (21) | 13 (19) |
| without bleeds (%) | 28 (82) | 27 (79) | 55 (81) |
| 9 | 10 | 19 | |
| Median ASBR (IQR) | 0,0 (NULL,0; 0,0) | 0,0 (NULL,0; 0,0) | 0,0 (NULL,0; 0,0) |
| Mean ASBR (SD) | 2.1 (7.3) | 0,6 (NULL,5) | 1.3 (5.3) |
| Blesi traumatiche trattate | |||
| with bleeds (%) | 15 (44) | 17 (50) | 32 (47) |
| without bleeds (%) | 19 (56) | 17 (50) | 36 (53) |
| 20 | 30 | 50 | |
| Mediana ATBR (IQR) | 0,0 (NULL,0; 2,0) | 0,9 (NULL,0; 2,0) | 0,0 (NULL,0; 2,0) |
| Media ATBR (SD) | 1.7 (4.0) | 1.7 (2.5) | 1.7 (3.3) |
| Blesi articolari trattati | |||
| with bleeds (%) | 7 (21) | 12 (35) | 19 (28) |
| without bleeds (%) | 27 (79) | 22 (65) | 49 (72) |
| 10 | 24 | 34 | |
| AJBR mediana (IQR) | 0,0 (NULL,0; 0,0) | 0,0 (NULL,0; 2,0) | 0,0 (NULL,0; 2,0) |
| Mean AJBR (SD) | 1.5 (6.3) | 1.4 (2.4) | 1.5 (4.7) |
| ABR = tasso di sanguinamento annualizzato; IQR = intervallo interquartile 25 ° percentile al 75 ° percentile; SD = deviazione standard; ASBR = velocità di sanguinamento spontaneo annuale; ATBR = velocità di sanguinamento traumatico annuale; AJBR = velocità di sanguinamento articolare annualizzato *Riflette tutti i sanguinamenti riportati da pazienti, compresi quelli in cui nessun esperoct ® è stato somministrato ** La media elevata ABRS è dovuta a soggetti che si sono ritirati dallo studio i cui tassi di sanguinamento sono stati estrapolati a un anno |
Informazioni sul paziente per Esperoct
Esperoct ®
[fattore antiemofilo (ricombinante) glicopegylated-exei]
Leggi le informazioni sul paziente e le istruzioni per l'uso fornite con Esperoct ® Prima di iniziare a prendere questo medicinale e ogni volta che ricevi una ricarica. Potrebbero esserci nuove informazioni.
Queste informazioni sul paziente non prendono il posto di parlare con il proprio operatore sanitario sulla condizione medica o sul trattamento. Se hai domande su esperoct ® Dopo aver letto queste informazioni chiedi al tuo medico.
Quali sono le informazioni più importanti che devo sapere su esperoct ® ?
Non tentare di fare un'infusione da soli a meno che non ti sia stato insegnato come dal tuo operatore sanitario o dal centro di trattamento dell'emofilia.
È necessario seguire attentamente le istruzioni del tuo operatore sanitario in merito alla dose e al programma per l'infusione di Esperoct ® in modo che il tuo trattamento funzioni meglio per te.
Cos'è Esperoct ® ?
Esperoct ® è una medicina iniettabile usata per sostituire il fattore VIII di coagulazione che manca nei pazienti con emofilia A. emofilia A è un disturbo sanguinante ereditario in tutte le fasce di età che impedisce al sangue di coagulazione normalmente.
Esperoct ® viene utilizzato per trattare e prevenire o ridurre il numero di episodi sanguinanti nelle persone con emofilia A.
può il fececainide causare ipertensione
Il tuo operatore sanitario può darti esperoct ® Quando hai un intervento chirurgico.
Chi non dovrebbe usare Esperoct ® ?
Non dovresti usare Esperoct ® Se tu
- sono allergici al fattore VIII o a uno qualsiasi degli altri ingredienti di Esperoct ®
- Se tu are allergic A hamster proteins
Se non sei sicuro di parlare con il tuo medico prima di utilizzare questo medicinale.
Di 'al tuo operatore sanitario se sei incinta o infermieristica perché Esperoct ® Potrebbe non essere giusto per te.
Cosa dovrei dire al mio operatore sanitario prima di usare Esperoct ® ?
Dovresti dire al tuo medico se tu:
- Avere o avere condizioni mediche.
- Prendi qualsiasi medicinali tra cui medicinali non prescritti e integratori alimentari.
- Sono infermieristici.
- Sono incinta o pianificano di rimanere incinta.
- Ti è stato detto che hai inibitori del fattore VIII.
Come dovrei usare Esperoct ® ?
Trattamento con esperoct ® Dovrebbe essere avviato da un operatore sanitario che ha esperienza nella cura dei pazienti con emofilia A.
Esperoct ® è dato come infusione nella vena.
Puoi infondere esperoct ® in un centro di trattamento dell'emofilia presso l'ufficio del proprio operatore sanitario o a casa. Dovresti essere addestrato su come eseguire le infusioni dal tuo centro di trattamento dell'emofilia o da un operatore sanitario. Molte persone con emofilia imparano a infondere la medicina da soli o con l'aiuto di un membro della famiglia.
Il tuo operatore sanitario ti dirà quanto esperoct ® Utilizzare in base al tuo peso la gravità dell'emofilia A e dove stai sanguinando. La tua dose sarà calcolata in unità internazionali IU.
Chiama subito il tuo operatore sanitario se il tuo sanguinamento non si ferma dopo aver preso Esperoct ® .
Se il tuo sanguinamento non è adeguatamente controllato, potrebbe essere dovuto allo sviluppo degli inibitori del fattore VIII. Questo dovrebbe essere controllato dal tuo medico. Potresti aver bisogno di una dose più elevata di esperoct ® o anche un prodotto diverso per controllare il sanguinamento.
Non aumentare la dose totale di esperoct ® Per controllare il sanguinamento senza consultare il tuo operatore sanitario.
Usa nei bambini
Esperoct ® può essere usato nei bambini. Il tuo operatore sanitario deciderà la dose di Esperoct ® riceverai.
Se dimentichi di usare Esperoct ®
Se dimentichi una dose, infondi la dose persa quando scopri l'errore. Non infondere una doppia dose per compensare una dose dimenticata. Procedi con le successive infusioni previste e continua come consigliato dal proprio medico.
Se smetti di usare Esperoct ®
Non smettere di usare Esperoct ® senza consultare il tuo medico.
Se hai ulteriori domande sull'uso di questo prodotto, chiedi al tuo operatore sanitario.
E se prendo troppo esperoct ® ?
Prendi sempre Esperoct ® Esattamente come ti ha detto il tuo operatore sanitario. Dovresti verificare con il tuo medico se non sei sicuro. Se infondi più esperoct ® di quanto raccomandata il tuo operatore sanitario il più presto possibile.
Quali sono i possibili effetti collaterali di Esperoct ® ?
Gli effetti collaterali comuni includono:
- eruzione cutanea or prurito
- Gonfiore antier e arrossamento nella posizione dell'infusione
Potresti avere una reazione allergica ai prodotti del fattore VIII di coagulazione. Chiama subito il tuo operatore sanitario o ricevi immediatamente un trattamento di emergenza se ricevi segni di reazione allergica come: orticaria tenuta toracica sibilante vertigini Difficoltà a respirare E/or swelling of the face.
Il tuo corpo può anche creare anticorpi chiamati inibitori contro Esperoct ® che può fermare l'esperoct ® dal lavoro correttamente. Il tuo operatore sanitario potrebbe essere necessario testare il sangue per gli inibitori di volta in volta.
Questi non sono tutti i possibili effetti collaterali di Esperoct ® . Chiedi al tuo operatore sanitario ulteriori informazioni. Sei incoraggiato a segnalare gli effetti collaterali alla FDA al numero 1-800-FDA-1088.
Dì al tuo operatore sanitario di qualsiasi effetto collaterale che ti disturba o che non scompare.
Cosa sono gli esperoct ® punti di forza del dosaggio?
Esperoct ® È disponibile in cinque diversi punti di forza del dosaggio. Il numero effettivo di unità internazionali (IU) del fattore VIII nella fiala sarà impresso sull'etichetta e sulla scatola. I cinque diversi punti di forza sono i seguenti:
| Indicatore di colore del cappuccio | Forza nominale |
| Rosso | 500 UI per vial |
| Verde | 1000 UI per vial |
| Grigio | 1500 UI per vial |
| Giallo | 2000 UI per vial |
| Nero | 3000 IU per vial |
Controlla sempre l'effettiva resistenza al dosaggio stampato sull'etichetta per assicurarti di utilizzare la forza prescritta dal tuo medico.
Come dovrei archiviare esperoct ® ?
Prima della ricostituzione (Mescolando la polvere secca nella fiala con il diluente):
Proteggere dalla luce. Non congelare Esperoct ® .
Esperoct ® può essere immagazzinato in refrigerazione da 36 ° F a 46 ° F (da 2 ° C a 8 ° C) per un massimo di 30 mesi fino alla data di scadenza dichiarata sull'etichetta. Durante la durata di 30 mesi Esperoct ® può essere mantenuto a temperatura ambiente (non superiore a 86 ° F/30 ° C) per un massimo di 12 mesi o fino a 104 ° F (40 ° C) per non più di 3 mesi.
Se scegli di archiviare Esperoct ® A temperatura ambiente:
- Registra la data in cui il prodotto è stato rimosso dal frigorifero.
- Non restituire il prodotto al frigorifero.
- Non utilizzare dopo 12 mesi se immagazzinato fino a 86 ° F (30 ° C) o dopo 3 mesi se conservato fino a 104 ° F (40 ° C) o la data di scadenza elencata sulla fiala a seconda di quale sia precedente.
Non utilizzare questo medicinale dopo la data di scadenza che si trova sul cartone esterno e sulla fiala. La data di scadenza si riferisce all'ultimo giorno di quel mese.
Dopo la ricostituzione:
Il ricostituito (il prodotto finale una volta che la polvere viene miscelata con il diluente) esperoct ® dovrebbe apparire chiaro e incolore senza particelle visibili.
L'esperoct ricostituito ® dovrebbe essere usato immediatamente.
Se non è possibile utilizzare ESPEROCT ricostituito ® Immediatamente deve essere utilizzato entro 4 ore quando conservato a 30 ° C) o inferiore a 86ºF (entro 24 ore quando conservato in frigorifero da 36 ° F a 46 ° F (da 2 ° C a 8 ° C). Conservare il prodotto ricostituito nella fiala.
Tieni questa medicina fuori dalla vista e fuori dalla portata dei bambini.
Cos'altro dovrei sapere su esperoct ® E hemophilia A?
Le medicine sono talvolta prescritte per scopi diversi da quelli elencati qui. Non usare esperoct ® per una condizione per la quale non è prescritta. Non condividere esperoct ® con altre persone anche se hanno gli stessi sintomi che hai.
Istruzioni per l'uso
Esperoct ®
[fattore antiemofilo (ricombinante) glicopegylated-exei] MixPro ®
Leggi attentamente queste istruzioni prima di usare Esperoct ® .
Esperoct ® viene fornito come polvere. Prima dell'infusione (somministrazione) deve essere miscelato (ricostituito) con il diluente liquido fornito nella siringa. Il diluente liquido è una soluzione di cloruro di sodio. L'esperoct misto ® Deve essere infuso nella tua vena (infusione endovenosa). L'apparecchiatura in questo pacchetto è progettata per mescolare e infondere Esperoct ® .
Avrai anche bisogno di un set di infusioni (ago per farfalla con tubo) tamponi e bende di garza sterili.
Non utilizzare l'attrezzatura senza una formazione adeguata dal medico o dall'infermiera.
Lavare sempre le mani e assicurarsi che l'area intorno a te sia pulita.
Quando prepari e infondi i farmaci direttamente nelle vene, è importante Usa una tecnica pulita e senza germi (asettici). Una tecnica impropria può introdurre germi che possono infettare il sangue.
Non aprire l'attrezzatura fino a quando non sei pronto per usarla.
Non utilizzare l'attrezzatura se è stata lasciata cadere o se è danneggiata. Usa invece un nuovo pacchetto.
Non utilizzare l'attrezzatura se è scaduta. Usa invece un nuovo pacchetto. The expiration date is printed on the outer carAn E on the vial the vial adapter E the pre-filled syringe.
Non utilizzare l'attrezzatura se sospetti che sia contaminata. Usa invece un nuovo pacchetto.
Non smaltire nessuno degli articoli fino a quando non hai infuso la soluzione mista.
L'attrezzatura è solo per uso singolo.
Contenitore monodose. Scartare la parte inutilizzata.
Contenuto
Il pacchetto contiene:
Pacchetto contents
| ® powder - Illustration' src='//pharmacie-hoffer.eu/img/coagulation-factors/92/esperoct-12.webp' > |
- Fial con Esperoct ® polvere
- Adattatore di fiala
- Siringa pre-riempita con diluente
- Asta dello stanger (posizionato sotto la siringa)
Panoramica
Puoi prendere 20 mg di Ambien
Non toccare la punta della siringa. Se tocchi la punta della siringa, i germi dalle dita possono essere trasferiti.
Attenzione: La siringa di diluente pre-riempita è realizzata in vetro con un diametro della punta interno di 0,037 pollici ed è compatibile con un connettore Luer-Lock standard.
Alcuni connettori senza bisogni per cateteri endovenosi sono incompatibili con le siringhe diluenti di vetro (ad esempio alcuni connettori con un picco interno come la clave ® /Microclave ® Invision-plus ® Invision- Plus CS ® Invision-plus ® Junior ® Bionector ® ).
Per somministrare Esperoct ® Attraverso i connettori incompatibili senza nemico prelevare il prodotto ricostituito in una siringa di plastica Luer-Lock sterile standard da 10 ml.
Se hai riscontrato problemi con l'attacco della siringa pre-riempita di cloruro di sodio a qualsiasi dispositivo compatibile Luer-blocco, contatta Novo Nordisk al numero (800) 727-6500.
- Preparare la fiala e la siringa
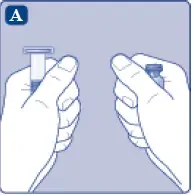
- Elimina il numero di Esperoct ® pacchetti di cui hai bisogno.
- Controlla la data di scadenza.
- Controlla la forza e il colore del nome del pacchetto per assicurarsi che contenga il prodotto corretto.
- Lavati le mani E dry them properly using a clean Awel or air dry.
- Prendi la fiala dell'adattatore di fiala e la siringa pre-riempita dal cartone. Lascia l'intatto dell'asta dello stantuffo nel cartone.
- Portare la siringa pre-riempita a temperatura ambiente. Puoi farlo tenendoli tra le mani fino a quando non si sentono caldi come le mani.
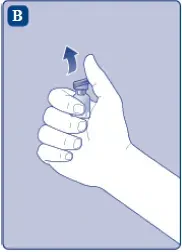
- Rimuovere il tappo di plastica dalla fiala. Se il tappo di plastica è allentato o mancante, non usa la fiala.
- Pulisci il tappo di gomma con un tampone di alcol sterile E allow it A air dry for a few seconds before use A ensure that it is as germ free as possible.
- Non toccare il tappo di gomma con le dita in quanto questo può trasferire germi.
- Attacca l'adattatore della fiala
Non togliere l'adattatore di fiala dal cappuccio protettivo con le dita. Se tocchi il picco sul fatto che i germi dell'adattatore della fiala dalle dita possono essere trasferiti.
Se la carta protettiva non è completamente sigillata o se è rotta, non utilizzare l'adattatore di fiala.

Una volta collegato non rimuovere l'adattatore della fiala dalla fiala.
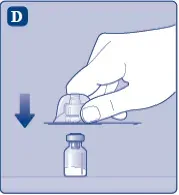
Non sollevare l'adattatore della fiala dalla fiala Quando si rimuove il cappuccio protettivo.

- Rimuovi la carta protettiva Dall'adattatore della fiala.
- Posizionare la fiala su una superficie piana e solida.
- Girare il cappuccio protettivo E snap the vial adapter onA the Fial.
- Rimuovere con cura il cappuccio protettivo Dall'adattatore della fiala.
- Collegare l'asta dello stantuffo e la siringa



- Afferrare l'asta dello stanger dall'estremità superiore e toglila dal cartone. Non toccare i lati o il filo dell'asta dello stanger. Se tocchi i lati o i germi del filo dalle dita possono essere trasferiti.
- Immediatamente Collegare l'asta dello stantuffo alla siringa trasformandola in senso orario nello stantuffo di gomma all'interno della siringa pre-riempita fino a quando non viene avvertita la resistenza.
- Rimuovere il tappo della siringa Dalla siringa pre-riempita piegandola fino a quando la perforazione si rompe. Non toccare la punta della siringa sotto il cappuccio della siringa. Se tocchi la punta della siringa, i germi dalle dita possono essere trasferiti. Se il tappo della siringa è allentato o mancante, non utilizzare la siringa pre-riempita.
- Avvitare saldamente la siringa pre-riempita Sull'adattatore della fiala fino a quando non viene avvertita la resistenza.
- Mescola la polvere con il diluente

Non scuotere la fiala in quanto ciò causerà schiuma.
Deve essere chiaro e incolore.
Se noti particelle visibili o scolorimento non lo usi.
Usa invece un nuovo pacchetto.

Esperoct ® si consiglia di essere utilizzato immediatamente dopo che è stato miscelato.
Se non è possibile utilizzare l'esperoct misto ® soluzione immediatamente Deve essere usato entro 4 ore quando conservato a ≤86 ° F (30 ° C) o entro 24 ore quando conservato in frigorifero da 36 ° F a 46 ° F (da 2 ° C a 8 ° C). Conservare il prodotto ricostituito nella fiala.
Non congelare l'esperoct misto ® soluzione o memorizzalo in siringhe.
Mantieni l'esperoct ricostituito ® soluzione fuori dalla luce diretta.
Se la tua dose richiede più di un passaggio di ripetizione della fiala A A J con ulteriori fiale di fiala e siringhe pre-riempite fino a quando non hai raggiunto la dose richiesta.
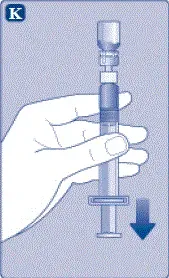
- Tenere la siringa pre-riempita leggermente inclusa con la fiala che punta verso il basso.
- Spingere l'asta dello stantuffo A inject all the diluent inA the Fial.
- Mantieni l'asta dello stantuffo premuto e turbina la fiala delicatamente fino a quando tutta la polvere non viene sciolta.
- Controlla la soluzione mista.
- Mantieni l'asta dello stantuffo spinto completamente dentro.
- Gira la siringa con la fiala capovolta.
- Smetti di spingere l'asta dello stantuffo e lasciarlo tornare indietro da sola mentre la soluzione mista riempie la siringa.
- Tirare l'asta dello stantuffo leggermente verso il basso A draw the mixed solution inA the syringe.
- Nel caso in cui tu abbia solo bisogno di parte dell'intera fiala, utilizzare la scala sulla siringa per vedere quanta soluzione mista prelevate come indicato dal medico o dall'infermiera.
- Mentre tiene la fiala a testa in giù Tocca delicatamente la siringa A let any air bubbles rise A the Ap.
- Spingere l'asta dello stantuffo Lentamente fino a quando tutte le bolle d'aria non sono sparite.
- Svitare l'adattatore della fiala con la fiala.
- Infondere la soluzione mista
Esperoct ® ora è pronto a infondere nella tua vena.
Infusione della soluzione tramite un dispositivo di accesso venoso centrale (CVAD) come un catetere venoso centrale o una porta sottocutanea:
L'etichetta peel-off trovata su esperoct ® Fial può essere utilizzato per registrare il numero del lotto.
Disposizione
Non buttarlo fuori con la normale spazzatura domestica.
Non smontare l'adattatore di fiala e fiala prima dello smaltimento.
Non riutilizzare l'attrezzatura.
Informazioni importanti
Contatta il tuo medico o il centro di trattamento dell'emofilia locale se si riscontrano problemi.
Per le informazioni complete sulla prescrizione si prega di leggere l'altro inserto incluso in questo pacchetto.
- Non mescolare l'esperoct ® con altre infusioni o farmaci per via endovenosa.
- Infondere la soluzione mista slowly over 1 a 3 minutes as instructed by your docAr or nurse.
- Usa una tecnica pulita e senza germi (asettici). Seguire le istruzioni per il corretto utilizzo per il tuo connettore e il dispositivo di accesso venoso centrale in consultazione con il medico o l'infermiera.
- Infondere in un CVAD può richiedere l'uso di una siringa di plastica da 10 ml sterili per il ritiro della soluzione mista e dell'infusione.
- Se necessario, utilizzare l'iniezione di cloruro di sodio 0,9% USP per eliminare la linea CVAD prima o dopo ESPEROCT ® infusione.
- Dopo l'infusione smaltita in modo sicuro di tutti gli esperoct inutilizzati ® Soluzione La siringa con l'infusione imposta la fiala con l'adattatore della fiala e altri materiali di scarto in un contenitore appropriato per buttare via i rifiuti medici.











