Le Informazioni Presenti Sul Sito Non Costituiscono Consulenza Medica. Non Vendiamo Nulla. L'Accuratezza Della Traduzione Non È Garantita. Disclaimer
Inibitori della decarbossilasiStalevo
Riepilogo della droga
Cos'è Stalevo?
Stalevo (carbidopa levodopa ed entacapone) è una combinazione di diversi farmaci usati per trattare i sintomi del parkinson come i tremori della rigidità muscolare spasmi e uno scarso controllo muscolare. Levodopa viene convertita in una sostanza chimica chiamata dopamina nel cervello. Sintomi di La malattia di Parkinson può essere causato da bassi livelli di dopamina nel cervello. Carbidopa aiuta a prevenire la rottura di Levodopa prima che possa raggiungere il cervello e avere effetto. Se usato con carbidopa e levodopa entacapone aumenta i livelli di levodopa nel corpo.
Quali sono gli effetti collaterali di Stalevo?
Stalevo
- orticaria
- Difficoltà a respirare
- gonfiore della lingua o della gola
- spasmo muscolare nuovo o peggioramento
- Aumentando notevolmente le palpebre per gli occhi o le contrazioni
- svenimento
- diarrea
- Cambiamenti della visione
- visione sfocata
- Dolore agli occhi
- grave dolore addominale
- sgabelli neri o invariati
- vomito che assomiglia a fondi di caffè
- dolori muscolari tenerezza o debolezza
- Modifica della quantità di urina
- Cambiamenti dell'umore
- confusione
- allucinazioni
- Pensieri di suicidio
- persistente mal di gola
- Sanguinamento facile o contuso
- stanchezza insolita
- formicolio delle mani o dei piedi
- impulsi forti insoliti (aumento del gioco d'azzardo impulsi)
- dolore al petto
- febbre
- insolita rigidità muscolare
- grave confusione
- sudorazione
- battito cardiaco veloce o irregolare
- respirazione rapida e
- Scrigette gravi
Ottieni subito assistenza medica se hai uno qualsiasi dei sintomi sopra elencati.
Gli effetti collaterali comuni di Stalevo includono:
- diarrea
- nausea
- vomito
- mal di testa
- vertigini
- sonnolenza
- visione sfocata
- Dolori di stomaco o sconvolgimento
- perdita di appetito
- stipsi
- bocca secca
- Cambiamenti nel tuo senso del gusto
- eruzione cutanea o prurito
- Cambiamenti insoliti della pelle
- Crampi muscolari
- mal di schiena
- agitazione
- ansia
- difficoltà a dormire (insonnia) o
- strano sogni .
Di 'al medico se hai gravi effetti collaterali di Stalevo, incluso:
- involontario movimenti (in particolare contrazioni della palpebra)
- svenimento or falling
- Difficoltà a deglutire
- Dolore allo stomaco/addominale
- persistente diarrea
- Cambiamenti della visione (including visione sfocata)
- sgabelli neri/invariati
- Dolore muscolare
- cambiamenti nella quantità di urina
- Cambiamenti mentali/dell'umore (come allucinazioni di confusione pensieri di suicidio)
- segni di infezione (ad esempio mal di gola persistente) o
- impulsi insoliti forti (come un aumento del gioco d'azzardo aumentato impulsi sessuali).
Cerca cure mediche o chiama il 911 contemporaneamente se hai i seguenti gravi effetti collaterali:
- Sintomi di occhiali gravi come la perdita di visione improvvisa del tunnel della visione sfocata Dolore alla visione o gonfiore o vedere aloni attorno alle luci;
- Sintomi cardiaci gravi come battiti cardiaci irregolari o martellanti veloci; svolazzando nel petto; fiato corto; e vertigini improvvise Accendino o svenire;
- Grave mal di testa confusione Il braccio del linguaggio bloccato o la debolezza delle gambe problemi perdite perdita di coordinamento sentendoti instabili muscoli molto rigidi ad alta febbre abbondante sudorazione o tremori.
Questo documento non contiene tutti i possibili effetti collaterali e altri possono verificarsi. Verificare con il tuo medico ulteriori informazioni sugli effetti collaterali.
Dosaggio per stalevo
Il dosaggio giornaliero ottimale di Stalevo deve essere determinato per ciascun paziente. La terapia deve essere individualizzata e adattata in base alla risposta terapeutica desiderata.
Quali sostanze o integratori di farmaci interagiscono con Stalevo?
Stalevo può interagire con l'apomorfina colestyramina dobutamina epinefrina isoniazid isoproterenolo metildopa metoclopramide di papaverina fenitoina probenecid antibiotici farmaci antidepressivi antidepressivi medicinali per trattare i disturbi psichiatrici freddi o allergia Medicina Narcotici Pugni per dormire Muscolo rilassante Medicina per convulsioni o farmaci anti-ansia. Dì al tuo medico tutti i farmaci che stai assumendo.
Stalevo durante la gravidanza e l'allattamento
Stalevo dovrebbe essere usato solo quando prescritto durante la gravidanza. Levodopa passa nel latte materno. Non è noto se il carbidopa o l'entacapone passino nel latte materno. Consulta il medico prima dell'allattamento al seno.
Ulteriori informazioni
Il nostro centro farmacologico stalevo (carbidopa levodopa ed entacapone) fornisce una visione completa delle informazioni disponibili sui farmaci sui potenziali effetti collaterali durante l'assunzione di questo farmaco.Informazioni sui farmaci FDA
- Descrizione del farmaco
- Indicazioni
- Effetti collaterali
- Interazioni farmacologiche
- Avvertimenti
- Overdose
- Farmacologia clinica
- Guida ai farmaci
Descrizione per Stalevo
Stalevo è una combinazione di carbidopa levodopa e entacapone per il trattamento della malattia di Parkinson.
Carbidopa Un inibitore della decarbossilazione aromatica di aminoacidi è un composto cristallino bianco leggermente solubile in acqua con un peso molecolare di 244,3. È designato chimicamente come (-)-l- (α-idrazino- (α-metil-β- (34-diidrossibenzene) acido propanoico monoidrato. La sua formula empirica è C 10 H 14 N 2 O 4 ·H 2 O e la sua formula strutturale è:
 |
Il contenuto di tablet è espresso in termini di carbidopa anidra che ha un peso molecolare di 226.3.
Levodopa Un aminoacido aromatico è un composto cristallino bianco leggermente solubile in acqua con un peso molecolare di 197.2. È designato chimicamente come (-)-L-α-ammino-β- (34-diidrossibenzene) acido propanoico. La sua formula empirica è C 9 H 11 NO 4 E la sua formula strutturale è:
 |
Entacapone Un inibitore COMT è un composto strutturato da nitro-catecolo con un peso molecolare di 305,3. Il nome chimico di entacapone è (e) -2-cyano-3- (34-diidrossi-5-nitrofenil) -nn-dieetil-2-propenamide. La sua formula empirica è C 14 H 15 N 3 O 5 E la sua formula strutturale è:
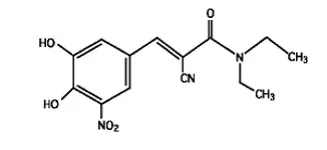 |
Stalevo è fornito come compresse in 6 punti di forza:
Stalevo 50: 12,5 mg di carbidopa 50 mg di levodopa e 200 mg di entecapone
Stalevo 75: 18,75 mg di Carbidopa 75 mg di Levodopa e 200 mg di entecapone
Stalevo 100: 25 mg di carbidopa 100 mg di Levodopa e 200 mg di entecapone
Stalevo125: 31,25 mg di carbidopa 125 mg di levodopa e 200 mg di entecapone
Stalevo 150: 37,5 mg di carbidopa 150 mg di levodopa e 200 mg di entecapone
Stalevo 200: 50 mg di carbidopa 200 mg di Levodopa e 200 mg di entecapone
Ingredienti inattivi: Amido di mais Croscarmellosio sodio glicerolo 85% ipromellosio magnesio stearato polisorbato 80 Povidone saccarosio ossido di ferro rosso e biossido di titanio. Stalevo 50 Stalevo 100 e Stalevo 150 contengono anche ossido di ferro giallo.
Usi per Stalevo
Stalevo è indicato per il trattamento della malattia di Parkinson.
Stalevo può essere usato:
- Sostituire (con punti di forza equivalenti di ciascuno dei tre componenti) Carbidopa/Levodopa e Entecapone precedentemente somministrati come singoli prodotti.
- Per sostituire la terapia carbidopa/levodopa (senza entacapone) quando i pazienti sperimentano segni e sintomi di uscita di endof-dose e quando hanno assunto una dose giornaliera totale di levodopa di 600 mg o meno e non hanno sperimentato diskinesie.
Dosaggio per stalevo
Stalevo dovrebbe essere usato come sostituto dei pazienti già stabilizzati su dosi equivalenti di carbidopa/levodopa e entecapone. Tuttavia, alcuni pazienti che sono stati stabilizzati su una determinata dose di carbidopa/levodopa possono essere trattati con stalevo se è stata presa una decisione per aggiungere entecapone (vedi sotto ). La terapia deve essere individualizzata e adattata in base alla risposta terapeutica desiderata.
Informazioni sul dosaggio
Il dosaggio giornaliero ottimale di Stalevo deve essere determinato mediante un'attenta titolazione in ciascun paziente.
L'esperienza clinica con dosi giornaliere superiori a 1600 mg di entecapone è limitata. La dose giornaliera massima raccomandata di Stalevo dipende dalla resistenza utilizzata. Il numero massimo di compresse da utilizzare in un periodo di 24 ore è inferiore con la massima resistenza (Stalevo 200) rispetto a resistenze più basse (vedere la Tabella 1). Gli studi dimostrano che la DOPA decarbossilasi periferica è satura da Carbidopa a circa 70 mg al giorno a 100 mg al giorno. I pazienti che ricevono meno di questa quantità di carbidopa hanno maggiori probabilità di sperimentare nausea e vomito.
Tabella 1: dose massima consigliata di stalevo in un periodo di 24 ore
| Forza di dosaggio di stalevo | Numero massimo di compresse in un periodo di 24 ore |
| Stalevo 50 Stalevo 75 Stalevo 100 Stalevo 125 Stalevo 150 | 8 |
| Stalevo 200 | 6 |
Convertire i pazienti da carbidopa levodopa e entacapone in stalevo
I pazienti attualmente trattati con Entacapone 200 mg con ogni dose di compressa carbidopa/levodopa a rilascio non esteso possono passare alla corrispondente resistenza di stalevo contenente le stesse quantità di levodopa e carbidopa. Ad esempio, i pazienti che ricevono una compressa di carbidopa/levodopa 25 mg/100 mg e una compressa di entecapone 200 mg ad ogni somministrazione possono passare a una singola compressa stalevo 100 (contenente 25 mg di carbidopa 100 mg di levodopa e 200 mg di entecapone).
Convertire i pazienti dai prodotti carbidopa e levodopa in stalevo
Non esiste esperienza nel trasferimento di pazienti attualmente trattati con formulazioni di rilascio esteso di prodotti carbidopa/levodopa o carbidopa/levodopa che non sono combinati in un rapporto 1: 4 di carbidopa e levodopa.
I pazienti con una storia di discinesie moderate o gravi o che assumono più di 600 mg della componente Levodopa al giorno sono probabili richiedere una riduzione della loro dose giornaliera di levodopa quando viene aggiunto entacapone. Poiché la regolazione della dose del singolo componente carbidopa o levodopa non è possibile con i prodotti a dose fissa inizialmente titolano i pazienti con una dose tollerata e che soddisfa la loro necessità terapeutica individuale utilizzando un tablet di carbidopa/levodopa separato (rapporto 1: 4) più un tablet di entecapone. Una volta che la dose individuale del paziente di carbidopa/levodopa più la dose di entacapone è stata stabilita utilizzando due compresse separate; Passa il paziente in una singola compressa corrispondente di Stalevo.
Quando è necessaria una minore levodopa, ridurre il dosaggio giornaliero totale di carbidopa/levodopa diminuendo la resistenza di stalevo ad ogni somministrazione o diminuendo la frequenza di somministrazione estendendo il tempo tra le dosi.
Uso concomitante con altri farmaci per la malattia di Anti-Parkinson
Agenti anticolinergici dopamina Gli agonisti monoamine ossidasi (MAO) - B inibitori dell'amantadina e altri farmaci standard per il morbo di Parkinson possono essere usati in concomitanza mentre lo stalevo viene somministrato; Tuttavia, possono essere richiesti aggiustamenti del dosaggio del farmaco concomitante o dello stalevo.
Diminuire o interruzione del dosaggio
Evita l'interruzione del dosaggio di stalevo perché l'iperpyrexia è stata segnalata in pazienti che improvvisamente interrompono o riducono il loro uso di levodopa [vedi Avvertimenti e precauzioni ].
Importanti istruzioni di amministrazione
Non dividere le compresse di schiacciamento o masticare stalevo. Somministrare solo una compressa ad ogni intervallo di dosaggio. Tutti i punti di forza di Stalevo contengono 200 mg di entecapone. La combinazione di più compresse o porzioni di compresse per ottenere una dose di levodopa più elevata può portare a un sovradosaggio di entecapone.
Somministrare stalevo con o senza cibo. Tuttavia, un pasto ad alto contenuto di grassi può ritardare l'assorbimento di Levodopa di circa 2 ore [vedi Farmacologia clinica ].
Come fornito
Forme di dosaggio e punti di forza
Ogni compressa Stalevo fornita in 6 punti di forza a dose singola contiene carbidopa e levodopa in un rapporto 1: 4 e una dose di 200 mg di entecapone. Stalevo (carbidopa levodopa ed entacapone) è fornito come compresse rivestite di film per la somministrazione orale nei seguenti 6 punti di forza:
Stalevo 50 compresse rivestite di film contenenti 12,5 mg di carbidopa 50 mg di levodopa e 200 mg di entecapone. Le compresse rotonde a forma di bi-convex sono LCE 50 brunastro o grigiastro e in rilievo su un lato.
Stalevo 75 compresse rivestite di film contenenti 18,75 mg di carbidopa 75 mg di levodopa e 200 mg di entecapone. I tablet a forma di ovalo sono un non punteggiati rossi marrone chiaro e in rilievo con il codice LCE 75 su un lato.
Stalevo 100 compresse rivestite di film contenenti 25 mg di carbidopa 100 mg di levodopa e 200 mg di entecapone. Le tavolette a forma di ovale sono LCE non punteggiate brunish o grigiastri e in rilievo LCE su un lato.
Stalevo 125 compresse rivestite con film contenenti 31,25 mg di carbidopa 125 mg di levodopa e 200 mg di entecapone. I tablet a forma di ovale sono un senza punteggio rosso marrone chiaro e in rilievo con il codice LCE 125 su un lato.
Stalevo 150 compresse rivestite di film contenenti 37,5 mg di carbidopa 150 mg di levodopa e 200 mg di entecapone. Le compresse a forma di ellisse allungate sono LCE 150 brunastro o grigiastro e in rilievo su un lato.
Stalevo 200 compresse rivestite di film contenenti 50 mg di carbidopa 200 mg di levodopa e 200 mg di entecapone. Le compresse a forma di ovale sono LCE non punteggiate rosse brunastre scure e in rilievo 200 su un lato.
Archiviazione e maneggevolezza
Stalevo (carbidopa levodopa e entacapone) è fornito come compresse rivestite di film per la somministrazione orale nei seguenti sei punti di forza:
Stalevo 50 film-coated tablets contenente 12,5 mg di carbidopa 50 mg di levodopa e 200 mg di entecapone.
Le compresse rotonde a forma di bi-convex sono LCE 50 brunastro o grigiastro e in rilievo su un lato.
Bottiglia HDPE di 100 compresse Ndc 52427-805-01
Stalevo 75 film-coated tablets contenente 18,75 mg di carbidopa 75 mg di levodopa e 200 mg di entecapone.
I tablet a forma di ovale sono un senza punteggio rosso marrone chiaro e in rilievo con il codice LCE 75 su un lato.
Bottiglia HDPE di 100 compresse Ndc 52427-809-01
Stalevo 100 film-coated tablets contenente 25 mg di carbidopa 100 mg di levodopa e 200 mg di entecapone.
Le compresse a forma di ovale sono LCE senza punteggio brunastro o grigiastro e in rilievo su un lato.
Bottiglia HDPE di 100 compresse Ndc 52427-816-01
Stalevo 125 film-coated tablets contenente 31,25 mg di carbidopa 125 mg di Levodopa e 200 mg di entecapone.
I tablet a forma di ovale sono un senza punteggio rosso marrone chiaro e in rilievo con il codice LCE 125 su un lato.
Bottiglia HDPE di 100 compresse Ndc 52427-827-01
Stalevo 150 film-coated tablets contenente 37,5 mg di carbidopa 150 mg di levodopa e 200 mg di entecapone.
Le compresse a forma di ellisse allungate sono LCE 150 brunastro o grigiastro e in rilievo su un lato.
Bottiglia HDPE di 100 compresse Ndc 52427-834-01
Stalevo 200 film-coated tablets contenente 50 mg di carbidopa 200 mg di levodopa e 200 mg di entecapone.
Le compresse a forma di ovale sono LCE non punteggiate rosse brunastre scure e in rilievo 200 su un lato.
Bottiglia HDPE di 100 compresse Ndc 52427-842-01
Conservare a 25 ° C (77 ° F); Escursioni consentite a 15 ° C a 30 ° C (da 59 ° F a 86 ° F).
[Vedere A temperatura ambiente controllata da USP .
Dispensare in contenitore stretto (USP).
Prodotto da: Orion Corporation Orion Pharma OrionIntie 1 FI-02200 ESPOO FINLAND. Distribuito da: Almatica Pharma LLC Morristown NJ 07960 USA. Revisionato: maggio 2020
Effetti collaterali for Stalevo
Le seguenti reazioni avverse sono discusse in modo più dettagliato nelle sezioni di avvisi e precauzioni dell'etichettatura:
- Addormentarsi durante le attività di vita quotidiana e sonnolenza [vedi Avvertimenti e precauzioni ]
- Ipotensione /Ipotensione ortostatica e sincope [vedi Avvertimenti e precauzioni ]
- Dyskinesia [vedi Avvertimenti e precauzioni ]
- Depressione e suicidalità [vedi Avvertimenti e precauzioni ]
- Allucinazioni/comportamento psicotico [vedi Avvertimenti e precauzioni ]
- Controllo degli impulsi e/o comportamenti compulsivi [vedi Avvertimenti e precauzioni ]
- Iperpyrexia e confusione emergente di ritiro [vedi Avvertimenti e precauzioni ]
- Diarrea e colite [vedi Avvertimenti e precauzioni ]
- Rabdomiolisi [vedi Avvertimenti e precauzioni ]
- Patora dell'ulcera peptica [vedi Avvertimenti e precauzioni ]
Esperienza di studi clinici
Poiché gli studi clinici sono condotti in condizioni ampiamente variabili, l'incidenza di reazioni avverse (numero di pazienti unici che sperimentano una reazione avversa associata al trattamento/numero totale di pazienti trattati) osservati negli studi clinici di un farmaco non può essere paragonato direttamente all'incidenza delle reazioni avverse negli studi clinici di un altro farmaco e non può riflettere l'incidenza delle reazioni avverse nella pratica clinica.
Entacapone
Le reazioni avverse più comunemente osservate (incidenza almeno il 3% maggiore dell'incidenza del placebo) nel doppio cieco blind-levodopa-placebo-controllati da prove di etacapone (n = 1003 pazienti) associati all'uso di DiarHinesia carbidopalesa e non visti da una frequenza equivalente tra i pazienti con traduzione da placebo: Diarhasia-Entacapone Dolore addominale vomito secco secco e scolorimento delle urine.
L'incidenza della differenza di trattamento per la discontinuazione dello studio prematuro per entecapone con l'inibitore di levodopa e DOPA decarbossilasi negli studi in doppio cieco controllato con placebo è stato del 5%. L'incidenza della differenza di trattamento per le cause più frequenti della sospensione dello studio è stata del 2% per la diarrea e dell'1% per altre reazioni avverse specifiche, tra cui ragioni psichiatriche per motivi di discinesia/ iperkinesia nausea o dolore addominale.
Incidenza di reazione avversa negli studi clinici controllati sull'ostacapone
La tabella 2 elenca il trattamento reazioni avverse emergenti che si sono verificate in almeno l'1% dei pazienti trattati con carbidopa/levodopa e 200 mg di etacapone che hanno partecipato agli studi controllati in doppio cieco con placebo e che erano numericamente più comuni in questo gruppo rispetto al gruppo Carbidopa/Levodopa Plusbo. In questi studi è stato aggiunto e entacapone o placebo a Carbidopa/Levodopa (o Benserazide/Levodopa).
Tabella 2: Riepilogo dei pazienti con reazioni avverse dopo l'inizio della somministrazione di farmaci di prova almeno l'1% nel gruppo di entacapone e maggiore del placebo
| Reazione avversa della classe di organi di sistema | Carbidopa/levodopa plus entacapone (n = 603) % dei pazienti | Carbidopa/Levodopa Plus Placebo (n = 400) % dei pazienti |
| Disturbi della pelle e delle appendici | ||
| La sudorazione aumentava | 2 | 1 |
| Disturbi del sistema muscoloscheletrico | ||
| Mal di schiena | 5 | 3 |
| Disturbi del sistema nervoso centrale e periferico | ||
| Discinesia | 25 | 15 |
| Iperkinesia | 10 | 5 |
| Ipocinesia | 9 | 8 |
| Vertigini | 8 | 6 |
| Sensi speciali altri disturbi | ||
| Gusto perversione | 1 | 0 |
| Disturbi psichiatrici | ||
| Ansia | 2 | 1 |
| Sonnolenza | 2 | 0 |
| Agitazione | 1 | 0 |
| Disturbi del sistema gastrointestinale | ||
| Nausea | 14 | 8 |
| Diarrea | 10 | 4 |
| Dolore addominale | 8 | 4 |
| Stipsi | 6 | 4 |
| Vomito | 4 | 1 |
| Bocca asciutta | 3 | 0 |
| Dispepsia | 2 | 1 |
| Flatulenza | 2 | 0 |
| Gastrite | 1 | 0 |
| Disturbi gastrointestinali nn | 1 | 0 |
| Disturbi del sistema respiratorio | ||
| Dispnea | 3 | 1 |
| Sanguinamento piastrinico e coagulazione Disturbi | ||
| Porpora | 2 | 1 |
| Disturbi del sistema urinario | ||
| Scolorimento delle urine | 10 | 0 |
| Corpo come disturbi generali interi | ||
| Fatica | 6 | 4 |
| Astenia | 2 | 1 |
| Disturbi del meccanismo di resistenza | ||
| Batterio di infezione | 1 | 0 |
Esperienza post -marketing
Le seguenti segnalazioni spontanee di eventi avversi temporalmente associati a entecapone o Stalevo sono stati identificati dall'introduzione del mercato e non sono elencati nella Tabella 2. Poiché queste reazioni sono riportate volontariamente da una popolazione di dimensioni sconosciute, non è sempre possibile stimare in modo affidabile la loro frequenza o stabilire una relazione causale con l'Etacapone o l'esposizione di Statalevo.
È stata segnalata l'epatite con caratteristiche principalmente colestatiche.
Effetti del genere ed età sulle reazioni avverse
Non sono state rilevate differenze nel tasso di reazioni avverse attribuibili al solo entacapone per età o sesso.
Interazioni farmacologiche for Stalevo
Inibitori MAO
I pazienti che ricevono inibitori del MAO non selettivi e carbidopa levodopa e entacapone possono essere a rischio di un tono adrenergico. Pertanto l'uso di stalevo è controindicato nei pazienti che ricevono inibitori MAO non selettivi [vedi Controindicazioni ].
Farmaci metabolizzati da catecol-o-metiltransferasi (COMT)
I farmaci noti per essere metabolizzati da COMT come l'isoproterenolo epinefrina norapiefrina dopamina dobutamina alfa-metildopa apomorfina isoetherine e butolterolo devono essere somministrati con cautela che ricevono ecologie in caso di pressione di ecorda che si possono essere in evento di ecordiatura e le loro variazioni del cuore devono essere somministrate in cautela e l'eccesso di ecologie e il loro aumento del cuore. [Vedere Avvertimenti e precauzioni ].
Agenti antiipertensivi
Sintomatico Ipotensione posturale Si è verificato quando Carbidopa/Levodopa è stato aggiunto al trattamento di pazienti che ricevono farmaci antiipertensivi. Quando si avvia la terapia con il dosaggio di stalevo può essere richiesto un farmaco antiipertensivo.
Antidepressivi triciclici
Sono stati segnalati reazioni avverse tra cui ipertensione e discinesia derivanti dall'uso concomitante del triciclico antidepressivi e carbidopa/levodopa.
Antagonisti del recettore della dopamina D2
Gli antagonisti del recettore della dopamina D2 (ad es. Le fenotiazine metoclopramide butirofenoni risperidone) possono ridurre gli effetti terapeutici della levodopa.
Isoniazide
Isoniazide may reduce the therapeutic effects of levodopa a dose increase may be necessary.
Phable
È stato riportato che gli effetti benefici della levodopa nella malattia di Parkinson sono stati invertiti dalla fenitoina. I pazienti che assumono fenitoina con carbidopa/levodopa devono essere attentamente osservati per la perdita di risposta terapeutica. Il dosaggio di stalevo dovrebbe essere aumentato come clinicamente necessario nei pazienti che ricevono fenitoina.
Papaverina
Gli effetti benefici della levodopa nella malattia di Parkinson sono stati riportati invertiti dalla papaverina. I pazienti che assumono papaverina con carbidopa/levodopa devono essere attentamente osservati per la perdita di risposta terapeutica. Il dosaggio di stalevo dovrebbe essere aumentato come clinicamente necessario nei pazienti che ricevono papaverina.
Sali di ferro
I sali di ferro o le multi vitamine contenenti sali di ferro devono essere somministrati con cautela. I sali di ferro possono formare chelati con levodopa carbidopa e entacapone e di conseguenza ridurre la biodisponibilità di levodopa carbidopa e entacapone.
Farmaci noti per interferire con la glucuronidazione dell'escrezione biliare e la beta-glucuronidasi intestinale
Poiché la maggior parte dell'escrezione di entacapone è tramite il Anche A cautela dovrebbe essere esercitata quando i farmaci noti per interferire con la glucuronidazione dell'escrezione biliare e la beta-glucuronidasi intestinale sono somministrati contemporaneamente con entecapone. Questi includono la colestyramina probenecid e alcuni antibiotici (ad es. Eritromicina di rifampicina ampicillina e cloramfenicolo).
Farmati metabolizzati tramite CYP2C9 (ad es. Coumadina)
Il dosaggio di Stalevo dovrebbe essere regolato come clinicamente necessario nei pazienti che utilizzano altri farmaci metabolizzati tramite CYP2C9. Uno studio di interazione su volontari sani Entacapone ha aumentato in media l'AUC di R-Warfarin del 18% e i valori INR in media del 13%. Casi di aumento dell'INR nei pazienti in concomitanza utilizzando warfarin sono stati segnalati durante l'uso post-approvazione di entecapone. Pertanto, si raccomanda il monitoraggio di INR quando viene avviato il trattamento con stalevo per i pazienti che ricevono warfarin.
Avvertimenti per Stalevo
Incluso come parte del PRECAUZIONI sezione.
Precauzioni per Stalevo
Le seguenti reazioni avverse descritte in questa sezione sono correlate ad almeno uno dei componenti di Stalevo (cioè Levodopa carbidopa e/o entacapone) in base all'esperienza di sicurezza negli studi clinici (in particolare studi fondamentali) o nei rapporti post -marketing.
Addormentarsi durante le attività di vita quotidiana e sonnolenza
I pazienti con malattia di Parkinson trattati con stalevo o altri prodotti Carbidopa/Levodopa si sono riportati improvvisamente che si sono addormentati senza preavviso senza preavviso mentre sono impegnati in attività della vita quotidiana (compreso il funzionamento dei veicoli a motore). Alcuni di questi episodi hanno provocato incidenti. Sebbene molti di questi pazienti abbiano riferito di sonnolenza durante l'assunzione di entecapone, alcuni non percepiscono segnali di avvertimento come eccessiva sonnolenza e credevano di essere stati vigili immediatamente prima dell'evento. Alcuni di questi eventi sono stati segnalati fino a un anno dopo l'inizio del trattamento.
Sonnolenza was reported in 2% of patients taking entacapone E 0% in placebo in controlled trials. It is reported that falling asleep while engaged in activities of daily living always occurs in a setting of pre-existing somnolence although patients may not give such a history. For this reason prescribers should reassess patients for sonnolenza or sleepiness especially since some of the events occur well after the start of treatment. Prescribers should also be aware that patients may not acknowledge sonnolenza or sleepiness until directly questioned about sonnolenza or sleepiness during specific activities. Patients who have already experienced somnolence E/or an episode of sudden sleep onset should not participate in these activities during treatment with Stalevo.
Prima di iniziare il trattamento con Stalevo consiglia ai pazienti il potenziale per sviluppare sonnolenza e chiedere specificamente i fattori che possono aumentare questo rischio come l'uso di farmaci sedativi concomitanti e la presenza di disturbi del sonno. Se un paziente sviluppa sonnolenza diurna o episodi di addormentarsi durante le attività che richiedono la partecipazione attiva (ad esempio conversazioni che mangiano ecc.) Stalevo dovrebbe essere normalmente interrotto [vedi Dosaggio e amministrazione E Avvertimenti e precauzioni ]. If the decision is made to continue Stalevo patients should be advised not to drive E to avoid other potentially dangerous activities. There is insufficient information to establish whether dose reduction will eliminate episodes of falling asleep while engaged in activities of daily living.
Ipotensione Orthostatic Ipotensione And Syncope
Le segnalazioni di Syncope erano generalmente più frequenti in pazienti in entrambi i gruppi di trattamento che avevano avuto un episodio precedente di ipotensione documentata (sebbene gli episodi di sincope ottenuti dalla storia non fossero essi stessi documentati con misurazione dei segni vitali). Ipotensione e sincope ortostatica ipotensione sono osservati nei pazienti trattati con farmaci che aumentano il tono dopaminergico centrale, incluso lo stalevo.
Discinesia
Discinesia (involontario movements) may occur or be exacerbated at lower dosages E sooner with Stalevo than with preparations containing only carbidopa E levodopa. The occurrence of dyskinesias may require dosage reduction.
Negli studi fondamentali l'incidenza della differenza di trattamento della discinesia è stata del 10% e per carbidopa-levodopa più 200 mg di entacapone. Sebbene la riduzione della dose di levodopa possa migliorare questo effetto collaterale, molti pazienti in studi controllati hanno continuato a sperimentare discinesie frequenti nonostante una riduzione della loro dose di levodopa. L'incidenza della differenza di trattamento del ritiro dello studio per la discinesia è stata dell'1% per il carbidopa-levodopa-eNtacapone.
Depressione e suicidalità
Tutti i pazienti devono essere osservati attentamente per lo sviluppo della depressione con tendenze suicide concomitanti. I pazienti con psicosi passate o attuali devono essere trattati con cautela.
Allucinazioni e/o comportamento psicotico
La terapia dopaminergica nei pazienti con malattia di Parkinson è stata associata ad allucinazioni. Le allucinazioni hanno portato alla sospensione dei farmaci e al ritiro prematuro da studi clinici nello 0,8% e lo 0% dei pazienti trattati con rispettivamente con carbidopa levodopa entecapone e carbidopa levodopa. Le allucinazioni hanno portato al ricovero in ospedale nell'1,0% e lo 0,3% dei pazienti nei gruppi di entecapone di Carbidopa Levodopa e Carbidopa Levodopa. L'agitazione si è verificata nell'1% dei pazienti trattati con carbidopa levodopa entecapone e 0% trattati con levodopa carbidopa.
Controllo degli impulsi e/o comportamenti compulsivi
I rapporti post-marketing suggeriscono che i pazienti trattati con farmaci anti-Parkinson possono sperimentare impulsi intensi a scommettere aumentando impulsi sessuali di intensi impulsi a spendere soldi in modo incontrollabile e altri impulsi intensi. I pazienti possono non essere in grado di controllare questi impulsi durante l'assunzione di uno o più farmaci generalmente utilizzati per il trattamento della malattia di Parkinson e che aumentano il tono dopaminergico centrale, incluso l'entacapone assunto con levodopa e carbidopa. In alcuni casi, sebbene non tutti questi impulsi si siano fermati quando la dose di farmaci anti-parkinson è stata ridotta o sospesa. Poiché i pazienti potrebbero non riconoscere questi comportamenti come anormali, è importante che i prescrittori chiedano specificamente ai pazienti o ai loro caregiver sullo sviluppo di impulsi di gioco nuovi o aumentati di impulsi sessuali spese incontrollate o altri impulsi mentre vengono trattati con entacapone. I medici dovrebbero prendere in considerazione la riduzione della dose o l'interruzione di Stalevo se un paziente sviluppa tali impulsi durante l'assunzione di stalevo [vedi Dosaggio e amministrazione Avvertimenti e precauzioni ].
Iperpyrexia e confusione emergente di ritiro
Casi di iperpyrexia e confusione che assomigliano alla sindrome neurolettica maligna (NMS) sono stati riportati in associazione con riduzione della dose o ritiro della terapia con levodopa carbidopa ed entacapone. Tuttavia, in alcuni casi, l'iperpyrexia e la confusione sono stati riportati dopo l'inizio del trattamento con entacapone. L'iperpyrexia e la confusione sono rari ma possono essere letali con una varietà di caratteristiche tra cui iperpyrexia/febbre/ipertermia Rigidità muscolare I movimenti involontari hanno alterato la coscienza/stato mentale modifica la disfunzione autonomica del tachycardia tachycardia Myoglobinuria e aumento della mioglobina sierica).
Se un paziente deve interrompere o ridurre la loro dose giornaliera di stalevo, la dose dovrebbe essere ridotta lentamente con la supervisione di un operatore sanitario [vedi Dosaggio e amministrazione ]. Specific methods for tapering entacapone have not been systematically evaluated.
Diarrea And Colitis
Negli studi clinici di diarrea di entacapone si sono sviluppati in 60 su 603 (NULL,0%) e 16 su 400 (NULL,0%) dei pazienti trattati con 200 mg di entecapone o placebo in combinazione con l'inibitore di levodopa e DOPA decarbossilasi rispettivamente. Nei pazienti trattati con diarrea di entacapone era generalmente da lieve a moderato di gravità (NULL,6%) ma era considerato grave nell'1,3%. La diarrea ha comportato un ritiro in 10 su 603 (NULL,7%) pazienti 7 (NULL,2%) con diarrea lieve e moderata e 3 (NULL,5%) con diarrea grave. La diarrea è stata generalmente risolta dopo l'interruzione dell'tacapone. Due pazienti con diarrea sono stati ricoverati in ospedale. Tipicamente la diarrea si presenta entro 4-12 settimane dall'inizio dell'endtacapone, ma può apparire già nella prima settimana e fino a tardi tanti mesi dopo l'inizio del trattamento. La diarrea può essere associata alla disidratazione per la perdita di peso e all'iprokalemia.
L'esperienza post-marketing ha dimostrato che la diarrea può essere un segno di colite microscopica indotta da farmaci principalmente linfocita. In questi casi la diarrea è stata generalmente da moderata a grave acquosa e non sangue a volte associata alla perdita di peso del dolore addominale di disidratazione. Nella maggior parte dei casi diarrea e altri sintomi correlati alla colite si sono risolti o migliorati significativamente quando il trattamento con entacapone è stato interrotto. In alcuni pazienti con biopsia confermata la colite diarrea si era risolta o significativamente migliorata dopo l'interruzione di entecapone ma si è ricorreta dopo il ritiro con entecapone.
Se si sospetta che la diarrea prolungata sia correlata a stalevo, il farmaco dovrebbe essere sospeso e considerata un'adeguata terapia medica. Se la causa della diarrea prolungata rimane poco chiara o continua dopo aver interrotto l'endtacapone, dovrebbero essere prese in considerazione ulteriori indagini diagnostiche tra cui colonscopia e biopsie.
Rabdomiolisi
Casi di rabdomiolisi grave sono stati riportati con entecapone se usati in combinazione con carbidopa e levodopa. Una grave attività motoria prolungata, compresa la discinesia, può eventualmente spiegare la rabdomiolisi. La maggior parte dei casi è stata manifestata dalla mialgia e aumentando i valori della creatina fosfocinasi (CPK) e mioglobina. Alcune delle reazioni includevano anche febbre e/o alterazione della coscienza. È anche possibile che la rabdomiolisi possa essere il risultato della sindrome descritta nell'iperpyrexia e confusione emergente di astinenza [vedi Avvertimenti e precauzioni ].
Interazione con i farmaci metabolizzati da COMT
Drugs known to be metabolized by COMT such as isoproterenol epinephrine norepinephrine dopamine dobutamine alpha-methyldopa apomorphine isoetherine and bitolterol should be administered with caution in patients receiving entacapone regardless of the route of administration (including inhalation) as their interaction may result in increased heart rate arrhythmia and/or increased blood pressure.
Complicanze fibrotiche
In alcuni pazienti sono stati riportati casi di fibrosi retroperitoneale infiltrati pleurici e ispessimento pleurico in alcuni pazienti trattati con agenti dopaminergici derivati da ERGOT. Queste complicanze possono risolvere quando il farmaco viene interrotto ma la risoluzione completa non si verifica sempre. Sebbene queste reazioni avverse possano essere correlate alla struttura di ergolina di questi composti è stato anche preso in considerazione anche un possibile ruolo causale dei farmaci derivati da nonno (ad es. Entacapone levodopa) che aumentano l'attività dopaminergica. L'incidenza prevista di complicanze fibrotiche è così bassa che anche se l'endtacapone ha causato queste complicanze a tassi simili a quelli attribuibili ad altre terapie dopaminergiche, è improbabile che sarebbe stata rilevata in una coorte delle dimensioni esposte all'entacapone durante il suo sviluppo clinico. Durante lo sviluppo clinico di entecapone sono stati riportati quattro casi di fibrosi polmonare; 3 di questi pazienti sono stati anche trattati con pergolide e 1 con bromocriptina. La durata del trattamento con entacapone variava da 7 mesi a 17 mesi.
Patora dell'ulcera peptica
Come per il trattamento con levodopa con stalevo può aumentare la possibilità di emorragia gastrointestinale superiore in pazienti con una storia di ulcera peptica.
Compromissione epatica
I pazienti con compromissione epatica devono essere trattati con cautela [vedi Farmacologia clinica ]. As with levodopa periodic evaluation of hepatic function is recommended during extended therapy.
Test di laboratorio
Le anomalie nei test di laboratorio possono includere aumenti dei test di funzionalità epatica come la fosfatasi alcalina SGOT (AST) SGPT (ALT) lattocrogenasi lattocro e bilirubina. Anomalie nel sangue urea Sono stati anche riportati test di coombaso di azoto e positivo. Comunemente i livelli di azoto di urea nel sangue creatinina e acido urico sono più bassi durante la somministrazione di stalevo che con levodopa.
Stalevo may cause a false-positive reaction for urinary ketone bodies when a test tape is used for determination of ketonuria . This reaction will not be altered by boiling the urine specimen. False-negative tests may result with the use of glucose-oxidase methods of testing for glucosuria. Cases of falsely diagnosed pheochromocytoma in patients on carbidopa/levodopa therapy have been reported very rarely.
Attenzione dovrebbe essere esercitata durante l'interpretazione dei livelli plasmatici e delle urine delle catecolamine e dei loro metaboliti nei pazienti in terapia carbidopa/levodopa.
Informazioni sulla consulenza del paziente
Addormentarsi durante le attività di vita quotidiana e sonnolenza
Consiglia ai pazienti il potenziale per gli effetti sedativi associati a Stalevo, tra cui la sonnolenza e la possibilità di addormentarsi mentre si è impegnati in attività della vita quotidiana. Poiché la sonnolenza può essere una frequente reazione avversa con conseguenze potenzialmente gravi, i pazienti non dovrebbero guidare un veicolo a motore azionare macchinari pesanti o impegnarsi in altre attività potenzialmente pericolose fino a quando non hanno acquisito un'esperienza sufficiente con Stalevo per determinare se colpisce o meno le loro prestazioni mentali e/o motorie. Avvertimenti e precauzioni ]. Advise patients that if increased somnolence or episodes of falling asleep during activities of daily living (e.g. conversations eating driving a motor vehicle etc.) are experienced at any time during treatment they should not drive or participate in potentially dangerous activities until they have contacted their physician.
Consiglia ai pazienti di parlare con il loro prescrittore sanitario prima di assumere farmaci sedati alcolici o altri depressivi del SNC (ad esempio antidepressivi antipsicotici benzodiazepine ecc.) A causa dei possibili effetti additivi in combinazione con lo stalevo.
Ipotensione Orthostatic Ipotensione And Syncope
Consiglia ai pazienti che possono sviluppare ipotensione posturale (o ortostatica) sintomatica (o asintomatica) o ipotensione non ortatica durante l'assunzione di Stalevo. Ipotensione/ipotensione ortostatica può verificarsi più frequentemente durante la terapia iniziale. I pazienti non devono salire rapidamente dopo essersi seduti o sdraiati soprattutto se lo hanno fatto per periodi prolungati e in particolare all'inizio del trattamento con Stalevo.
Consiglia ai pazienti il potenziale per la sincope nei pazienti che utilizzano agonisti della dopamina. Per questo motivo informare i pazienti sulla possibilità di sincope durante l'assunzione di stalevo [vedi Avvertimenti e precauzioni ].
Discinesias
Informare i pazienti che Stalevo può causare e/o esacerbare discinesie preesistenti [vedi Avvertimenti e precauzioni ].
Allucinazioni e/o comportamento psicotico
Informare i pazienti che possono verificarsi allucinazioni e altri comportamenti psicotici mentre si prende lo stalevo [vedi Avvertimenti e precauzioni ].
Controllo degli impulsi e/o comportamenti compulsivi
Consiglia ai pazienti che possono sperimentare il controllo degli impulsi e/o comportamenti compulsivi durante l'assunzione di uno o più farmaci utilizzati per il trattamento della malattia di Parkinson, incluso Stalevo. Chiedere ai pazienti lo sviluppo di impulsi di gioco nuovi o maggiori impulsi di impulsi sessuali per la spesa incontrollata o altri impulsi intensi mentre vengono trattati con Stalevo. Consiglia ai pazienti di informare il proprio medico o un operatore sanitario se sperimentano impulsi di gioco nuovi o maggiori aumenti di impulsi sessuali o altri impulsi intensi durante l'assunzione di Stalevo. I medici dovrebbero prendere in considerazione la riduzione della dose o l'interruzione del farmaco se un paziente sviluppa tali impulsi durante l'assunzione di stalevo [vedi Avvertimenti e precauzioni ].
Iperpyrexia e confusione emergente di ritiro
Consiglia ai pazienti che possono sviluppare febbre e confusione come parte di una sindrome che ricorda NMS e possibilmente con altre caratteristiche cliniche (ad esempio iper o ipotensione della disfunzione autonoma di rigidità muscolare ecc.). Questa sindrome da febbre e confusione può verificarsi in particolare con riduzioni della dose o ritiro di Stalevo, ma può anche svilupparsi dopo l'inizio del trattamento. Consiglia ai pazienti di contattare il proprio operatore sanitario se desiderano interrompere o ridurre la dose di stalevo e di contattare un operatore sanitario se sviluppano febbre e confusione [vedi Avvertimenti e precauzioni ].
Diarrea And Colitis
Informare i pazienti che la diarrea può verificarsi con Stalevo e può avere un esordio ritardato. A volte la diarrea prolungata può essere causata dalla colite (infiammazione dell'intestino crasso). I pazienti con diarrea devono bere liquidi per mantenere un'adeguata idratazione e monitorare la perdita di peso. Se la diarrea associata allo stalevo è prolungato di interrompere il farmaco, dovrebbe portare alla risoluzione. Se la diarrea continua dopo aver interrotto lo stalevo è necessario ulteriori indagini diagnostiche. In alcuni casi la diarrea può essere associata alla colite [vedi Avvertimenti e precauzioni ].
Rabdomiolisi
Consiglia ai pazienti che possono sviluppare rabdomiolisi e mialgia se sperimentano un'attività motoria prolungata compresa la discinesia. Questo evento può anche essere associato alla febbre e alla confusione [vedi Avvertimenti e precauzioni ].
Nausea And Vomito
Informare i pazienti che lo stalevo può causare nausea e vomito può verificarsi più frequentemente durante la terapia iniziale e può richiedere un aggiustamento della dose.
Istruzioni per l'uso
Istruire i pazienti a prendere Stalevo solo come prescritto. Istruisci i pazienti a prendere solo una singola compressa di stalevo ad ogni intervallo di dosaggio. Istruisci i pazienti a non prendere più compresse o porzioni aggiuntive di compresse per ottenere una dose più elevata di levodopa. Consiglia ai pazienti di non dividere la cotta o masticare lo stalevo.
Informare il paziente che Stalevo è una formulazione di carbidopa/levodopa combinata con entacapone progettato per iniziare il rilascio di ingredienti entro 30 minuti dall'ingestione. È importante che lo stalevo sia preso a intervalli regolari secondo il programma delineato dal medico. Attenzione al paziente di non cambiare il regime di dosaggio prescritto e di non aggiungere ulteriori farmaci antiparkinsoniani tra cui altri preparativi carbidopa/levodopa senza prima consultare il medico.
Consiglio ai pazienti che gli episodi fuori (usura dell'effetto farmaco) si verificano alla fine dell'intervallo di dosaggio, ma possono verificarsi imprevedibili episodi in qualsiasi momento. Consiglia al paziente di avvisare un operatore sanitario per possibili aggiustamenti del trattamento se tale risposta pone un problema alla vita quotidiana del paziente.
Consiglia ai pazienti che la colorazione scura (marrone rosso o nero) può apparire nelle urine o sul sudore della saliva dopo aver preso Stalevo. Sebbene il colore sembri essere clinicamente insignificanti gli indumenti possono essere scoloriti.
Consiglia ai pazienti che un cambiamento nella dieta per gli alimenti ricchi di proteine può ritardare l'assorbimento della levodopa. L'acidità eccessiva ritarda anche lo svuotamento dello stomaco ritardando così l'assorbimento di levodopa. I sali di ferro (come nelle compresse multi-vitaminici) possono anche ridurre l'efficacia di Stalevo.
Gravidanza
Istruire i pazienti a avvisare il proprio operatore sanitario se rimangono incinta o intendono rimanere incinta durante la terapia [vedi Utilizzare in popolazioni specifiche ].
Lattazione
Istruire i pazienti a avvisare il proprio operatore sanitario se intendono allattare o stanno allattando un bambino [vedi Utilizzare in popolazioni specifiche ].
Tossicologia non clinica
Mutagenesi della carcinogenesi compromissione della fertilità
Carcinogenesi
Nei ratti la somministrazione orale di carbidopa-levodopa per 2 anni non ha comportato alcuna evidenza di cancerogenicità a dosi di circa 2 volte (carbidopa) -4 volte (levodopa) la massima dose umana raccomandata (MRHD).
Studi di cancerogenicità a due anni di entecapone sono stati condotti in topi e ratti. Nei topi non è stato osservato alcun aumento dei tumori a dosi orali di 100 200 e 400 mg/kg/giorno. Alla dose più alta, le esposizioni al plasma (AUC) erano 4 volte superiori a quelle nell'uomo alla massima dose giornaliera raccomandata (MRDD) di 1600 mg. Nei ratti somministrati dosi orali di 20 90 o 400 mg/kg/giorno è stata osservata una maggiore incidenza di adenomi e carcinomi tubulari renali nei maschi alla più alta dose testata. Le AUC plasmatiche alla dose più elevata non associate ad un aumento dei tumori renali (90 mg/kg/giorno) erano circa 5 volte quello nell'uomo al MRDD di Entacapone.
Il potenziale cancerogeno di entacapone somministrato in combinazione con carbidopa-levodopa non è stato valutato.
Mutagenesi
Carbidopa era mutagenico nel dosaggio della mutazione inversa batterica in vitro (AMES) in presenza e assenza di attivazione metabolica e nel test della timidina chinasi del linfoma chinasi (TK) in vitro in assenza di attivazione metabolica. Carbidopa era negativo nel test del micronucleo del topo in vivo.
Entacapone was mutagenic E clastogenic in the in vitro mouse lymphoma tk assay in the presence E absence of metabolic activation E was clastogenic in cultured human lymphocytes in the presence of metabolic activation. Entacapone either alone or in combination with carbidopa-levodopa was negative in the in vivo mouse micronucleus E in the Ames assays.
Compromissione della fertilità
Negli studi di riproduzione non sono stati riscontrati effetti sulla fertilità nei ratti che ricevono carbidopa-levodopa a dosi di circa 2 volte (carbidopa) -4 volte (Levodopa) il MRHD.
Nei ratti trattati per via orale con entacapone (fino a 700 mg/kg/giorno) non sono stati osservati effetti sulla fertilità o sulle prestazioni riproduttive generali. Le esposizioni al plasma (AUC) alla dose più alta testate sono state circa 30 volte quella negli umani al MRHD di Entacapone. L'accoppiamento ritardato era evidente nelle femmine alla dose più alta testata.
Utilizzare in popolazioni specifiche
Gravidanza
Riepilogo del rischio
Non ci sono dati adeguati sul rischio di sviluppo associato all'uso di Stalevo nelle donne in gravidanza. Nella somministrazione di animali di carbidopa-levodopa o entacapone durante la gravidanza è stata associata alla tossicità dello sviluppo, tra cui un aumento delle incidenze di malformazioni fetali (vedi Dati ). Il rischio di background stimato di importanti difetti alla nascita e aborto spontaneo nella popolazione indicata non è noto. Nella popolazione generale degli Stati Uniti i rischi di base stimati di importanti difetti alla nascita e aborti di aborto nelle gravidanze clinicamente riconosciute sono rispettivamente dal 2 al 4% e dal 15 al 20%.
Dati
Dati sugli animali
In studi non clinici in cui è stata somministrata carbidopa-levodopa ad animali in gravidanza aumentati incidenze di malformazioni viscerali e scheletriche nei conigli a tutte le dosi e i rapporti di carbidopa-levodopa, che si sono verificati da 10 volte (carbidopa) -5 volte (levodopa a 20 volte (carbidopa). dose (MRHD) di 1600 mg/giorno. Nei ratti si è verificata una diminuzione del numero di cuccioli vivi consegnati da dighe che hanno ricevuto circa due volte (carbidopa)-volte tempi (Levodopa) il MRHD in tutta l'organogenesi. Non sono stati osservati effetti sulle frequenze di malformazione nei topi che ricevono fino a 20 volte il MRHD di Carbidopa-Levodopa.
Negli studi di sviluppo embrionale di embrioni di animali in gravidanza entecapone hanno ricevuto dosi fino a 1000 mg/kg/die (ratti) o 300 mg/kg/giorno (conigli) durante l'organogenesi. L'aumento delle incidenze di variazioni fetali erano evidenti nelle cucciolate dei ratti trattati con la dose più alta in assenza di segni palesi di tossicità materna. L'esposizione al plasma di entecapone materno (AUC) associata a questa dose era di circa 34 volte quella negli umani al MRHD. Sono state osservate maggiori frequenze di aborti e riassorbimento in ritardo/totali e una riduzione dei pesi fetali nelle cucciolate dei conigli trattati con dosi maternamente tossiche di 100 mg/kg/giorno (AUC plasmatiche inferiori a quelli nell'uomo del MRHD). Non ci sono stati aumenti dei tassi di malformazione in questi studi.
Quando l'entacapone fu somministrato ai ratti femminili prima dell'accoppiamento e durante la gestazione precoce fu osservata una maggiore incidenza di anomalie oculari fetali (macroftalmia microftalmia anophtalmia) nei litte delle dighe trattate con dosi di 160 mg/kg/giorno (plasma aucs sette volte in mrhd) o maggiore in materia di tossici. Somministrazione di fino a 700 mg/kg/die (AUC al plasma 28 volte quella nell'uomo del MRHD) ai ratti durante l'ultima parte della gestazione e durante l'allattamento non ha prodotto prove di compromissione dello sviluppo nella prole.
Lattazione
Riepilogo del rischio
Levodopa è stata rilevata nel latte umano dopo la somministrazione di carbidopa-levodopa. Non ci sono dati sulla presenza di entecapone o carbidopa nel latte umano gli effetti di Levodopa carbidopa o entacapone sul bambino allattato al seno o sugli effetti sulla produzione di latte. Tuttavia, può verificarsi inibizione dell'allattamento perché la levodopa diminuisce la secrezione di prolattina [vedi Farmacologia clinica ]. Carbidopa E entacapone are excreted in rat milk. In lactating rat oral administration of radiolabeled entacapone resulted in levels of entacapone E/or metabolites in milk up to 2 to 3 times that in plasma. The developmental E health benefits of breastfeeding should be considered along with the mother's clinical need for Stalevo E any potential adverse effects on the breastfed infant from Stalevo or from the underlying maternal condition.
Uso pediatrico
La sicurezza ed efficacia nei pazienti pediatrici non è stata stabilita.
Uso geriatrico
Del numero totale di soggetti negli studi clinici di Stalevo, il 43,8% aveva 65 anni e più, mentre il 7,2% aveva 75 anni e oltre. Non sono state osservate differenze complessive nella sicurezza o nell'efficacia tra questi soggetti e i soggetti più giovani e altre esperienze cliniche riportate non hanno identificato differenze nelle risposte tra i pazienti anziani e più giovani; Tuttavia, non può essere esclusa una maggiore sensibilità di alcuni anziani.
Stalevo tablets have not been studied in La malattia di Parkinson patients or in healthy volunteers older than 75 years [see Farmacologia clinica ].
Compromissione renale
La compromissione renale non influisce sulla farmacocinetica di entacapone. Non ci sono studi sulla farmacocinetica di Levodopa e Carbidopa nei pazienti con compromissione renale [vedi Farmacologia clinica ].
Compromissione epatica Or Biliary Obstruction
Non ci sono studi sulla farmacocinetica di Carbidopa e Levodopa in pazienti con compromissione epatica. Stalevo deve essere somministrato con cautela ai pazienti con ostruzione biliare o malattia epatica poiché l'escrezione biliare sembra essere la principale via di escrezione di entecapone e la compromissione epatica ha avuto un effetto significativo sulla farmacocinetica di entecapone quando 200 mg di entecapone è stato somministrato da solo [vedi Farmacologia clinica ].
Informazioni per overdose per Stalevo
Segni e sintomi di sovradosaggio
Ci sono pochissimi casi di sovradosaggio con levodopa riportati nella letteratura pubblicata. Sulla base delle informazioni disponibili, ci si può aspettare che i sintomi acuti del sovradosaggio dell'inibitore della levodopa e della DOPA decarbossilasi derivano dalla sovrastimolazione dopaminergica. Le dosi di alcuni grammi possono provocare disturbi del SNC con una crescente probabilità di disturbo cardiovascolare (ad esempio tachicardia ipotensione) e problemi psichiatrici più gravi a dosi più elevate. Un rapporto isolato di rabdomiolisi e un altro di insufficienza renale transitoria suggerisce che il sovradosaggio di levodopa può dare origine a complicanze sistemiche secondarie alla sovrastimolazione dopaminergica.
L'inibizione COMT mediante il trattamento con entacapone è dose-dipendente. Un enorme sovradosaggio di entecapone può teoricamente produrre un'inibizione del 100% dell'enzima COMT nelle persone, impedendo così la metilazione O di cateco endogeni ed esogeni.
Negli studi clinici la più alta dose singola di entecapone somministrata all'uomo era di 800 mg con conseguente concentrazione plasmatica di 14,1 mcg per ml. La dose giornaliera più alta somministrata all'uomo è stata somministrata 2400 mg in uno studio come 400 mg sei volte al giorno con Carbidopa/Levodopa per 14 giorni in 15 pazienti con malattia di Parkinson e in un altro studio come 800 mg tre volte al giorno per 7 giorni in 8 volontari sani. A questa dose giornaliera le concentrazioni plasmatiche di picco di entacapone erano in media 2,0 mcg per ml (a 45 minuti rispetto a 1,0 mcg per ml e 1,2 mcg per ml con entecapone da 200 mg a 45 minuti). Il dolore addominale e le feci sciolte sono stati gli eventi avversi più comunemente osservati durante questo studio. Dosi giornaliere fino a 2000 mg di entacapone sono state somministrate come 200 mg 10 volte al giorno con carbidopa/levodopa o benserazide/levodopa per almeno 1 anno in 10 pazienti per almeno 2 anni in 8 pazienti e per almeno 3 anni in 7 pazienti. Nel complesso, tuttavia, l'esperienza clinica con dosi giornaliere superiori a 1600 mg è limitata.
Gestione del sovradosaggio
È consigliato il ricovero in ospedale e le misure di supporto generali dovrebbero essere impiegate insieme a lavaggi gastrici immediati e ripetute dosi di carbone nel tempo. Ciò può accelerare l'eliminazione di entacapone in particolare diminuendo il suo assorbimento e riassorbimento dal tratto gastrointestinale. I fluidi per via endovenosa dovrebbero essere somministrati con giudizio e mantenute una vie aerea adeguata.
La funzione circolatoria e renale respiratoria deve essere monitorata e le misure di supporto appropriate impiegate. Il monitoraggio elettrocardiografico deve essere istituito e il paziente osservato con cura per lo sviluppo di aritmie; Se richiesto dovrebbe essere somministrata una terapia antiaritmica appropriata. La possibilità che il paziente possa aver assunto altri farmaci aumentando il rischio di interazioni farmacologiche (in particolare farmaci strutturati dalla catecolo) dovrebbe essere presa in considerazione. Ad oggi non è stata segnalata alcuna esperienza con dialisi; Quindi il suo valore nel sovradosaggio non è noto. È improbabile che l'emodialisi o l'emoperfusione riducano i livelli di entecapone a causa del suo alto legame con le proteine plasmatiche. La piridossina non è efficace nell'invertire le azioni di Stalevo.
Controindicazioni per Stalevo
Stalevo is contraindicated in patients:
- Assunzione di inibitori della monoamina ossidasi non selettiva (MAO) (ad esempio fenelzina e tranlilcipromina). Questi inibitori MAO non selettivi devono essere sospesi almeno due settimane prima di iniziare la terapia con Stalevo.
- Con angolo stretto glaucoma .
Farmacologia clinica for Stalevo
Meccanismo d'azione
Levodopa
Le prove attuali indicano che i sintomi della malattia di Parkinson sono correlati all'esaurimento della dopamina nel corpus striato. La somministrazione di dopamina è inefficace nel trattamento della malattia di Parkinson perché non attraversa la barriera emato-encefalica. Tuttavia levodopa il precursore metabolico della dopamina attraversa la barriera emato-encefalica ed è presumibilmente convertito in dopamina nel cervello. Si pensa che questo sia il meccanismo in base al quale Levodopa allevia i sintomi della malattia di Parkinson.
Carbidopa
Quando la levodopa viene somministrata per via orale, viene rapidamente decarbossilata nella dopamina nei tessuti extracerebrali in modo che solo una piccola parte di una determinata dose venga trasportata invariata nel sistema nervoso centrale. Carbidopa inibisce la decarbossilazione della levodopa periferica che rende più levodopa disponibile per la consegna al cervello.
Entacapone
Entacapone is a selective E reversible inhibitor of catechol-O-methyltransferase (COMT).
COMT catalizza il trasferimento del gruppo metilico di s-adenosil-L-metionina al gruppo fenolico di substrati che contengono una struttura catecolo. I substrati fisiologici di COMT includono catecolamine DOPA (dopamina noradrenalina ed epinefrina) e i loro metaboliti idrossilati. Quando la decarbossilazione di Levodopa è prevenuta da Carbidopa Comt diventa il principale enzima metabolizzante per levodopa che catalizza il suo metabolismo in 3-metossi-4- idrossi-lfenilalanina (3-OMD).
Farmacocinetica
La farmacocinetica delle compresse di Stalevo è stata studiata in soggetti sani (dai 45 anni a 75 anni). Complessivamente dopo la somministrazione di dosi corrispondenti di levodopa carbidopa ed entacapone come stalevo o come carbidopa e levodopa Product Plus Comtan (ENtacapone) compresse Le concentrazioni plasmatiche medie di Levodopa carbidopa ed entacapone sono comparabili.
Assorbimento e distribuzione
Sia la levodopa che l'entacapone vengono rapidamente assorbiti ed eliminati e il loro volume di distribuzione è moderatamente piccolo. Carbidopa viene assorbita ed eliminata leggermente più lentamente rispetto a Levodopa e Entecapone. Esistono sostanziali variazioni inter- e intra-individuali nell'assorbimento di Levodopa carbidopa ed entacapone in particolare per quanto riguarda il suo CMAX.
L'effetto alimentare sulla compressa Stalevo non è stato valutato. Poiché Levodopa compete con alcuni aminoacidi per il trasporto attraverso la parete intestinale, l'assorbimento di Levodopa può essere compromesso in alcuni pazienti dopo aver mangiato un pasto ad alto contenuto di proteine. I pasti ricchi di grandi aminoacidi neutri possono ritardare e ridurre l'assorbimento di levodopa [vedi Informazioni sulla consulenza del paziente ].
Levodopa
Le proprietà farmacocinetiche di Levodopa in seguito alla somministrazione di compresse stalevo a dosi monodosa (carbidopa levodopa ed entacapone) sono riassunte nella Tabella 3.
Tabella 3: Caratteristiche farmacocinetiche di Levodopa con diversi punti di forza di Stalevo (media ± DS)
| Forza della compressa | AUC0 -∞ (nanogramma • h via ml) | CMAX (nanogramma per ml) | TMAX (H) |
| 12,5 mg per 50 mg per 200 mg | 1040 ± 314 | 470 ± 154 | 1,1 ± 0,5 |
| 25 mg per 100 mg per 200 mg | 2910 ± 715 | 975 ± 247 | 1,4 ± 0,6 |
| 37,5 mg per 150 mg per 200 mg | 3770 ± 1120 | 1270 ± 329 | 1,5 ± 0,9 |
| 50 mg per 200 mg per 200 mg | 6115 ± 1536 | 1859 ± 455 | 1,76 ± 0,7 |
Levodopa is bound to plasma protein only to a minor extent (about 10% to 30%).
Carbidopa
Dopo la somministrazione di Stalevo come singola dose a soggetti sani maschi e femmine, il picco di concentrazione di carbidopa è stata raggiunta entro 2,5 ore a 3,4 ore in media. Il CMAX medio variava da circa 40 nanogrammi per ml a 225 nanogrammi per ml e l'AUC media da 170 nanogrammi • H per ml a 1200 nanogrammi • H per ml con diversi punti di forza dello stalevo che forniscono 12,5 mg 25 mg 37,5 mg o 50 mg di carbidopa.
Carbidopa is approximately 36% bound to plasma protein.
Entacapone
Dopo la somministrazione di Stalevo come singola dose a soggetti sani maschi e femmine, il picco di concentrazione di entecapone nel plasma è stato raggiunto entro 0,8 ore a 1,2 ore in media. Il cmax medio di entacapone era di circa 1200 nanogrammi per ml a 1500 nanogrammi per ml e il nanogramma AUC 1250 • H per ml a 1750 nanagram • H per ml dopo la somministrazione di diversi punti di forza dello stalevo che forniscono 200 mg di entecapone.
Il legame plasmatico della proteina di entacapone è del 98% nell'intervallo di concentrazione di 0,4 mcg per ml a 50 mcg per ml. Entecapone si lega principalmente all'albumina sierica.
Metabolismo ed eliminazione
Levodopa
L'emivita di eliminazione di Levodopa La porzione attiva dell'attività antiparkinsoniana era di 1,7 ore (intervallo da 1,1 ore a 3,2 ore).
Levodopa is extensively metabolized to various metabolites. Two major pathways are decarboxylation by dopa decarboxylase (DDC) E O-methylation by COMT.
Carbidopa
L'emivita di eliminazione di Carbidopa è stata in media da 1,6 ore a 2 ore (intervallo da 0,7 ore a 4,0 ore).
Carbidopa is metabolized to two main metabolites (α-methyl-3-methoxy-4-hydroxyphenylpropionic acid E α-methyl- 34-dihydroxyphenylpropionic acid). These 2 metabolites are primarily eliminated in the urine unchanged or as glucuronide conjugates. Unchanged carbidopa accounts for 30% of the total urinary excretion.
Entacapone
L'emivita di eliminazione di entecapone era in media da 0,8 ore a 1 ora (da 0,3 ore a 4,5 ore).
Entacapone is almost completely metabolized prior to excretion with only a very small amount (0.2% of dose) found unchanged in urine. The main metabolic pathway is isomerization to the cis-isomer the only active metabolite. Entacapone E the cis-isomer are eliminated in the urine as glucuronide conjugates. The glucuronides account for 95% of all urinary metabolites (70% as parent E 25% as cis-isomer glucuronides). The glucuronide conjugate of the cis-isomer is inactive. After oral administration of a 14 La dose marcata in C di entacapone il 10% del genitore e metabolita marcato viene escreto nelle urine e il 90% nelle feci.
A causa di una breve emittente emittente, nessun vero accumulo di levodopa o entacapone si verifica quando vengono somministrati ripetutamente.
Compromissione renale
Entacapone
La farmacocinetica di entacapone è stata studiata dopo una singola dose di entacapone di 200 mg in soggetti con funzioni renali normali moderate e gravemente compromesse senza levodopa e la configurazione dell'inibitore della DOPA decarbossilasi. Non sono stati trovati effetti significativi della funzione renale sulla farmacocinetica di entacapone.
Levodopa And carbidopa
Nessun studio sulla farmacocinetica di Levodopa e Carbidopa nei pazienti con compromissione renale.
Compromissione epatica
Entacapone
La compromissione epatica ha avuto un effetto significativo sulla farmacocinetica di entacapone quando sono stati somministrati 200 mg di entecapone. Una singola dose di 200 mg di entecapone senza co-somministrazione dell'inibitore della levodopa e della DOPA decarbossilasi ha mostrato valori AUC e CMAX di circa 2 volte più alti in pazienti con una storia di alcolismo e compromissione epatica (n = 10) rispetto ai soggetti normali (n = 10). Tutti i pazienti presentavano cirrosi epatica proveniente dalla biopsia causata dall'alcol. Secondo la classificazione infantile 7 pazienti con malattia epatica avevano un lieve compromissione epatica e 3 pazienti avevano un moderato deterioramento epatico. Poiché solo circa il 10% della dose di entacapone viene escreto nelle urine come composto genitore e l'escrezione biliare con glucuronide coniugata sembra essere la principale via di escrezione di questo farmaco. Stalevo dovrebbe essere somministrato con cura ai pazienti con ostruzione biliare o malattia epatica.
Levodopa And Carbidopa
Non ci sono studi sulla farmacocinetica di Levodopa e Carbidopa nei pazienti con compromissione epatica.
Uso geriatrico
Negli studi di farmacocinetica condotti su volontari sani a seguito di una singola dose di tavolette carbidopa-levodopa e entecapone (come stalevo o come separate carbidopa/levodopa e comtan):
Levodopa
L'AUC di Levodopa è significativamente (in media dal 10% al 20%) più alto negli anziani (da 60 anni a 75 anni) rispetto ai soggetti più giovani (da 45 anni a 60 anni). Non vi è alcuna differenza significativa nel CMAX di Levodopa tra soggetti più giovani (da 45 anni a 60 anni) e anziani (da 60 anni a 75 anni).
Carbidopa
Non vi è alcuna differenza significativa nel CMAX e nell'AUC di Carbidopa tra i soggetti più giovani (da 45 anni a 60 anni) e anziani (da 60 anni a 75 anni).
Entacapone
L'AUC di Entacapone è significativamente (in media del 15%) più alto negli anziani (da 60 anni a 75 anni) rispetto ai soggetti più giovani (da 45 anni a 60 anni). Non vi è alcuna differenza significativa nel CMAX di Entacapone tra soggetti più giovani (da 45 anni a 60 anni) e anziani (da 60 anni a 75 anni).
Genere
Farmacocinetica following a single dose of carbidopa levodopa E entacapone together either as Stalevo or as separate carbidopa/levodopa E Comtan tablets in healthy volunteers (age range 45 years to 74 years):
Levodopa
L'esposizione al plasma (AUC e CMAX) di Levodopa è significativamente più alta nelle femmine rispetto ai maschi (in media il 40% per AUC e il 30% per CMAX). Queste differenze sono spiegate principalmente dal peso corporeo. Altre letterature pubblicate hanno mostrato un effetto di genere significativo (concentrazioni più elevate nelle femmine) anche dopo la correzione del peso corporeo.
Carbidopa
Non vi è alcuna differenza di genere nella farmacocinetica di Carbidopa.
Entacapone
Non vi è alcuna differenza di genere nella farmacocinetica di entacapone.
Studi sull'interazione farmacologica
Farmaco metabolizzato da COMT
Quando è stata somministrata una singola dose di 400 mg di entacapone insieme all'isoprenalina endovenosa (isoproterenolo) ed epinefrina senza levodopa amministrata in co -co -co -co -cofano e inibitore della DOPA decarbossilasi, rispettivamente i cambiamenti massimi medi complessivi nella frequenza cardiaca durante l'infusione erano circa il 50% e l'80% rispetto al placebo per l'isoprenalina ed Epinefrina rispettivamente.
I farmaci noti per essere metabolizzati da COMT devono essere somministrati con cautela nei pazienti che ricevono entacapone indipendentemente dalla via di somministrazione [vedi Interazioni farmacologiche ].
Farmaci metabolizzati tramite CYP2C9
A causa della sua affinità con l'entacapone in vitro del CYP2C9 può potenzialmente interferire con i prodotti medicinali con metabolismo dipendente da questo isoenzima. In uno studio di interazione in volontari sani, Entacapone ha aumentato in media l'AUC di R-Warfarin del 18% e i valori INR sono aumentati in media del 13% [vedi Interazioni farmacologiche ].
Livelli ormonali
Degli ingredienti di Stalevo Levodopa è noto per deprimere la secrezione di prolattina e aumentare ormone della crescita livelli.
Studi clinici
L'efficacia dell'entacapone in aggiunta a Levodopa nel trattamento della malattia di Parkinson è stata stabilita in tre studi randomizzati a doppio cieco randomizzati a 24 settimane in pazienti con malattia di Parkinson. In 2 di questi studi (studi 1 e 2) la malattia dei pazienti stava fluttuando, cioè era caratterizzata da periodi documentati di On (periodi di funzionamento relativamente buono) e off (periodi di funzionamento relativamente scarso) nonostante la terapia di levodopa ottimale. C'è stato anche un periodo di ritiro dopo 6 mesi di trattamento. Nel terzo studio non è stato tenuto ai pazienti di aver subito fluttuazioni. Prima della parte controllata di questi studi, i pazienti erano stabilizzati su Levodopa per 2 settimane a 4 settimane.
Vi è un'esperienza limitata utilizzando l'entacapone nei pazienti che non sperimentano fluttuazioni.
Negli studi 1 e 2 pazienti sono stati randomizzati a ricevere placebo o entacapone 200 mg somministrati in concomitanza con ogni dose di carbidopa/levodopa (fino a 10 volte al giorno, ma i pazienti hanno registrato una media di 4 dosi a 6 dosi al giorno). La parte in doppio cieco di entrambi gli studi è durata 6 mesi. I pazienti hanno periodicamente registrato il tempo trascorso negli stati on e off nei diari domestici per tutta la durata della sperimentazione. In uno studio condotto nei paesi nordici, la misura di risultato primaria era il tempo medio totale trascorso nello stato di On durante un giorno registrato di 18 ore (dalle 6 a mezzanotte). Nell'altro studio la misura del risultato primario era la percentuale di tempo sveglio trascorso oltre 24 ore nello stato.
Oltre alla misura di esito primario, è stata valutata la quantità di tempo trascorso nello stato OFF e anche i pazienti sono stati valutati dalle sottoparti della scala di valutazione della malattia di Parkinson unificata (UPDRS) di una scala di valutazione multi-elemento usata frequentemente intesa a valutare la menzione (Parte I) delle attività quotidiane della vita quotidiana (Parte II) Moto (Parte III) Complicanze della terapia (Parte IV) e della malattia (Parte V e della Parte); Valutazione globale di un investigatore e del paziente sulle condizioni cliniche Una scala soggettiva a 7 punti progettata per valutare il funzionamento globale nella malattia di Parkinson; e il cambiamento nella dose giornaliera di carbidopa/levodopa.
Quale classe di droga è Strattera
Nello studio 1 171 i pazienti sono stati randomizzati in 16 centri in Finlandia Norvegia Svezia e Danimarca (Studio 1) che hanno ricevuto tutti in concomitante Levodopa Plus DOPA decarbossilasi (o Carbidopa/Levodopa o Benserazide/Levodopa). Nello studio 2 205 pazienti sono stati randomizzati in 17 centri in Nord America (Stati Uniti e Canada); Tutti i pazienti hanno ricevuto carbidopa concomitante/levodopa.
Le seguenti tabelle (Tabella 4 e Tabella 5) mostrano i risultati di questi due studi:
Tabella 4: risultati di efficacia dello studio 1
| Misura primaria dal diario domestico (da un giorno di diario di 18 ore) | |||
| Basale | Modifica dal basale al mese 6* | Value p vs. placebo | |
| Ore di tempo sveglio | |||
| Placebo | 9.2 | 0.1 | - |
| Entacapone | 9.3 | 1.5 | Meno di 0,001 |
| Durata di punta dopo la prima dose di AM (HRS) | |||
| Placebo | 2.2 | 0.0 | - |
| Entacapone | 2.1 | 0.2 | Meno di 0,05 |
| Misure secondarie dal diario domestico (da un giorno di diario di 18 ore) † | |||
| Ore di tempo libero | |||
| Placebo | 5.3 | 0.0 | - |
| Entacapone | 5.5 | -1.3 | Meno di 0,001 |
| Proporzione del tempo sveglio su ‡ (%) | |||
| Placebo | 63.8 | 0.6 | - |
| Entacapone | 62.7 | 9.3 | Meno di 0,001 |
| Levodopa Total Daily Dose (mg) | |||
| Placebo | 705 | 14 | - |
| Entacapone | 701 | -87 | Meno di 0,001 |
| Frequenza delle assunzioni quotidiane di Levodopa | |||
| Placebo | 6.1 | 0.1 | - |
| Entacapone | 6.2 | - 0.4 | Meno di 0,001 |
| Altre misure secondarie | |||
| Basale | Cambia dal basale al mese 6 | Value p vs. placebo | |
| % Globale (complessivo) di investigatore migliorato§ | |||
| Placebo | - | 28 | - |
| Entacapone | - | 56 | Meno di 0,01 |
| % Globale (complessivo) del paziente migliorato§ | |||
| Placebo | - | 22 | - |
| Entacapone | - | 39 | N.S.¶ |
| UPDRS totale | |||
| Placebo | 37.4 | -1.1 | - |
| Entacapone | 38.5 | -4.8 | Meno di 0,01 |
| Motore updrs | |||
| Placebo | 24.6 | -0.7 | - |
| Entacapone | 25.5 | -3.3 | Meno di 0,05 |
| UPDRS ADL | |||
| Placebo | 11.0 | -0.4 | - |
| Entacapone | 11.2 | -1.8 | Meno di 0,05 |
| *Significare; I valori del mese 6 rappresentano la media delle settimane 8 16 e 24 mediante misura di esito definito dal protocollo. † I valori P per le misure secondarie sono valori P nominali senza alcun adeguamento per la molteplicità. ‡ Non un endpoint per questo studio ma endpoint primario nello studio nordamericano. § con almeno una modifica di categoria all'endpoint. ¶Non significativo. |
Tabella 5: risultati di efficacia dello studio 2
| Misura primaria dal diario di casa (per un giorno di diario di 24 ore) | |||
| Basale | Modifica dal basale al mese 6* | Value p vs. placebo | |
| Percentuale del tempo sveglio | |||
| Placebo | 60.8 | 2.0 | - |
| Entacapone | 60.0 | 6.7 | Meno di 0,05 |
| Misure secondarie dal diario domestico (per un giorno di diario di 24 ore) † | |||
| Ore di tempo libero | |||
| Placebo | 6.6 | -0.3 | - |
| Entacapone | 6.8 | -1.2 | Meno di 0,01 |
| Ore di tempo sveglio | |||
| Placebo | 10.3 | 0.4 | - |
| Entacapone | 10.2 | 1.0 | N.S. ‡ |
| Levodopa Total Daily Dose (mg) | |||
| Placebo | 758 | 19 | - |
| Entacapone | 804 | -93 | Meno di 0,001 |
| Frequenza delle assunzioni quotidiane di Levodopa | |||
| Placebo | 6.0 | 0.2 | - |
| Entacapone | 6.2 | 0.0 | N.S. ‡ |
| Altre misure secondarie† | |||
| Basale | Cambia dal basale al mese 6 | Value p vs. placebo | |
| % Globale (complessivo) di investigatore migliorato§ | |||
| Placebo | - | 21 | - |
| Entacapone | - | 34 | Meno di 0,05 |
| % Globale (complessivo) del paziente migliorato§ | |||
| Placebo | - | 20 | - |
| Entacapone | - | 31 | Meno di 0,05 |
| UPDRS totale¶ | |||
| Placebo | 35.6 | 2.8 | - |
| Entacapone | 35.1 | -0.6 | Meno di 0,05 |
| Motore updrs ¶ | |||
| Placebo | 22.6 | 1.2 | - |
| Entacapone | 22.0 | -0.9 | Meno di 0,05 |
| UPDRS ADL¶ | |||
| Placebo | 11.7 | 1.1 | - |
| Entacapone | 11.9 | 0.0 | Meno di 0,05 |
| *Significare; I valori del mese 6 rappresentano la media delle settimane 8 16 e 24 mediante misura di esito definito dal protocollo. † I valori P per le misure secondarie sono valori P nominali senza alcun adeguamento per la molteplicità. ‡ Non significativo. § con almeno una modifica di categoria all'endpoint. ¶Core Cambia all'endpoint Analogamente allo studio nordico. |
Gli effetti sul tempo non differivano in base alla gravità della malattia del peso sessuale di età alla dose di levodopa al basale e al trattamento concorrente con agonisti della dopamina o selegilina.
Ritiro di entecapone
Nello studio 2 il brusco ritiro di entacapone senza alterazione della dose di carbidopa/levodopa ha comportato un significativo peggioramento delle fluttuazioni rispetto al placebo. In alcuni casi i sintomi erano leggermente peggiori rispetto al basale ma sono tornati alla gravità approssimativamente basale entro 2 settimane dopo l'aumento della dose di Levodopa in media di 80 mg. Nello studio 1 allo stesso modo è stato osservato un peggioramento significativo dei sintomi parkinsoniani dopo il ritiro di entacapone come valutato 2 settimane dopo il ritiro del farmaco. In questa fase i sintomi erano approssimativamente alla gravità basale dopo l'aumento della dose di levodopa di circa 50 mg.
Nel terzo studio controllato con placebo (studio 3) un totale di 301 pazienti sono stati randomizzati in 32 centri in Germania e Austria. In questo studio, come negli altri 2 studi, Entacapone 200 mg è stato somministrato con ogni dose di inibitore di Levodopa e DOPA decarbossilasi (fino a 10 volte al giorno) e le parti UPDRS II e III e il totale quotidiano in tempo erano le misure primarie di efficacia. I risultati per le misure primarie e per alcune misure secondarie sono presentati nella Tabella 6.
Tabella 6: risultati di efficacia dello studio 3
| Misure primarie | |||
| Basale | Cambia dal basale al mese 6 | Value p vs. placebo (LOCF) | |
| Updrsadl* | |||
| Placebo | 12.0 | 0,5 | - |
| Entacapone | 12.4 | -0.4 | Meno di 0,05 |
| Motore updrs* | |||
| Placebo | 24.1 | 0.1 | - |
| Entacapone | 24.9 | -2.5 | Meno di 0,05 |
| Ore di tempo sveglio (Home Diary)† | |||
| Placebo | 10.1 | 0,5 | - |
| Entacapone | 10.2 | 1.1 | N.S. ‡ |
| Misure secondarie§ | |||
| Basale | Cambia dal basale al mese 6 | Value p vs. placebo | |
| UPDRS totale * | |||
| Placebo | 37.7 | 0.6 | - |
| Entacapone | 39.0 | -3.4 | Meno di 0,05 |
| Percentuale del tempo sveglio (Home Diary) ** | |||
| Placebo | 59.8 | 3.5 | - |
| Entacapone | 62.0 | 6.5 | N.S. ‡ |
| Ore di tempo libero (Home Diary) | |||
| Placebo | 6.8 | -0.6 | - |
| Entacapone | 6.3 | -1.2 | 0.07 |
| Levodopa Total Daily Dose (mg)* | |||
| Placebo | 572 | 4 | - |
| Entacapone | 566 | -35 | N.S. |
| Frequenza dell'assunzione quotidiana di Levodopa* | |||
| Placebo | 5.6 | 0.2 | - |
| Entacapone | 5.4 | 0.0 | Meno di 0,01 |
| % (Complessiva) % migliorato¶ | |||
| Placebo | - | 34 | - |
| Entacapone | - | 38 | N.S. ‡ |
| *Popolazione totale; CAMBIAMENTO PUNTEGGI A Endpoint. † Popolazione fluttuante con 5 dosi a 10 dosi; CAMBIAMENTO PUNTEGGI A Endpoint. ‡ Non significativo. I valori §P per le misure secondarie sono valori P nominali senza alcun adeguamento per la molteplicità. ¶Totale popolazione; Almeno una modifica di una categoria all'endpoint. |
Informazioni sul paziente per Stalevo
Addormentarsi durante le attività di vita quotidiana e sonnolenza
Consiglia ai pazienti il potenziale per gli effetti sedativi associati a Stalevo, tra cui la sonnolenza e la possibilità di addormentarsi mentre si è impegnati in attività della vita quotidiana. Poiché la sonnolenza può essere una frequente reazione avversa con conseguenze potenzialmente gravi, i pazienti non dovrebbero guidare un veicolo a motore azionare macchinari pesanti o impegnarsi in altre attività potenzialmente pericolose fino a quando non hanno acquisito un'esperienza sufficiente con Stalevo per determinare se colpisce o meno le loro prestazioni mentali e/o motorie. Avvertimenti e precauzioni ]. Advise patients that if increased somnolence or episodes of falling asleep during activities of daily living (e.g. conversations eating driving a motor vehicle etc.) are experienced at any time during treatment they should not drive or participate in potentially dangerous activities until they have contacted their physician.
Consiglia ai pazienti di parlare con il loro prescrittore sanitario prima di assumere farmaci sedati alcolici o altri depressivi del SNC (ad esempio antidepressivi antipsicotici benzodiazepine ecc.) A causa dei possibili effetti additivi in combinazione con lo stalevo.
Ipotensione Orthostatic Ipotensione And Syncope
Consiglia ai pazienti che possono sviluppare ipotensione posturale (o ortostatica) sintomatica (o asintomatica) o ipotensione non ortatica durante l'assunzione di Stalevo. Ipotensione/ipotensione ortostatica può verificarsi più frequentemente durante la terapia iniziale. I pazienti non devono salire rapidamente dopo essersi seduti o sdraiati soprattutto se lo hanno fatto per periodi prolungati e in particolare all'inizio del trattamento con Stalevo.
Consiglia ai pazienti il potenziale per la sincope nei pazienti che utilizzano agonisti della dopamina. Per questo motivo informare i pazienti sulla possibilità di sincope durante l'assunzione di stalevo [vedi Avvertimenti e precauzioni ].
Discinesias
Informare i pazienti che Stalevo può causare e/o esacerbare discinesie preesistenti [vedi Avvertimenti e precauzioni ].
Allucinazioni e/o comportamento psicotico
Informare i pazienti che possono verificarsi allucinazioni e altri comportamenti psicotici mentre si prende lo stalevo [vedi Avvertimenti e precauzioni ].
Controllo degli impulsi e/o comportamenti compulsivi
Consiglia ai pazienti che possono sperimentare il controllo degli impulsi e/o comportamenti compulsivi durante l'assunzione di uno o più farmaci utilizzati per il trattamento della malattia di Parkinson, incluso Stalevo. Chiedere ai pazienti lo sviluppo di impulsi di gioco nuovi o maggiori impulsi di impulsi sessuali per la spesa incontrollata o altri impulsi intensi mentre vengono trattati con Stalevo. Consiglia ai pazienti di informare il proprio medico o un operatore sanitario se sperimentano impulsi di gioco nuovi o maggiori aumenti di impulsi sessuali o altri impulsi intensi durante l'assunzione di Stalevo. I medici dovrebbero prendere in considerazione la riduzione della dose o l'interruzione del farmaco se un paziente sviluppa tali impulsi durante l'assunzione di stalevo [vedi Avvertimenti e precauzioni ].
Iperpyrexia e confusione emergente di ritiro
Consiglia ai pazienti che possono sviluppare febbre e confusione come parte di una sindrome che ricorda NMS e possibilmente con altre caratteristiche cliniche (ad esempio iper o ipotensione della disfunzione autonoma di rigidità muscolare ecc.). Questa sindrome da febbre e confusione può verificarsi in particolare con riduzioni della dose o ritiro di Stalevo, ma può anche svilupparsi dopo l'inizio del trattamento. Consiglia ai pazienti di contattare il proprio operatore sanitario se desiderano interrompere o ridurre la dose di stalevo e di contattare un operatore sanitario se sviluppano febbre e confusione [vedi Avvertimenti e precauzioni ].
Diarrea And Colitis
Informare i pazienti che la diarrea può verificarsi con Stalevo e può avere un esordio ritardato. A volte la diarrea prolungata può essere causata dalla colite (infiammazione dell'intestino crasso). I pazienti con diarrea devono bere liquidi per mantenere un'adeguata idratazione e monitorare la perdita di peso. Se la diarrea associata allo stalevo è prolungato di interrompere il farmaco, dovrebbe portare alla risoluzione. Se la diarrea continua dopo aver interrotto lo stalevo è necessario ulteriori indagini diagnostiche. In alcuni casi la diarrea può essere associata alla colite [vedi Avvertimenti e precauzioni ].
Rabdomiolisi
Consiglia ai pazienti che possono sviluppare rabdomiolisi e mialgia se sperimentano un'attività motoria prolungata compresa la discinesia. Questo evento può anche essere associato alla febbre e alla confusione [vedi Avvertimenti e precauzioni ].
Nausea And Vomito
Informare i pazienti che lo stalevo può causare nausea e vomito può verificarsi più frequentemente durante la terapia iniziale e può richiedere un aggiustamento della dose.
Istruzioni per l'uso
Istruire i pazienti a prendere Stalevo solo come prescritto. Istruisci i pazienti a prendere solo una singola compressa di stalevo ad ogni intervallo di dosaggio. Istruisci i pazienti a non prendere più compresse o porzioni aggiuntive di compresse per ottenere una dose più elevata di levodopa. Consiglia ai pazienti di non dividere la cotta o masticare lo stalevo.
Informare il paziente che Stalevo è una formulazione di carbidopa/levodopa combinata con entacapone progettato per iniziare il rilascio di ingredienti entro 30 minuti dall'ingestione. È importante che lo stalevo sia preso a intervalli regolari secondo il programma delineato dal medico. Attenzione al paziente di non cambiare il regime di dosaggio prescritto e di non aggiungere ulteriori farmaci antiparkinsoniani tra cui altri preparativi carbidopa/levodopa senza prima consultare il medico.
Consiglio ai pazienti che gli episodi fuori (usura dell'effetto farmaco) si verificano alla fine dell'intervallo di dosaggio, ma possono verificarsi imprevedibili episodi in qualsiasi momento. Consiglia al paziente di avvisare un operatore sanitario per possibili aggiustamenti del trattamento se tale risposta pone un problema alla vita quotidiana del paziente.
Consiglia ai pazienti che la colorazione scura (marrone rosso o nero) può apparire nelle urine o sul sudore della saliva dopo aver preso Stalevo. Sebbene il colore sembri essere clinicamente insignificanti gli indumenti possono essere scoloriti.
Consiglia ai pazienti che un cambiamento nella dieta per gli alimenti ricchi di proteine può ritardare l'assorbimento della levodopa. L'acidità eccessiva ritarda anche lo svuotamento dello stomaco ritardando così l'assorbimento di levodopa. I sali di ferro (come nelle compresse multi-vitaminici) possono anche ridurre l'efficacia di Stalevo.
Gravidanza
Istruire i pazienti a avvisare il proprio operatore sanitario se rimangono incinta o intendono rimanere incinta durante la terapia [vedi Utilizzare in popolazioni specifiche ].
Lattazione
Istruire i pazienti a avvisare il proprio operatore sanitario se intendono allattare o stanno allattando un bambino [vedi Utilizzare in popolazioni specifiche ].
