Le Informazioni Presenti Sul Sito Non Costituiscono Consulenza Medica. Non Vendiamo Nulla. L'Accuratezza Della Traduzione Non È Garantita. Disclaimer
Anticonvulsiranti, altroFintepla
Riepilogo della droga
Cos'è Fintepla?
Fintepla (fenfluramina) è un anticonvulsivante Utilizzato per trattare le convulsioni associate alla sindrome di Dravet in pazienti di età pari o superiore a 2 anni.
Quali sono gli effetti collaterali della fintepla?
Fintepla
- orticaria
- Difficoltà a respirare
- gonfiore della lingua o della gola
- Mood o comportamento cambia
- ansia
- attacchi di panico
- difficoltà a dormire
- impulsività
- agitazione
- ostilità
- aggressioni
- irrequietezza
- iperattività (mentalmente o fisicamente)
- aumento della depressione
- Pensieri di autolesionismo
- dolore al petto
- battiti cardiaci martellanti
- svolazzando nel petto
- fiato corto
- pelle di colore blu o labbra
- gonfiore alle gambe inferiori
- stanchezza insolita
- debolezza
- Accendino
- perdita di appetito
- perdita di peso
- peggioramento delle convulsioni
- visione sfocata
- Visione del tunnel
- Dolore agli occhi o arrossamento
- vedere aloni intorno alle luci
- nausea
- vomito
- grave mal di testa
- visione sfocata
- martellando nel collo o nelle orecchie
- nascosto
- febbre
- sudorazione
- allucinazioni
- rabbrividire
- frequenza cardiaca veloce
- rigidità muscolare
- contrazione
- crescita rallentata (nei bambini)
- perdita di coordinamento e
- diarrea
Ottieni subito assistenza medica se hai uno qualsiasi dei sintomi sopra elencati.
Gli effetti collaterali della fintepla includono:
- diminuzione dell'appetito
- sonnolenza
- sedazione
- letargia
- diarrea
- stipsi
- Ecocardiogramma anormale
- fatica
- Sentirsi male (malessere)
- debolezza
- Problemi con la coordinazione muscolare
- disturbo dell'equilibrio
- disturbo dell'andatura
- aumento della pressione sanguigna
- sbavando/salivazione in eccesso
- febbre
- infezione del tratto respiratorio superiore
- vomito
- perdita di peso
- cade e
- stato epilepticus
Cerca cure mediche o chiama il 911 contemporaneamente se hai i seguenti gravi effetti collaterali:
- Sintomi di occhiali gravi come la perdita di visione improvvisa del tunnel della visione sfocata Dolore alla visione o gonfiore o vedere aloni attorno alle luci;
- Sintomi cardiaci gravi come battiti cardiaci irregolari o martellanti veloci; svolazzando nel petto; fiato corto; e improvviso vertigini giuria o svenuta;
- Grave mal di testa confusione Il braccio del linguaggio bloccato o la debolezza delle gambe problemi perdite perdita di coordinamento sentendoti instabili muscoli molto rigidi ad alta febbre abbondante sudorazione o tremori.
Questo documento non contiene tutti i possibili effetti collaterali e altri possono verificarsi. Verificare con il tuo medico ulteriori informazioni sugli effetti collaterali.
Dosaggio per fintepla
Il dosaggio iniziale di avvio e manutenzione di Fintepla è di 0,1 mg/kg due volte al giorno, il che può essere aumentato settimanalmente in base all'efficacia e alla tollerabilità.
Fintepla nei bambini
La sicurezza e l'efficacia della fintepla per il trattamento delle convulsioni associate alla sindrome di Dravet sono state stabilite in pazienti di età pari o superiore a 2 anni. Non sono state stabilite sicurezza ed efficacia della fintepla in pazienti di età inferiore ai 2 anni.
Le distonie e altri sintomi extrapiramidali associati alla metoclopramide sono più comuni nei pazienti pediatrici che negli adulti. Inoltre, i neonati hanno ridotto livelli di NADH-citocromo B5 reduttasi rendendoli più suscettibili alla metemoglobinemia una possibile reazione avversa dell'uso di metoclopramide nei neonati.
Quali sostanze o integratori di farmaci interagiscono con Fintepla?
Fintepla può interagire con altri medicinali come:
- rifampin
- Stilmopentol Plus Clobazam
- ciproheptadina
- potente 5-HT1A 5- HT1D 5-HT2A o 5-HT2C serotonina antagonisti del recettore e
- Farmaci da banco o integratori a base di droghe che aumentano la serotonina come inibitori selettivi della reuptake della serotonina (SSRIS) Serotonina-Norepinefrina Inibitori (SNRI) Antidepressivi triciclici Inibitori della monoamina ossidasi
Dì al medico tutti i farmaci e gli integratori che usi.
Fintepla durante la gravidanza e l'allattamento
Di 'al medico se sei incinta o hai intenzione di rimanere incinta prima di usare Fintepla; Non è noto come influirebbe su un feto. Esiste un registro di esposizione alla gravidanza che monitora gli esiti di gravidanza nelle donne esposte a farmaci antiepilettici (DAE) come la fintepla durante la gravidanza. Non è noto se Fintepla passi nel latte materno. Consulta il medico prima dell'allattamento al seno.
Ulteriori informazioni
Il nostro centro farmaceutico orale di fintepla (fenfluramina) civiche fornisce una visione completa delle informazioni disponibili sui farmaci sui potenziali effetti collaterali durante l'assunzione di questo farmaco.
Questo non è un elenco completo di effetti collaterali e altri possono verificarsi. Chiama il medico per consigli medici sugli effetti collaterali. È possibile segnalare gli effetti collaterali alla FDA al numero 1-800-FDA-1088.
Informazioni sui farmaci FDA
- Descrizione del farmaco
- Indicazioni
- Effetti collaterali
- Interazioni farmacologiche
- Avvertimenti
- Overdose
- Farmacologia clinica
- Guida ai farmaci
AVVERTIMENTO
Malarità della cardiopatia valvolare e ipertensione arteriosa polmonare
Esiste un'associazione tra farmaci serotoninergici con attività agonista del recettore 5-HT2B tra cui la fenfluramina (ingrediente attivo in fintepla) e la cardiopatia valvolare e l'ipertensione arteriosa polmonare [vedi AVVERTIMENTOS AND PRECAUTIONS ].
Le valutazioni dell'ecocardiogramma sono richieste prima durante e dopo il trattamento con Fintepla. I benefici rispetto ai rischi di avvio o continuo fintepla devono essere considerati in base ai risultati dell'ecocardiogramma [vedi Dosaggio e amministrazione E AVVERTIMENTOS AND PRECAUTIONS ].
A causa dei rischi della cardiopatia valvolare e dell'ipertensione arteriosa polmonare Fintepla è disponibile solo attraverso un programma limitato nell'ambito di una strategia di valutazione e mitigazione del rischio (REMS) chiamata Fintepla REMS [vedi AVVERTIMENTOS AND PRECAUTIONS ].
Descrizione per fintepla
La soluzione orale di fintepla contiene 2,2 mg/ml di fenfluramina equivalente a 2,5 mg/ml di sale di cloridrato.
Il principio attivo fenfluramina cloridrato è designato chimicamente come N-etil-α-metil-3- (trifluorometil) fenetilammina cloridrato.
La formula strutturale è:
| |
La fenfluramina cloridrato è un solido cristallino da bianco a bianco sporco. La PKA di fenfluramina è 10.2.
Fintepla è una soluzione chiara incolore pH 5.
Fintepla contiene i seguenti ingredienti inattivi: sapore citrato di acido citrico etilparaben idrossietilcellulosio metilparaben citrato di potassio sucralosio e acqua.
Fintepla non contiene ingredienti a base di grano contenente glutine (orzo di grano o segale).
Usi per Fintepla
Fintepla è indicato per il trattamento delle convulsioni associate alla sindrome di Dravet (DS) e alla sindrome di Lennox-Gastaut (LGS) in pazienti di età pari o superiore a 2 anni.
Dosaggio per fintepla
Valutazioni prima di iniziare la fintepla
Prima di iniziare il trattamento con fintepla, ottenere una valutazione dell'ecocardiogramma per valutare la malattia cardiaca valvolare e l'ipertensione arteriosa polmonare [vedi Valutazioni durante e dopo la somministrazione di fintepla E AVVERTIMENTOS AND PRECAUTIONS ].
Informazioni sul dosaggio
La fintepla deve essere somministrata per via orale e può essere presa con o senza cibo.
Sindrome di Dravet
- Il dosaggio iniziale di avvio e mantenimento per i pazienti con sindrome di Dravet è di 0,1 mg/kg due volte al giorno, il che può essere aumentato settimanalmente in base all'efficacia e alla tollerabilità. La tabella 1 fornisce il programma di titolazione consigliato se necessario.
- I pazienti con sindrome di Dravet non su patitudine concomitante che tollerano la fintepla a 0,1 mg/kg due volte al giorno e richiedono un'ulteriore riduzione delle convulsioni possono beneficiare di un aumento del dosaggio fino a un dosaggio di mantenimento massimo raccomandato di 0,35 mg/kg due volte al giorno (massimo il dosaggio giornaliero di 26 mg).
- I pazienti con sindrome di Dravet che assumono commeditore concomitante più clobazam che tollerano la fintepla a 0,1 mg/kg/kg due volte al giorno e richiedono un'ulteriore riduzione delle convulsioni possono beneficiare di un aumento del dosaggio fino a un dosaggio di mantenimento massimo raccomandato di 0,2 mg/kg due volte al giorno (massimo dosaggio giornaliero di 17 mg) [vedi Interazioni farmacologiche ].
Sindrome di Lennox-Gastaut
- Il dosaggio iniziale iniziale per i pazienti con sindrome di Lennox-Gastaut è di 0,1 mg/kg due volte al giorno, il che dovrebbe essere aumentato settimanalmente in base alla tollerabilità. La tabella 1 fornisce il programma di titolazione consigliato.
- I pazienti con sindrome di Lennox-Gastaut non in concomitante stirmipolo che tollerano la fintepla devono essere titolati al dosaggio di manutenzione raccomandato di 0,35 mg/kg due volte al giorno (dosaggio massimo giornaliero di 26 mg).
- I pazienti con sindrome di Lennox-Gastaut che assumono il patipololo concomitante più clobazam che tollerano la fintepla devono essere titolati al dosaggio di manutenzione raccomandato di 0,2 mg/kg due volte al giorno (dosaggio massimo giornaliero di 17 mg) [vedi Interazioni farmacologiche ].
Tabella 1: programma di titolazione consigliato da fintepla*
| Senza comitatolo concomitante* | Con concomitante StilEpentol Plus Clobazam | |||
| Dosaggio a base di peso | Dosaggio totale massimo giornaliero ± | Dosaggio a base di peso | Dosaggio massimo ± totale giornaliero | |
| Dosaggio iniziale | 0,1 mg/kg due volte al giorno | 26 mg | 0,1 mg/kg due volte al giorno | 17 mg |
| Giorno 7 | 0,2 mg/kg due volte al giorno | 26 mg | 0,15 mg/kg due volte al giorno | 17 mg |
| Giorno 14 ** | 0,35 mg/kg due volte al giorno | 26 mg | 0,2 mg/kg due volte al giorno | 17 mg |
| * Per i pazienti non in concomitante stivallo in cui è giustificata una titolazione più rapida, la dose può essere aumentata ogni 4 giorni. Per i pazienti con dosaggio della sindrome di Dravet può essere aumentato in base alla risposta clinica al dosaggio massimo raccomandato, se necessario. ** Per i pazienti con dosaggio di sindrome di Lennox-Gastaut deve essere aumentato come tollerato al dosaggio di mantenimento raccomandato (cioè giorno 14). ± per il massimo dosaggio con uso concomitante di forti inibitori del CYP1A2 o del CYP2D6 in pazienti con grave compromissione renale o in pazienti con compromissione epatica. Modifica del dosaggio per i pazienti con uso concomitante di forti modifiche al dosaggio di dosaggio (DS e LG) di dosaggio (DS e LG) di dosaggio (DS e LG) (DS e LG) di modifiche al dosaggio renale (DS e LG) di dosaggi (DS) (DS e LG) di dosaggi (LG) di dosaggio (LG) di dosaggio (LG) e LG) di modifiche del dosaggio renale (LG) di pazienti con gravi (LG) sono presenti modifiche che hanno commesso modifiche al dosaggio di dosaggio renali (DS e LG) di pazienti con riduzione errazione renale (LGS) lievi e gravi gravi) per i pazienti con i pazienti leggeri e gravi epatici gravi) (LGS). |
Modifiche al dosaggio per i pazienti con uso concomitante di forti inibitori del CYP1A2 o del CYP2D6 (DS e LGS)
Per i pazienti con un uso concomitante di fintepla con un forte inibitore del CYP1A2 o del CYP2D6, si raccomanda un dosaggio totale massimo giornaliero di 20 mg senza stirmipolo concomitante e 17 mg con ampentolo concomitante più clobazam [vedi Interazioni farmacologiche ].
Modifiche al dosaggio per i pazienti con grave compromissione renale (DS e LG)
Per i pazienti con grave compromissione renale (velocità di filtrazione glomerulare stimata (EGFR) da 15 a 29 ml/min/1,73 m 2 ) Un dosaggio totale massimo giornaliero di 20 mg senza concomitante amipol e 17 mg con concomitante stirice più clobazam si raccomanda [vedi Utilizzare in popolazioni specifiche ].
Modifiche al dosaggio per i pazienti con lieve compromissione epatica moderata e grave (DS e LG)
Vedere la Tabella 2 per gli aggiustamenti del dosaggio e le raccomandazioni per i pazienti con compromissione epatica [vedi Utilizzare in popolazioni specifiche ].
Tabella 2: Modifica e raccomandazioni del dosaggio di Fintepla per i pazienti con problemi di compromissione
| Classificazione di compromissione epatica | Senza comitatolo concomitante* | Con concomitante StilEpentol Plus Clobazam |
| Dosaggio massimo totale giornaliero | Dosaggio massimo totale giornaliero | |
| Blando (Child-Pugh a) | 20 mg | 13 mg* |
| Moderare (Child-Pugh B) | 20 mg | Utilizzare non consigliato |
| Acuto (Child-Pugh C) | 17 mg | Utilizzare non consigliato |
| * titolare come consigliato [vedi Informazioni sul dosaggio |
Valutazioni durante e dopo la somministrazione di fintepla
Per valutare la malattia valvolare e l'ipertensione arteriosa polmonare ottenere una valutazione dell'ecocardiogramma ogni 6 mesi durante il trattamento con fintepla e 3-6 mesi dopo la dose finale di fintepla [vedi AVVERTIMENTOS AND PRECAUTIONS ].
Istruzioni di amministrazione
Un dispositivo di misurazione calibrato (una siringa orale da 3 ml o 6 ml) sarà fornito dalla farmacia e si consiglia di misurare e somministrare accuratamente la dose prescritta [vedi Come fornito ]. A household teaspoon or tablespoon is not an adequate measuring device E should not be used.
Scartare qualsiasi soluzione orale di fintepla inutilizzata rimanente dopo 3 mesi di apertura prima della bottiglia o lo scarto dopo la data sulla bottiglia a seconda di quale sia esso.
Fintepla è compatibile con tubi di alimentazione gastrici e nasogastrici disponibili in commercio.
Interruzione di fintepla
Quando si interrompe la fintapla, la dose dovrebbe essere diminuita gradualmente. Come per tutti i farmaci antiepilettici bruschi l'interruzione dovrebbe essere evitato quando possibile per ridurre al minimo il rischio di aumento della frequenza delle crisi e dello stato epilettico [vedi AVVERTIMENTOS AND PRECAUTIONS ].
Come fornito
Forme di dosaggio e punti di forza
Soluzione orale : 2,2 mg/ml di fenfluramina come liquido aromatizzato in ciliegia chiaro.
Fintepla La soluzione orale è un liquido aromatizzato in ciliegia chiaro contenente 2,2 mg/ml di fenfluramina ed è fornito in una bottiglia di plastica bianca con una chiusura resistente ai bambini come segue:
- Cartone contenente una bottiglia da 360 ml ( Ndc 43376-322-36)
- Cartone contenente una bottiglia da 30 ml ( Ndc 43376-322-30)
Prima di distribuire il farmacista inserirà un adattatore per bottiglia con la bottiglia di erogazione. La farmacia fornirà siringhe di dosaggio orale calibrate da 3 ml o 6 ml.
Archiviazione e maneggevolezza
Conservare la fintepla a temperatura ambiente da 20 ° C a 25 ° C (da 68 ° F a 77 ° F); Le escursioni sono consentite da 15 ° C a 30 ° C (da 59 ° F a 86 ° F) [vedi temperatura ambiente controllata da USP].
Non refrigerare o congelare. Conservare insieme la bottiglia e la siringa.
Scartare qualsiasi porzione inutilizzata 3 mesi dopo l'apertura della bottiglia o lo scarto dopo la data sulla bottiglia a seconda di quale sia prima.
Riduzione percentuale dal basale nella frequenza convulsiva a caduta
Proporzione di pazienti (%)
Prodotto per: UCB Inc. Smyrna GA 30080. Revisionato: aprile 2025.
Effetti collaterali for Fintepla
Le seguenti reazioni avverse clinicamente significative sono descritte altrove nell'etichettatura:
- Malattia valvolare e ipertensione arteriosa polmonare [vedi AVVERTIMENTOS AND PRECAUTIONS ]
- Diminuzione dell'appetito e una riduzione del peso [vedi AVVERTIMENTOS AND PRECAUTIONS ]
- Somnolence Sedation and Letargy [vedi AVVERTIMENTOS AND PRECAUTIONS ]
- Comportamento suicidario e ideazione [vedi AVVERTIMENTOS AND PRECAUTIONS ]
- Ritiro di farmaci antiepilettici [vedi AVVERTIMENTOS AND PRECAUTIONS ]
- Sindrome di Seroton [vedi AVVERTIMENTOS AND PRECAUTIONS ]
- Aumento della pressione sanguigna [vedi AVVERTIMENTOS AND PRECAUTIONS ]
- Glaucoma [vedi AVVERTIMENTOS AND PRECAUTIONS ]
Esperienza di studi clinici
Poiché gli studi clinici sono condotti in condizioni di reazione avverse ampiamente variabili osservate negli studi clinici di un farmaco non possono essere paragonati direttamente ai tassi negli studi clinici di un altro farmaco e potrebbero non riflettere i tassi osservati nella pratica.
In studi controllati e non controllati in pazienti con sindrome di Dravet (DS) 341 pazienti sono stati trattati con Fintepla, tra cui 312 pazienti trattati per più di 6 mesi 284 pazienti trattati per più di 1 anno e 138 pazienti trattati per più di 2 anni.
In studi controllati e non controllati in pazienti con sindrome di Lennox-Gastaut (LGS) 262 pazienti sono stati trattati con Fintepla tra cui 219 pazienti trattati per più di 6 mesi 172 pazienti trattati per più di 1 anno e 127 pazienti trattati per più di 2 anni.
Sindrome di Dravet
Negli studi controllati con placebo su pazienti con DS che assumono standard di cure concomitanti di AEDS 122 pazienti sono stati trattati con fintepla e 84 pazienti hanno ricevuto placebo [vedi Studi clinici ]. The duration of treatment in these trials was 16 weeks (Studio 1) or 17 weeks (Studio 2).
Nello Studio 1 e Studio 2 L'età media era di 9 anni (range da 2 a 19 anni) e circa il 46% dei pazienti era femmina e il 74% era bianco. Tutti i pazienti stavano ricevendo almeno un altro DAE.
Nello studio 1 e dello studio 2 i tassi di interruzione a seguito di qualsiasi reazione avversa sono stati il 13% 0% e il 7% per i pazienti trattati con Fintepla 0,7 mg/kg/giorno 0,2 mg/kg/giorno e 0,4 mg/kg/giorno in combinazione rispettivamente con Stiripentol rispetto al 6% per i pazienti sul placebo. La reazione avversa più frequente che ha portato alla sospensione nei pazienti trattati con qualsiasi dose di fintepla è stata la sonnolenza (3%).
Le reazioni avverse più comuni che si sono verificate nei pazienti trattati con fintepla (incidenza di almeno il 10% e maggiore del placebo) sono state ridotte l'appetito; Somnolence Sedation Letargy; diarrea; stipsi; ecocardiogramma anormale; fatica malessere astenia; Disturbo del disturbo del bilanciamento dell'atassia Disturbi dell'andatura; La pressione sanguigna è aumentata; sbavare l'ipersecrezione salivare; Pyrexia; Infezione del tratto respiratorio superiore; vomito; riduzione del peso; autunno; stato epilepticus.
La tabella 4 elenca le reazioni avverse che sono state riportate nel 5% o più dei pazienti trattati con Fintepla e ad una velocità maggiore di quelle sul placebo durante le fasi di titolazione e mantenimento dello studio 1 e dello studio 2.
Tabella 4: reazioni avverse nel 5% o più dei pazienti trattati con fintepla e grave rispetto al placebo negli studi controllati con placebo per la sindrome di Dravet (Studio 1 e 2)
| Reazione avversa | Fintepla Dose Group | Gruppo placebo combinato (2) | ||
| Studio 1 | Studio 2 | |||
| 0,2 mg/kg/giorno | 0,7 mg/kg/giorno | 0,4 mg/kg/giorno (1) | ||
| N = 39 % | N = 40 % | N = 43 % | N = 84 % | |
| Diminuzione dell'appetito | 23 | 38 | 49 | 8 |
| Somnolence Sedation Letargy | 26 | 25 | 23 | 11 |
| Ecocardiogramma anormale (3) | 18 | 23 | 9 | 6 |
| Diarrea | 31 | 15 | 23 | 6 |
| Stipsi | 3 | 10 | 7 | 0 |
| Fatica malessere astenia | 15 | 10 | 30 | 5 |
| Disturbo del disturbo dell'equilibrio di atassia | 10 | 10 | 7 | 1 |
| Comportamento anormale | 0 | 8 | 9 | 0 |
| La pressione sanguigna è aumentata | 13 | 8 | 0 | 5 |
| Sbavare l'ipersecrezione salivare | 13 | 8 | 2 | 0 |
| Ipotonia | 0 | 8 | 0 | 0 |
| Eruzione cutanea | 8 | 8 | 5 | 4 |
| La prolattina del sangue è aumentata | 0 | 5 | 0 | 0 |
| Brividi | 0 | 5 | 2 | 0 |
| Diminuzione dell'attività | 0 | 5 | 0 | 1 |
| Disidratazione | 0 | 5 | 0 | 0 |
| Insonnia | 0 | 5 | 5 | 2 |
| Pyrexia | 15 | 5 | 21 | 14 |
| Stereotipi | 0 | 5 | 0 | 0 |
| Infezione del tratto respiratorio superiore | 21 | 5 | 7 | 10 |
| Vomito | 10 | 5 | 5 | 8 |
| Il peso è diminuito | 13 | 5 | 7 | 1 |
| Groppa | 5 | 3 | 0 | 1 |
| Infezione all'orecchio | 8 | 3 | 9 | 5 |
| Gastroenterite | 8 | 3 | 2 | 0 |
| Aumento della frequenza cardiaca | 5 | 3 | 0 | 2 |
| Irritabilità | 0 | 3 | 9 | 2 |
| Rinite | 8 | 3 | 7 | 2 |
| Tremore | 3 | 3 | 9 | 0 |
| Incontinenza urinaria | 5 | 3 | 0 | 0 |
| Diminuzione della glicemia | 0 | 0 | 9 | 1 |
| Bronchite | 3 | 0 | 9 | 1 |
| Contusione | 5 | 0 | 0 | 0 |
| Eczema | 0 | 0 | 5 | 0 |
| Enuresi | 5 | 0 | 0 | 0 |
| Autunno | 10 | 0 | 0 | 4 |
| Mal di testa | 8 | 0 | 0 | 2 |
| Laringite | 0 | 0 | 5 | 0 |
| Negativismo | 5 | 0 | 0 | 0 |
| Stato epilepticus | 3 | 0 | 12 | 2 |
| Infezione del tratto urinario | 5 | 0 | 5 | 0 |
| Infezione virale | 0 | 0 | 5 | 1 |
| (1) 0,4 mg/kg/giorno was not an intermediate dose. Patients on the 0,4 mg/kg/giorno dose were also taking concomitant Stilmopentol Plus Clobazam which increases exposure of Fintepla. (2) I pazienti nei gruppi di placebo degli studi 1 e 2 sono stati raggruppati. (3) Consisteva in tracce e lieve rigurgito mitrale e rintraccia aortica che sono considerati fisiologici |
Sindrome di Lennox-Gastaut
Nello studio controllato con placebo su pazienti con LGS che assumono standard di cure concomitanti (studio 3) 176 pazienti sono stati trattati con fintepla e 87 pazienti hanno ricevuto placebo [vedi Studi clinici ]. The duration of treatment in this trial was 16 weeks. The mean age was 13.7 years (range 2 to 35 years) E 29% of patients were at least 18 years of age 45% of patients were female E 79% were White. All patients were receiving at least one other AED.
I tassi di interruzione a seguito di qualsiasi reazione avversa sono stati il 6% e il 5% per i pazienti trattati con Fintepla rispettivamente di 0,7 mg/kg/giorno e 0,2 mg/kg/giorno rispetto all'1% per i pazienti sul placebo. Le reazioni avverse più frequenti che hanno portato alla sospensione nei pazienti trattati con qualsiasi dose di fintepla sono state convulsive (2%) e sonnolenza (2%).
Le reazioni avverse comuni che si sono verificate nei pazienti trattati con fintepla (incidenza di almeno il 10% e maggiore del placebo) erano diarrea; diminuzione dell'appetito; fatica; sonnolenza; vomito.
La tabella 5 elenca le reazioni avverse che sono state riportate nel 5% o più dei pazienti trattati con Fintepla e ad una velocità maggiore di quelle sul placebo durante le fasi di titolazione e mantenimento dello studio 3.
Tabella 5: reazioni avverse nel 5% o più dei pazienti trattati con fintepla e maggiore del placebo nello studio controllato con placebo per la sindrome di Lennox Gastaut (Studio 3)
| Reazione avversa | Fintepla Dose Group | ||
| Studio 3 | Gruppo placebo | ||
| 0,2 mg/kg/giorno | 0,7 mg/kg/giorno | ||
| N = 89 % | N = 87 % | N = 87 % | |
| Diminuzione dell'appetito | 20 | 36 | 12 |
| Fatica malessere astenia | 14 | 24 | 16 |
| Somnolence Sedation Letargy | 12 | 22 | 16 |
| Diarrea | 11 | 13 | 5 |
| Stipsi | 6 | 9 | 6 |
| Vomito | 14 | 8 | 6 |
| Il peso è diminuito | 2 | 8 | 2 |
| Infezione del tratto respiratorio superiore | 8 | 7 | 3 |
| Confisca | 9 | 5 | 7 |
| Irritabilità | 8 | 3 | 6 |
Valutazioni della sicurezza ecocardiografica della malattia cardiaca valvolare e dell'ipertensione arteriosa polmonare
Le malattie della cardiopatia valvolare e l'ipertensione arteriosa polmonare sono state valutate negli studi di estensione del placebocontrollati e di etichette aperte attraverso l'ecocardiografia per una durata fino a 3 anni per 341 pazienti e 263 pazienti LGS [vedi AVVERTIMENTOS AND PRECAUTIONS ]. Screening for valvular heart disease assessed for mild or greater aortic regurgitation or moderate or greater mitral regurgitation E assessed for additional characteristics of VHD (e.g. valve thickening or restrictive valve motion).
In questi studi clinici due pazienti con LGS hanno mostrato un lieve rigurgito aortico (AR) ma nessuno dei due pazienti aveva segni cardiaci o sintomi o evidenza di cambiamenti strutturali valvolari.
Nessuno dei due pazienti aveva VHD. I tassi di AR lieve sono coerenti con quelli osservati nel periodo di screening prima del trattamento (3 pazienti in LGS e 1 paziente negli studi clinici DS).
Esperienza post -marketing
Le seguenti reazioni avverse sono state identificate durante l'uso post -approvazione di Fintepla. Poiché queste reazioni sono riportate volontariamente da una popolazione di dimensioni incerte, non è sempre possibile stimare in modo affidabile la loro frequenza o stabilire una relazione causale con l'esposizione ai farmaci.
Disturbi psichiatrici : aggressività
Interazioni farmacologiche for Fintepla
Effetto di altri farmaci sulla fintepla
Stilmopentol Plus Clobazam
La co -somministrazione di fintepla con stirmipentol più clobazam con o senza valproato aumenta Farmacologia clinica ]. If Fintepla is coadministered with Stilmopentol Plus Clobazam the maximum daily dosage of Fintepla is 0,2 mg/kg due volte al giorno (maximum daily dosage of 17 mg) [see Dosaggio e amministrazione ].
Forti induttori CYP1A2 CYP2B6 o CYP3A
La somministrazione di co -induttore di recinzione con forti induttori CYP1A2 CYP2B6 o CYP3A diminuirà le concentrazioni plasmatiche di fenfluramina che possono ridurre l'efficacia di Fintepla [vedi Farmacologia clinica ].
Si raccomanda di evitare l'interruzione del co -co -CYP1A2 induttori CYP2B6 o CYP3A. Se è necessario il co -somministrazione di un forte induttore CYP1A2 CYP2B6 o CYP3A con Fintepla, monitorare il paziente per una ridotta efficacia e prendere in considerazione l'aumento del dosaggio di Fintepla, se necessario; tuttavia non superare il dosaggio giornaliero massimo di fintepla [vedi Dosaggio e amministrazione ].
Se un forte induttore CYP1A2 CYP2B6 o CYP3A viene interrotto durante il trattamento di mantenimento con Fintepla considera una riduzione graduale nel dosaggio di fintepla alla dose somministrata prima di iniziare l'induttore [vedi AVVERTIMENTOS AND PRECAUTIONS ].
Inibitori forti CYP1A2 o CYP2D6
La somministrazione di co -conclusione di fintepla con forti inibitori del CYP1A2 o del CYP2D6 aumenterà le concentrazioni plasmatiche di fenfluramina [vedi Farmacologia clinica ]. If Fintepla is coadministered with strong CYP1A2 or CYP2D6 inhibitors the maximum daily dosage of Fintepla is 20 mg [see Dosaggio e amministrazione ].
Se durante il trattamento di mantenimento viene interrotto un forte inibitore del CYP1A2 o del CYP2D6 con il trattamento di mantenimento con Fintepla considera un graduale aumento del dosaggio di fintepla alla dose raccomandata senza inibitori del CYP1A2 o del CYP2D6; tuttavia non superare il dosaggio giornaliero massimo di fintepla [vedi Dosaggio e amministrazione ].
Se la fintepla è amministrata con co -stival e un forte inibitore del CYP1A2 o del CYP2D6 non supera il dosaggio giornaliero massimo di fintepla di 17 mg [vedi Dosaggio e amministrazione ].
Effetti degli antagonisti del recettore della serotonina
Ciproheptadina e potenti antagonisti del recettore della serotonina 5-HT1A 5-HT1D e 5-HT2C possono ridurre l'efficacia della fintepla. Se la ciproheptadina o la potente 5-HT1A 5-HT1D 5-HT2A o 5-HT2C, gli antagonisti del recettore della serotonina sono monitorati con i pazienti in fintepla devono essere monitorati in modo appropriato.
Farmaci serotonergici
Concomitante somministrazione di fintepla e farmaci (ad es. Ssris snris tcas mao inibitori trazodone ecc.) Farmaci da banco (ad esempio dextrometorphan) o integratori a base di erbe (ad es. St. Johns Wort) che aumentano la serotonina può aumentare il rischio di sindrome della serotonin [vedi sindrome di Serotonin. AVVERTIMENTOS AND PRECAUTIONS ]. Concomitant use of Fintepla is contraindicated within 14 days of taking MAOIs. Use Fintepla with caution in patients taking other medications that increase serotonina.
Avvertimenti per Fintepla
Incluso come parte del 'PRECAUZIONI' Sezione
Precauzioni per Fintepla
Malarità della cardiopatia valvolare e ipertensione arteriosa polmonare
Fintepla can cause valvular heart disease (VHD) E pulmonary arterial hypertension (PAH). There is a known association between serotonergic drugs with 5-HT2B receptor agonist activity including fenfluramine (the active ingredient in Fintepla) E valvular heart disease E pulmonary arterial hypertension. Although no patients receiving Fintepla developed valvular heart disease or pulmonary arterial hypertension in clinical trials for DS E LGS of up to 3 years in duration cases of valvular heart disease E pulmonary arterial hypertension have been reported during use of Fintepla in the postmarketing setting [see Avvertenza della scatola E Reazioni avverse ].
A causa di questo rischio è richiesto il monitoraggio cardiaco prima di iniziare il trattamento durante il trattamento e dopo il trattamento con Fintepla. Il monitoraggio cardiaco tramite ecocardiogramma può identificare l'evidenza di malattie cardiache valvolari e ipertensione arteriosa polmonare prima che un paziente diventasse sintomatico aiutando a rilevazione precoce di queste condizioni.
Monitoraggio
Prima di avviare i pazienti con trattamento devono sottoporsi a un ecocardiogramma per valutare la cardiopatia valvolare e l'ipertensione arteriosa polmonare.
Gli ecocardiogrammi devono essere ripetuti ogni 6 mesi e una volta 3-6 mesi dopo il trattamento con Fintepla.
Il prescrittore deve considerare i benefici rispetto ai rischi di avvio o trattamento continuo con Fintepla se uno dei seguenti segni viene osservato tramite eco:
- Anomalia valvolare o nuova anomalia tramite ecocardiogramma.
- VHD come indicato da rigurgito aortico lieve o maggiore o rigurgito mitralico moderato o maggiore con ulteriori caratteristiche di VHD (ad esempio ispessimento della valvola o movimento della valvola restrittiva).
- PAH come indicato dalla pressione elevata del cuore a destra/arteria polmonare (PASP> 35 mm Hg).
Fintepla is available only through a restricted program under a REMS [see Fintepla REMS Program ].
Fintepla REMS Program
Fintepla is available only through a restricted distribution program called the Fintepla REMS program because of the risk of valvular heart disease E pulmonary arterial hypertension [see Malarità della cardiopatia valvolare e ipertensione arteriosa polmonare ].
I requisiti notevoli del programma Fintepla REMS includono:
- I prescrittori devono essere certificati iscrivendoti al programma Fintepla REMS.
- I prescrittori devono consigliare i pazienti che ricevono fintepla per il rischio di malattie cardiache valvolari e ipertensione arteriosa polmonare come riconoscere i segni e i sintomi della malattia valvolare e dell'ipertensione arteriosa polmonare la necessità di basale (pretrattamento) e periodico cardiaco mediante ecocardiogramma durante il trattamento di Fintepla e il monitoraggio cardiaco dopo il trattamento di pintepla.
- I pazienti devono iscriversi al programma REMS e rispettare i requisiti di monitoraggio in corso [vedi Malarità della cardiopatia valvolare e ipertensione arteriosa polmonare ].
- La farmacia deve essere certificata iscrivendoti al programma REMS e deve solo rinunciare ai pazienti autorizzati a ricevere Fintepla.
- I grossisti e i distributori devono distribuire solo a farmacie certificate.
Ulteriori informazioni sono disponibili su www.finteplarems.com o per telefono al numero 1-877-964-3649.
Diminuzione dell'appetito e una riduzione del peso
Fintepla can cause decreases in appetite E weight. In placebo-controlled studies for DS (Studio 1 E Studio 2 combined) approximately 37% of patients treated with Fintepla reported as an adverse reaction diminuzione dell'appetito E approximately 9% reported Diminuzione del peso as compared to 8% E 1% respectively of patients on placebo. In the placebocontrolled study for LGS (Studio 3) approximately 28% of patients treated with Fintepla reported as an adverse reaction diminuzione dell'appetito E approximately 5% reported Diminuzione del peso as compared to 15% E 2% respectively of patients on placebo [see Reazioni avverse ]. By the end of the controlled studies 19% (Studies 1 E 2 combined) of DS patients E 7% (Studio 3) of LGS patients treated with Fintepla had a measured decrease in weight of 7% or greater from their baseline weight compared to 2% (Studio 1 E 2) E 0% (Studio 3) of patients on placebo. This measured decrease in weight appeared to be dose-related. In the controlled studies for DS 26% of patients on Fintepla 0,7 mg/kg/giorno (Studio 1) 19% of patients on Fintepla 0,4 mg/kg/giorno in combination with stiripentol (Studio 2) E 13% of patients taking Fintepla 0,2 mg/kg/giorno (Studio 1) experienced at least a 7% decrease in weight from baseline. In the controlled study for LGS 9% of patients on Fintepla 0,7 mg/kg/giorno (Studio 3) E 6% of patients on Fintepla 0,2 mg/kg/giorno (Studio 3) experienced at least a 7% decrease in weight from baseline. Approximately half of the patients with LGS E most patients with DS resumed the expected measured increases in weight during the open-label extension studies. Given the frequency of these adverse reactions the growth of pediatric patients treated with Fintepla should be carefully monitored. Weight should be monitored regularly during treatment with Fintepla E dose modifications should be considered if a decrease in weight is observed.
Somnolence Sedation and Letargy
Fintepla can cause somnolence sedazione E letargia. In controlled studies for DS (Studio 1 E Studio 2 combined) the incidence of somnolence sedazione E letargia was 25% in patients treated with Fintepla compared with 11% of patients on placebo. In the controlled study for LGS (Studio 3) the incidence of somnolence sedazione E letargia was 19% in patients treated with Fintepla compared with 16% of patients on placebo. In general these effects may diminish with continued treatment [see Reazioni avverse ].
Altri depressivi del sistema nervoso centrale (CNS), incluso l'alcol, potrebbero potenziare questi effetti della fintepla. I prescrittori dovrebbero monitorare i pazienti per la sonnolenza e la sedazione e dovrebbero consigliare ai pazienti di non guidare o gestire macchinari fino a quando non hanno acquisito un'esperienza sufficiente su Fintepla per valutare se influisce negativamente sulla loro capacità di guidare o gestire macchinari.
Comportamento suicida e ideazione
I farmaci antiepilettici (DAE) tra cui Fintepla aumentano il rischio di pensieri o comportamenti suicidari nei pazienti che assumono questi farmaci per qualsiasi indicazione. I pazienti trattati con un DAE per qualsiasi indicazione devono essere monitorati per l'emergere o il peggioramento dei pensieri o del comportamento suicidari della depressione o eventuali cambiamenti insoliti nell'umore o nel comportamento.
Analisi aggregate di 199 studi clinici controllati con placebo (terapia mono e aggiuntiva) di 11 diversi DAE che non includevano Fintepla hanno mostrato che i pazienti randomizzati in uno degli AED avevano circa il doppio del rischio (rischio relativo adeguato 1,8 IC 95%: 1,2 2,7) di pensiero o comportamento suicidali rispetto ai pazienti randomizzati a Placebo. In questi studi che avevano una durata del trattamento mediano di 12 settimane il tasso di incidenza stimato di comportamento suicidario o ideazione tra 27863 pazienti trattati con AED era dello 0,43% rispetto allo 0,24% tra 16029 pazienti trattati con placebo che rappresentavano un aumento di circa un caso di pensiero o comportamento suicidario per ogni 530 pazienti curati. Ci sono stati quattro suicidi nei pazienti trattati con farmaci negli studi e nessuno nei pazienti trattati con placebo, ma il numero è troppo piccolo per consentire qualsiasi conclusione sull'effetto farmaco sul suicidio.
L'aumento del rischio di pensieri o comportamenti suicidari con DAE è stato osservato già 1 settimana dopo aver avviato il trattamento farmacologico con DAE e persistito per la durata del trattamento valutato. Poiché la maggior parte degli studi inclusi nell'analisi non si estendeva oltre le 24 settimane, non è stato possibile valutare il rischio di pensieri o comportamenti suicidari oltre 24 settimane.
Il rischio di pensieri o comportamenti suicidari era generalmente coerente tra i farmaci nei dati analizzati. La scoperta di un aumentato rischio con DAE di diversi meccanismi d'azione e attraverso una serie di indicazioni suggerisce che il rischio si applica a tutti i DAE utilizzati per qualsiasi indicazione. Il rischio non variava sostanzialmente di età (5-100 anni) negli studi clinici analizzati. La tabella 3 mostra il rischio assoluto e relativo per indicazione per tutti i DAE valutati.
Tabella 3: rischio di pensieri o comportamenti suicidari per indicazione per i farmaci antiepilettici nell'analisi aggregata
| Indicazione | Pazienti con placebo con eventi per 1000 pazienti | Pazienti farmacologici con eventi per 1000 pazienti | Rischio relativo: incidenza di eventi nei pazienti farmacologici/ incidenza nei pazienti con placebo | Differenza di rischio: ulteriori pazienti con farmaci con eventi per 1000 pazienti |
| Epilessia | 1.0 | 3.4 | 3.5 | 2.4 |
| Psichiatrico | 5.7 | 8.5 | 1.5 | 2.9 |
| Altro | 1.0 | 1.8 | 1.9 | 0.9 |
| Totale | 2.4 | 4.3 | 1.8 | 1.9 |
Il rischio relativo di pensieri o comportamenti suicidari era più elevato negli studi clinici nei pazienti con epilessia rispetto agli studi clinici nei pazienti con condizioni psichiatriche o di altro tipo, ma le differenze di rischio assoluto erano simili per le indicazioni epilessarie e psichiatriche.
Chiunque stia prendendo in considerazione la prescrizione di fintepla o qualsiasi altro DAE deve bilanciare il rischio di pensieri o comportamenti suicidari con il rischio di malattie non trattate. L'epilessia e molte altre malattie per le quali sono prescritti i DAE sono essi stessi associati alla morbilità e alla mortalità e ad un aumento del rischio di pensieri e comportamenti suicidi. I pensieri suicidari e il comportamento emergano durante il trattamento, considerano se l'emergere di questi sintomi in un dato paziente può essere correlato alla malattia da trattare.
Ritiro di farmaci antiepilettici
Come con la maggior parte dei DAE, la fintepla dovrebbe essere generalmente ritirata gradualmente a causa del rischio di aumento della frequenza delle crisi e dello stato epilettico. Se è necessario un ritiro a causa di una grave reazione avversa una rapida interruzione può essere presa in considerazione.
Sindrome di Seroton
Sindrome di serotonina Una condizione potenzialmente potenzialmente letale può verificarsi con fintepla, in particolare con una concomitante somministrazione di fintepla con altri farmaci serotoninergici, inclusi ma non limitati al selettivo serotonina-norepinefrina, inibitori del reuptake di reupta di serotonina (ssris) antidepressivi (TCAS) BUPRIPION TRIPTANS INGRESSIMENTI DIETERIO (ad esempio il triptofano di San Giovanni) che compromettono il metabolismo della serotonina (inclusi inibitori della monoamina ossidasi [MAOIS] che sono controindicati da Fintepla [vedi Controindicazioni ] destrometorfano Tramadolo di litio e antipsicotici con attività agonista serotoninergica. I pazienti devono essere monitorati per l'emergere di segni e sintomi della sindrome della serotonina che includono cambiamenti di stato mentale (ad esempio allucinazioni di agitazione coma) Instabilità autonomica (ad es. Tachicardia ipertermia della pressione sanguigna). Se la sindrome della serotonina è sospetta di un trattamento con fintepla deve essere arrestato immediatamente e il trattamento sintomatico dovrebbe essere avviato.
Aumento della pressione sanguigna
Fintepla can cause an increase in blood pressure [see Reazioni avverse ]. Rare cases of significant elevation in blood pressure including hypertensive crisis has been reported in adult patients treated with fenfluramine including patients without a history of hypertension. In clinical trials of up to 3 years in duration no pediatric or adult patient receiving Fintepla developed a hypertensive crisis. Monitor blood pressure in patients treated with Fintepla.
Glaucoma
La fenfluramina può causare midriasi e può precipitare la chiusura dell'angolo glaucoma . Prendi in considerazione l'interruzione del trattamento con fintepla in pazienti con diminuzione acuta dell'acuità visiva o del dolore oculare.
Informazioni sulla consulenza del paziente
Consiglia al paziente di leggere l'etichettatura del paziente approvato dalla FDA ( Guida ai farmaci E Instructions for Use ).
Informazioni sull'amministrazione
Consiglia ai pazienti a cui è prescritto Fintepla di utilizzare le siringhe di dosaggio orale fornite dalla farmacia [vedi Dosaggio e amministrazione E Istruzioni per l'uso ]. Instruct patients to discard any unused Fintepla 3 months after first opening the bottle or if the discard after date on the dispensing bottle has passed whichever is sooner [see Come fornito ].
Malarità della cardiopatia valvolare e ipertensione arteriosa polmonare
Consiglia ai pazienti che il monitoraggio cardiaco deve essere eseguito utilizzando l'ecocardiografia per monitorare gravi cambiamenti della valvola cardiaca o la pressione alta nelle arterie dei polmoni [vedi AVVERTIMENTOS AND PRECAUTIONS ].
Fintepla REMS Program
Fintepla is available only through a restricted program called the Fintepla REMS program [see AVVERTIMENTOS AND PRECAUTIONS ]. Inform the patient of the following notable requirements:
- I pazienti devono iscriversi al programma e rispettare i requisiti di monitoraggio dell'ecocardiogramma in corso [vedi AVVERTIMENTOS AND PRECAUTIONS ].
Fintepla is only prescribed by certified health care providers E only dispensed from certified pharmacies participating in the program. Therefore provide patients with the telephone number E website for information on how to obtain the product [see AVVERTIMENTOS AND PRECAUTIONS ].
Diminuzione dell'appetito e una riduzione del peso
Consiglia i pazienti che diminuiscono l'appetito è frequente durante il trattamento con fintepla che può causare una riduzione del peso [vedi AVVERTIMENTOS AND PRECAUTIONS ].
Somnolence Sedation and Letargy
Informare i pazienti che Fintepla può causare sedazione di sonnolenza e letargia. ATTENZIONE I pazienti in merito a macchinari pericolosi in funzione, compresi i veicoli a motore fino a quando non sono ragionevolmente certi che la fintepla non li influisce negativamente (ad esempio, compromettere il pensiero di giudizio o le capacità motorie) [vedi AVVERTIMENTOS AND PRECAUTIONS ].
Pensiero e comportamento suicidi
Consiglio ai pazienti i loro caregiver e le loro famiglie secondo cui i farmaci antiepilettici possono aumentare il rischio di pensieri e comportamenti suicidari e consigliarli di essere vigili per l'emergere o il peggioramento dei sintomi della depressione eventuali cambiamenti insoliti nell'umore o nel comportamento o l'emergere del comportamento dei pensieri suicidi o dei pensieri di autolesile. Istruire i caregiver e le famiglie dei pazienti di segnalare immediatamente comportamenti di preoccupazione per gli operatori sanitari [vedi AVVERTIMENTOS AND PRECAUTIONS ].
Ritiro di farmaci antiepilettici (AEDs)
Consiglia ai pazienti di non interrompere l'uso di Fintepla senza consultare il proprio operatore sanitario. Fintepla deve normalmente essere gradualmente ritirato per ridurre il potenziale per un aumento della frequenza delle crisi e dello stato epilettico [vedi Dosaggio e amministrazione E AVVERTIMENTOS AND PRECAUTIONS ].
Sindrome di Seroton
Informare i pazienti sul rischio di sindrome della serotonina che può essere pericolosa per la vita. Consigliare i pazienti sui segni e sui sintomi della sindrome della serotonina e che alcuni farmaci da banco e integratori a base di erbe possono aumentare questo rischio [vedi AVVERTIMENTOS AND PRECAUTIONS ].
Aumento della pressione sanguigna
Informare i pazienti che la fintepla può causare un aumento della pressione sanguigna [vedi AVVERTIMENTOS AND PRECAUTIONS ].
Glaucoma
Informare i pazienti che Fintepla può causare midriasi e può precipitare il glaucoma della chiusura dell'angolo.
Istruire i pazienti a contattare il proprio operatore sanitario se hanno qualche riduzione acuta dell'acuità visiva o del dolore oculare [vedi AVVERTIMENTOS AND PRECAUTIONS ].
Registro di gravidanza
Consiglia ai pazienti di avvisare il proprio operatore sanitario se rimangono in gravidanza o intendono rimanere incinta durante la terapia del recinta. Incoraggia le donne che stanno prendendo Fintepla ad iscriversi al registro di gravidanza antiepilettico nordamericano (NAAED) se rimangono incinta.
Questo registro sta raccogliendo informazioni sulla sicurezza dei farmaci antiepilettici durante la gravidanza [vedi Utilizzare in popolazioni specifiche ].
Tossicologia non clinica
Mutagenesi della carcinogenesi compromissione della fertilità
Carcinogenesi
La somministrazione orale di fenfluramina ai topi Tg.rash2 (0 4.3 13,0 34,6 o 51,8 mg/kg/giorno) per 26 settimane e verso ratti maschi e femmine (0 0,9 2,2 o 6,9 mg/kg/giorno) per 89 e 97 settimane rispettivamente non hanno provocato alcuna evidenza di tumori indotti da farmaci nelle specie. Nelle esposizioni plasmatiche di ratti (AUC) di fenfluramina e norfenfluramina (il metabolita principale) alla dose più alta testata erano rispettivamente circa 5 e 11 volte quelli nell'uomo alla massima dose umana raccomandata (MRHD) di 26 mg/giorno.
Mutagenesi
La fenfluramina era negativa in un in vitro dosaggio di mutazione batterica (AMES) e un in vivo Tosaggio di micronucleo e cometa nei ratti.
Compromissione della fertilità
La somministrazione orale di fenfluramina (0 3.0 6.9 o 17,3 mg/kg/giorno) ai ratti maschi e femmine prima e attraverso l'accoppiamento e la continuazione nelle femmine fino al giorno 7 di gestazione hanno comportato una diminuzione della fertilità e degli aumenti antomici e dell'epiteliale epiteliale dell'epididimomica al più alto e alternato. Impiantazioni e aumento dell'embriletalità a media e alta dose. Queste dosi erano associate alla tossicità dei genitori. Le dosi senza effetto per gli effetti avversi sulla fertilità e sulle prestazioni riproduttive nei ratti (rispettivamente 6,9 e 3,0 mg/kg/giorno nei maschi e nelle femmine) erano associate a esposizioni plasmatiche di fenfluramina (AUC) circa 3 e 0,6 volte rispettivamente e rispettivamente esposizioni di néfenfluttumina rispettivamente.
Utilizzare in popolazioni specifiche
Gravidanza
Gravidanza Exposure Registry
Esiste un registro di esposizione alla gravidanza che monitora gli esiti di gravidanza nelle donne esposte a farmaci antiepilettici (DAE) come la fintepla durante la gravidanza. Incoraggiare le donne che stanno assumendo la fintepla durante la gravidanza per iscriversi al registro di gravidanza antiepilettico nordamericano (NAAED) chiamando il numero 1-888-233-2334 o visitando https://www.aedpregnancyregistry.org.
Riepilogo del rischio
Non ci sono dati sull'uso di fintepla nelle donne in gravidanza. I dati disponibili da studi epidemiologici con fenfluramina o dexfenfluramina sono insufficienti per valutare un rischio associato ai farmaci di gravi difetti alla nascita o altri risultati avversi materni o fetali. Fintepla può causare una riduzione dell'appetito e una riduzione del peso [vedi AVVERTIMENTOS AND PRECAUTIONS ]; Monitorare per un adeguato aumento di peso durante la gravidanza. Nella somministrazione di studi sugli animali di fenfluramina durante l'organogenesi (ratto e coniglio) o per tutta la gestazione e l'allattamento (ratto) ha portato a effetti avversi sullo sviluppo (malformazioni fetali embriofetali e mortalità e compromissione della crescita) in presenza di tossici materni per la fenflutura materna e la sua metabolite attivo (vedi metabolite attivo (vedi metabolite attivi attivo (vedi metabolite attivo attivo (vedi metabolite attivi attivo (vedi metaboliti Dati ).
Il rischio di background stimato di principali difetti alla nascita e aborto spontaneo per la popolazione indicata non è noto. Tutte le gravidanze hanno un rischio di fondo Difetto alla nascita perdita o altri risultati avversi. Nella popolazione generale degli Stati Uniti il rischio di background stimato di gravi difetti alla nascita e aborto in gravidanza clinicamente riconosciuta è rispettivamente dal 2 al 4% e dal 15 al 20%.
Dati
Dati sugli animali
La somministrazione orale di fenfluramina (0 4,5 8,6 o 34,6 mg/kg/giorno) ai ratti in gravidanza durante l'organogenesi ha comportato una riduzione dei pesi corporei fetali e marcati aumenti delle malformazioni fetali (viscerale esterna e scheletrica) alla dose più alta testata che era associata a tossicità materna. Alla dose senza effetto (NULL,6 mg/kg/giorno) per effetti avversi sullo sviluppo dell'embriofetale nei ratti esposizioni al plasma materna (AUC) di fenfluramina e norfenfluramina (il principale metabolita) erano circa 2 e 5 volte rispettivamente quelli nell'uomo alla massima dose umana (MRHD) di 26 mg/day.
La somministrazione orale di fenfluramina (0 4.3 8.6 13,0 mg/kg/giorno) a conigli incinta durante l'organogenesi ha comportato un aumento della mortalità dell'embriofetale a tutte le dosi e aumenti delle malformazioni fetali (esterne e scheletriche) al più alto test della dose che era associato con tossicità materna. Non è stata identificata una dose di effetto senza effetti avversi per effetti avversi sullo sviluppo dell'embriofetale nei conigli. Alla dose più bassa testata nei conigli (NULL,3 mg/kg/die) le esposizioni al plasma materna di fenfluramina e norfenfluramina erano inferiori a quelle degli umani al MRHD.
La somministrazione orale di fenfluramina (0 4.3 86 o 34,6 mg/kg/giorno) ai ratti femminili durante la gestazione e l'allattamento ha comportato aumenti marcati nei cuccioli nati morti e nei morti della prole neonatale al massimo dosaggio e la crescita ritardata e lo sviluppo del riflesso durante il periodo di preweaning a tutti i dosi. L'aumento di peso corporeo materno è stato ridotto a tutte le dosi durante la gravidanza e alle due dosi più alte durante l'allattamento. Non è stata determinata una dose senza effetto per effetti avversi sullo sviluppo pre e post-natale nei ratti. Alla dose più bassa testata nei ratti (NULL,3 mg/kg/die) le esposizioni materne di plasma di fenfluramina e norfenfluramina erano circa 0,5 e 3 volte rispettivamente quelle nell'uomo al MRHD.
Lattazione
Riepilogo del rischio
Non ci sono dati sulla presenza di fenfluramina o sui suoi metaboliti nel latte umano gli effetti sul bambino allattato al seno o sugli effetti sulla produzione di latte.
I benefici per lo sviluppo e la salute dell'allattamento dovrebbero essere considerati insieme alla necessità clinica delle madri di Fintepla e a potenziali effetti avversi sul bambino allattato al seno dalla fintepla o dalla condizione materna sottostante.
Femmine e maschi di potenziale riproduttivo
Infertilità
Negli studi sugli animali La somministrazione orale di fenfluramina ha comportato effetti riproduttivi avversi nei maschi e nelle femmine a dosi clinicamente rilevanti in presenza di tossicità parentale [vedi Tossicologia non clinica ].
Uso pediatrico
La sicurezza e l'efficacia della fintepla per il trattamento delle convulsioni associate a DS e LG sono state stabilite in pazienti di età pari o superiore a 2 anni.
L'uso di Fintepla per il trattamento delle convulsioni associate alla DS in pazienti di età pari o superiore a 2 anni è supportato da due studi randomizzati controllati in doppio cieco in doppio cieco in 202 pazienti da 2 a 18 anni. L'uso di Fintepla per il trattamento delle convulsioni associate a LGS è supportato da uno studio randomizzato in doppio cieco controllato con placebo in 263 pazienti di età compresa tra 2 e 35 anni di cui 187 pazienti in meno di 18 anni [vedi Avvertenza della scatola AVVERTIMENTOS AND PRECAUTIONS Reazioni avverse E Studi clinici ].
Fintepla can cause decreases in appetite E weight. The growth of pediatric patients treated with Fintepla should be carefully monitored.
La sicurezza ed efficacia nei pazienti di età inferiore ai 2 anni non è stata stabilita.
Dati sugli animali giovanili
La somministrazione orale di fenfluramina (0 3.0 78 o 17,3 mg/kg/giorno) a giovani ratti per 10 settimane a partire dal giorno post -natale 7 ha comportato una riduzione del peso corporeo e dei cambiamenti neurocomportamentali (riduzione dell'attività locomotoria e dei deficit di apprendimento e della memoria) a tutti i dosi testate. Gli effetti neurocomportamentali persistevano dopo che il dosaggio fu interrotto. La dimensione dell'osso è stata ridotta a metà e alte dosi; La dimensione del cervello è stata ridotta alla dose più alta. È stato visto un recupero parziale o completo per questi endpoint. Non è stata identificata una dose senza effetto per la tossicità dello sviluppo postnatale. La dose più bassa testata (NULL,0 mg/kg/giorno) era associata alle esposizioni di fenfluramina plasmatica (AUC) in meno di quella negli esseri umani alla massima dose umana raccomandata (MRHD) di 26 mg/die e Norfenfluramine (metabolite) Exposures (AUC) circa 2 volte che negli esseri umani dell'MRHD.
Uso geriatrico
Studi clinici sulla fintepla per il trattamento di DS o LGS non includevano i pazienti di età pari o superiore a 65 anni per determinare se rispondono in modo diverso dai pazienti più giovani. In generale, la selezione della dose per un paziente anziano dovrebbe essere cauta di solito a partire dalla fascia bassa dell'intervallo di dosaggio che riflette la maggiore frequenza della ridotta funzione renale e cardiaca epatica e di malattia concomitante o altra terapia farmacologica.
Reazione allergica a Botox intorno agli occhi
Compromissione renale
Nei pazienti con velocità di filtrazione glomerulare stimata (EGFR) da 15 a 29 ml/min/1,73 m 2 Non superare il dosaggio giornaliero massimo di fintepla di 20 mg. Nei pazienti con EGFR da 15 a 29 ml/min/1,73 m 2 E concomitant stiripentol use do not exceed the maximum daily dosage of Fintepla of 17 mg [see Dosaggio e amministrazione E Farmacologia clinica ].
Fintepla has not been studied in patients with eGFR <15 mL/min/1.73m 2 .
Compromissione epatica
Le esposizioni molari combinate di fenfluramina e norfenfluramina sono state aumentate in soggetti con vari gradi di compromissione epatica (Classe A B e C) che richiedono un aggiustamento del dosaggio in questi pazienti [vedi Dosaggio e amministrazione E Farmacologia clinica ].
Informazioni per overdose per fintepla
Non è stato osservato il sovradosaggio nel programma di sperimentazione clinica Fintepla. Tuttavia, il sovradosaggio di fenfluramina, il principio attivo nella fintepla è stato riportato a dosi più elevate rispetto a quelle incluse nel programma di studio clinico. Alcuni dei casi erano fatali. Gli eventi segnalati dopo il sovradosaggio includono tachicicardia di midriasi Tremori di lavaggio/contrazioni/spasmi muscolari Agitazione/irrequietezza/ansia aumentata il tono muscolare/rigore/opisthotonos Disticità respiratoria o fallimento e attacco. Il coma convulsivo e l'arresto cardiorespiratorio sono stati segnalati nella maggior parte delle overdose fatali.
Non esiste un antidoto specifico disponibile alle reazioni di overdose di Fintepla. In caso di overdose, è necessario utilizzare una pratica medica standard per la gestione del sovradosaggio di droghe. Dovrebbero essere garantite un'ossigenazione e ventilazione adeguate delle vie aeree; Si raccomanda il monitoraggio del ritmo cardiaco e della misurazione del segno vitale. Un centro di controllo del veleno certificato deve essere contattato per informazioni aggiornate sulla gestione del sovradosaggio con Fintepla.
Controindicazioni per Fintepla
Fintepla is contraindicated in patients with:
- Ipersensibilità alla fenfluramina o uno qualsiasi degli eccipienti nella fintepla [vedi DESCRIZIONE ]
- Uso concomitante o entro 14 giorni dalla somministrazione di inibitori della monoamina ossidasi a causa di un aumentato rischio di sindrome della serotonina [vedi AVVERTIMENTOS AND PRECAUTIONS ]
Farmacologia clinica for Fintepla
Meccanismo d'azione
Il meccanismo preciso mediante il quale la fenfluramina esercita i suoi effetti terapeutici nel trattamento delle convulsioni associate alla sindrome di Dravet e alla sindrome di Lennox-Gastaut non è noto. La fenfluramina e il metabolita Norfenfluramina presentano attività agoniste nei recettori della serotonina 5-HT2. Esiste un'associazione tra farmaci serotonergici con attività agonista del recettore 5-HT2B tra cui fenfluramina e norfenfluramina e malattia valvolare e ipertensione arteriosa polmonare.
Farmacodinamica
Elettrofisiologia cardiaca
Ad una dose 4 volte la dose massima raccomandata fintepla non ha prolungato l'intervallo QT quando testato in una popolazione adulta.
Farmacocinetica
La farmacocinetica di fenfluramina e norfenfluramina è stata studiata in soggetti sani in pazienti pediatrici con DS e in pazienti pediatrici e adulti con LGS. L'esposizione sistemica allo stato stazionario (CMAX e AUC) di fenfluramina era leggermente maggiore della dose proporzionale nell'intervallo di dose da 13 a 51,8 mg di fenfluramina due volte al giorno (cioè da 1 a 4 volte la dose massima raccomandata). Nei pazienti pediatrici con DS che hanno ricevuto fintepla 0,7 mg/kg/giorno fino a una dose giornaliera totale di 26 mg di fenfluramina la fenfluramina medio geometrica stazionaria fenfluramina (coefficiente di variazione) CMAX era 68,0 (41%) ng/ml e AUC0-24h era 1390 (44%) ng*ml.
Assorbimento
La fenfluramina ha un tempo alla massima concentrazione plasmatica (TMAX) da 3 a 5 ore a stato stazionario. La biodisponibilità assoluta della fenfluramina è di circa il 68-74%. Non vi è stato alcun effetto di cibo sulla farmacocinetica della fenfluramina o della norfenfluramina.
Distribuzione
La media geometrica (CV%) il volume apparente di distribuzione (VZ/F) della fenfluramina è di 11,9 (NULL,5%) L/kg dopo la somministrazione orale di Fintepla in soggetti sani. La fenfluramina è legata al 50% alle proteine plasmatiche umane in vitro E binding is independent of drug concentrations.
Eliminazione
L'emivita di eliminazione della fenfluramina è stata di 20 ore e la mediazione media (CV%) (CV%) (CL/F) era di 24,8 (29%) L/H dopo la somministrazione orale di Fintepla in soggetti sani.
Metabolismo
Oltre il 75% della fenfluramina viene metabolizzato in norfenfluramina prima dell'eliminazione principalmente dal CYP1A2 CYP2B6 e CYP2D6. Altri enzimi del CYP coinvolti in misura minore sono CYP2C9 CYP2C19 e CYP3A4/5. Sia la fenfluramina che la norfenfluramina sono farmacologicamente attive. La norfenfluramina è ulteriormente deaminata e ossidata per formare metaboliti inattivi.
Escrezione
La maggior parte di una dose somministrata per via orale di fenfluramina (maggiore del 90%) viene escreta nelle urine come fenfluramina norfenfluramina o altri metaboliti con fenfluramina e norfenfluramina che rappresentano meno del 25% del totale; Meno del 5% si trova nelle feci.
Popolazioni specifiche
L'effetto dell'età (intervallo: da 2 a 50 anni) sesso e razza non hanno avuto alcun effetto clinicamente significativo sulla farmacocinetica della fenfluramina.
Pazienti con compromissione renale
In uno studio clinico dedicato che confronta la farmacocinetica di una singola dose di 0,35 mg/kg di fintepla in soggetti con grave compromissione renale (EGFR <30 mL/min/1.73m 2 Determinato da MDRD) e abbinati volontari sani CMAX e AUC0-INF di fenfluramina sono aumentati rispettivamente del 20% e dell'88% e CMAX e AUC0-INF di Norfenfluramina sono aumentati del 13% e del 21% rispettivamente nei soggetti con grave compromissione renale [vedi Utilizzare in popolazioni specifiche ].
Fintepla has not been studied in patients with eGFR <15 mL/min/1.73m 2 (determinato da MDRD). Non è noto se la fenfluramina o la norfenfluramina sono dializzabili.
Pazienti con compromissione epatica
In uno studio che confronta la farmacocinetica di una singola dose di 0,35 mg/kg di fintepla in soggetti con lieve moderata o grave compromissione epatica (bambino-pugh di classe A B o C) e soggetti con funzionalità epatica normale di fenfluramina aumentata rispettivamente del 95% e 185% in soggetti lievi moderati e gravi erepatica rispettivamente. CMAX di fenfluramina è aumentato del 19% 16% e del 29% nei soggetti con lieve moderata e grave compromissione epatica rispettivamente. L'AUC0-T di Norfenfluramina è aumentato del 18% in lieve compromissione epatica del 4% in moderata compromissione epatica e diminuito dell'11% in grave compromissione epatica. La CMAX di Norfenfluramina è diminuita del 21% del 36% e del 45% nei soggetti con lieve moderata e grave compromissione epatica rispettivamente. L'AUC0-T molare combinato di fenfluramina e norfenfluramina è aumentato del 55% 56% e 82% nei soggetti con un lieve compromissione epatica moderata e grave rispettivamente. Il CMAX molare combinato di fenfluramina e norfenfluramina è aumentato del 7,5% dell'1,3% e dell'8% nei soggetti con lieve moderata e grave compromissione epatica rispettivamente. Il dosaggio giornaliero massimo di fintepla dovrebbe essere ridotto in pazienti con lieve compromissione epatica con/senza stirtidel più clobazam. Il dosaggio giornaliero massimo di fintepla dovrebbe essere ridotto in pazienti con compromissione epatica moderata o grave senza stirpollo più clobazam [vedi Dosaggio e amministrazione E Utilizzare in popolazioni specifiche ].
Studi sull'interazione farmacologica
Studi clinici
Effetto di una singola dose di ampientolo clobazam e combinazione di acido valproico
Coadministration of a single 0.7 mg/kg dose of FINTEPLA with a single dose of a stiripentol clobazam and valproic acid combination in healthy volunteers increased the AUC0-inf of fenfluramine by 69% and the Cmax by 18% and decreased the AUC0-72 hours of norfenfluramine by 41% and the Cmax by 42% as compared to FINTEPLA administered solo.
Effetto del maghipenlo a stato stazionario più clobazam con o senza valproato
I dati di farmacocinetica di fenfluramina sono stati raccolti dai pazienti dopo aver ricevuto somministrazioni multiple di fenfluramina nello Studio 1 e nello studio 2. La modellazione e la simulazione di farmacocinetica della popolazione sono state utilizzate per valutare l'effetto di Stimipenol più Clobazam con o senza valproato sulla farmacocinetica della fenfluramina. L'effetto di StilEpentol Plus Clobazam con o senza valproato sulla farmacocinetica della fenfluramina è maggiore quando Fintepla è allo stato stazionario rispetto alla prima dose di fintepla. A stato stazionario nella popolazione di pazienti la somministrazione di co-co-0,1 mg/kg due volte al giorno (NULL,2 mg/kg/giorno) massimo 17 mg/giorno di fintepla con stirtide più clobazam con o senza valproato dovrà comportare un aumento del 166% nella fenfluramina auc0-24 e un diminuzione del 38% nell'aucfenfluramina rispetto a 0,2% in fase di fenfluramine auc0-24 e un riduzione del 38% nell'aucffenflurammina rispetto a 0,2% in fase di fenfluramina Auc0-24 e un diminuzione del 38% nella norfenfluramina rispetto a 0,2% in fase di fenfluramine AUC0-24 e un diminuzione del 38% nella Norfenflurammina rispetto a 0,2 per il 0,2%. Dose di recinta massima di 26 mg/giorno somministrata da sola [vedi Dosaggio e amministrazione E Interazioni farmacologiche ].
Effetto del cannabidiolo stazionario
La somministrazione di co-somministrazione di una singola dose di Fintepla di 0,35 mg/kg con dosi ripetute di cannabidiolo ha aumentato l'AUC0-INF della fenfluramina del 59% e il CMAX e hanno ridotto l'AUC0-INF di Norfenfluramina del 22% e il CMAX del 33% rispetto a Fintepla da solo. Questa interazione non dovrebbe essere clinicamente significativa.
Effetto di forti inibitori del CYP1A2 o del CYP2D6
La somministrazione di co-somministrazione di una singola dose di 0,35 mg/kg di fintepla con fluvoxamina (un forte inibitore del CYP1A2) allo stato stazionario (50 mg una volta al giorno) in volontari sani ha aumentato l'AUC0- INF di Fenfluramine del 44% a causa del 44% e somministrato da solo [vedi Interazioni farmacologiche ].
Coadministration of a single 0.35 mg/kg dose of FINTEPLA with paroxetine (a strong CYP2D6 inhibitor) at steady state (30 mg once daily) in healthy volunteers increased the AUC0-inf of fenfluramine by 81% and the Cmax by 13% and decreased the AUC0-inf of norfenfluramine by 13% and the Cmax by 29% as compared to FINTEPLA somministrato da solo [vedi Interazioni farmacologiche ].
Effetto di forti induttori CYP1A2 CYP2B6 o CYP3A
La somministrazione di co-somministrazione di un singolo dose di 0,35 mg/kg di fintepla con rifampina (un induttore CYP1A2 CYP2B6 e CYP3A) allo stato stazionario (600 mg una volta al giorno) in volontari sani ha ridotto l'AUC0-INF di Fenfluramine del 58% e il CMAX del 40% e ha diminuito il cM-Inf del NOUC di NOUCF di 5% e Norfenfluramina del 13% rispetto alla fintepla somministrata da sola [vedi Interazioni farmacologiche ].
Effetto della fintepla su altri farmaci
Coadministration of a single 0.7 mg/kg dose of FINTEPLA with a single dose of a stiripentol clobazam and valproic acid combination did not affect the pharmacokinetics of stiripentol nor the pharmacokinetics of clobazam or its N.desmethyl-metabolite norclobazam nor the pharmacokinetics of valproic acid as compared to the stiripentol clobazam e solo combinazione di acido valproico. La somministrazione di co -somministrazione di una singola dose di 0,35 mg/kg di fintepla con dosi ripetute di cannabidiolo non ha influenzato la farmacocinetica del cannabidiolo rispetto al solo cannabidiolo.
Studi in vitro
La fenfluramina è principalmente metabolizzata da CYP1A2 CYP2B6 e CYP2D6 in vitro . Altri enzimi del CYP coinvolti in misura minore sono CYP2C9 CYP2C19 e CYP3A4/5.
Effetto della fenfluramina e della norfenfluramina sui substrati del CYP: fenfluramina e norfenfluramina non sono inibitori o induttori di CYP1A2 CYP2B6 CYP2C8 CYP2C9 CYP2C19 CYP2D6 o CYP3A4 a concentrazioni clinicamente relative.
Effetto dei trasportatori su fenfluramina e norfenfluramina: la fenfluramina e la norfenfluramina non sono substrati di OAT1 OAT1 OAT1 OAT1 OAT1 o Mate2-K.
Effetto della fintepla sui trasportatori: la fenfluramina e la norfenfluramina non sono inibitori dei trasportatori OAT1B1 OAT1B1 OATP1B3 OAT1 OAT1 OAT1 o Mate2-K.
Studi clinici
Sindrome di Dravet
L'efficacia della fintepla per il trattamento delle convulsioni associate alla DS in pazienti di età pari o superiore a 2 anni è stata stabilita in due studi randomizzati controllati in doppio cieco contro il placebo in pazienti di età compresa tra 2 e 18 anni.
Studio 1 (N=117) compared a 0,7 mg/kg/giorno E a 0,2 mg/kg/giorno dose of Fintepla with placebo in patients who were not receiving stiripentol (NCT02682927 E NCT02826863).
Studio 2 (N=85) compared a 0,4 mg/kg/giorno dose of Fintepla with placebo in patients who were receiving stiripentol E either clobazam valproate or both (NCT02926898). In both studies patients had a clinical diagnosis of DS E were inadequately controlled on at least one AED or other antiseizure treatment including vagal nerve stimulation or a ketogenic diet. Both trials had a 6-week baseline period during which patients were required to have a minimum of 6 convulsive seizures while on stable AED therapy. Convulsive seizures included tonic clonic generalized tonic-clonic tonic-atonic secondarily generalized tonic-clonic hemiclonic E focal with observable motor signs. The baseline period was followed by rEomization into a 2- week (Studio 1) or 3-week (Studio 2) titration period E a subsequent 12-week maintenance period where the dose of Fintepla remained stable.
Nello studio 1 98% dei pazienti stava assumendo tra 1 e 4 DAE concomitanti. I DAE concomitanti più frequentemente utilizzati (in almeno il 25%dei pazienti) sono stati il clobazam valproato (61%) (59%) e il topiramato (25%). Nello studio 2 il 100% dei pazienti stava assumendo tra 2 e 4 DAE concomitanti. I DAE concomitanti più frequentemente utilizzati (in almeno il 25%dei pazienti) sono stati lo stirmipentolo (100%) clobazam (94%) e valproato (89%).
L'endpoint di efficacia primaria in entrambi gli studi è stato il cambiamento dal basale nella frequenza delle convulsioni convulsive per 28 giorni durante i periodi combinati di titolazione e manutenzione (Studio 1) o 15 settimane (studio 2) (cioè periodo di trattamento). È stato anche valutato l'intervallo più lungo mediano tra convulsioni convulsive.
Nello studio 1 e dello studio 2 la riduzione della frequenza convulsiva convulsiva per 28 giorni era statisticamente significativamente maggiore per tutti i gruppi di dose di fintepla rispetto al placebo (Tabella 6). Una riduzione delle convulsioni convulsive è stata osservata entro 3-4 settimane dall'inizio della fintepla e l'effetto è rimasto generalmente coerente nel periodo di trattamento di 14 o 15 settimane.
Tabella 6: variazione della frequenza convulsiva convulsiva durante il periodo di trattamento i pazienti ricoverati con sindrome di Dravet (Studio 1 e Studio 2)
| Frequenza convulsiva convulsiva (per 28 giorni) | Placebo | Fintepla 0,2 mg/kg/giorno | Fintepla 0,7 mg/kg/giorno | Fintepla 0,4 mg/kg/giorno |
| Studio 1 | N = 39 | N = 38 | N = 40 | N / a |
| Media del periodo di base | 29.4 | 18.1 | 18.7 | N / a |
| % Di differenza rispetto al placebo* | -31,7% | -70,0% | N / a | |
| valore p rispetto al placebo | 0.043 | <0.001 | ||
| Studio 2 | N = 42 | N / a | N / a | N = 43 |
| Media del periodo di base | 11.5 | N / a | N / a | 15.0 |
| % Di differenza rispetto al placebo* | N / a | -59,5% | ||
| valore p rispetto al placebo | <0.001 | |||
| *Derivato dal modello di analisi primaria ± tutti i pazienti con 0,4 mg/kg/giorno stavano anche assumendo un patipentolo concomitante che aumenta l'esposizione di fintepla. |
La Figura 1 e la Figura 2 mostrano la percentuale di pazienti per categoria di risposta convulsiva dalla linea di base nella frequenza convulsiva convulsiva (per 28 giorni) durante il periodo di trattamento rispettivamente nello studio 1 e nello studio 2.
Figura 1: proporzione di pazienti per categoria di risposta convulsiva per fintepla e placebo in pazienti con sindrome di Dravet (Studio 1)
| |
Figura 2: proporzione di pazienti per categoria di risposta convulsiva per fintepla e placebo in pazienti con sindrome di Dravet (Studio 2)
| |
Nello studio 1 3 su 40 (8%) pazienti nel gruppo Fintepla 0,7 mg/kg/giorno e 3 su 38 (8%) pazienti nel gruppo Fintepla 0,2 mg/kg/giorno non hanno riportato convulsioni convulsive durante il periodo di trattamento di 14 settimane rispetto a 0 pazienti nel gruppo placebo. Nello studio 2 1 su 43 (2%) pazienti nel gruppo Fintepla 0,4 mg/kg/giorno non ha riportato convulsioni convulsive durante il periodo di trattamento di 15 settimane rispetto a 0 pazienti nel gruppo placebo.
Nello studio 1 e dello studio 2 Fintepla è stato associato a un intervallo statisticamente significativo più lungo tra convulsioni convulsive rispetto al placebo (Figura 3).
Figura 3: intervallo più lungo mediano tra convulsioni convulsive nei pazienti con sindrome di Dravet (Studio 1 e Studio 2)
| |
Sindrome di Lennox-Gastaut
L'efficacia di Fintepla per il trattamento delle convulsioni associate a LGS in pazienti di età pari o superiore a 2 anni è stata stabilita in uno studio randomizzato in doppio cieco controllato con placebo in 263 pazienti da 2 a 35 anni (Studio 3; NCT03355209).
Studio 3 compared a 0,7 mg/kg/giorno E a 0,2 mg/kg/giorno dose of Fintepla with placebo.
I pazienti avevano una diagnosi di LGS e venivano controllati in modo inadeguato su almeno un DAE con o senza stimolazione del nervo vagale e/o dieta chetogenica. Lo studio ha avuto un periodo di base di 4 settimane durante il quale i pazienti dovevano avere un minimo di 8 convulsioni di caduta durante la terapia con DAD stabile. Le convulsioni di caduta sono state generalizzate convulsioni toniche toniche-cloniche e toniche-cloniche secondarie generalizzate che sono state confermate per provocare gocce. Il periodo di base è stato seguito da randomizzazione in un periodo di titolazione di 2 settimane e un successivo periodo di manutenzione di 12 settimane in cui la dose di fintepla è rimasta stabile.
Nello studio 3 il 99% dei pazienti stava assumendo tra 1 e 4 DAE concomitanti. I DAE concomitanti più frequentemente utilizzati (in almeno il 25%dei pazienti) sono stati Clobazam (45%) lamotrigina (34%) e valproato (56%).
L'endpoint di efficacia primaria nello Studio 3 era la variazione della percentuale mediana dal basale nella frequenza delle convulsioni di caduta per 28 giorni durante i periodi combinati di titolazione e manutenzione di 14 settimane (cioè periodo di trattamento). La percentuale di pazienti che ottengono miglioramenti (minimamente o molto migliorati) nell'impressione clinica globale del cambiamento (CGI-I) valutato dal ricercatore principale era un endpoint secondario.
Nello studio 3 la variazione della percentuale mediana dal basale (riduzione) nella frequenza delle convulsioni di caduta per 28 giorni era significativamente maggiore per il gruppo di dose di 0,7 mg/kg/giorno di recinte rispetto al placebo (Tabella 7). Una riduzione delle convulsioni di caduta è stata osservata entro 2 settimane dall'inizio del trattamento con fintepla e l'effetto è rimasto generalmente coerente nel periodo di trattamento di 14 settimane.
La riduzione della percentuale mediana dal basale nella frequenza convulsiva per caduta per 28 giorni per la dose più bassa di fintepla (NULL,2 mg/kg/giorno) non ha raggiunto una significatività statistica rispetto al placebo (Tabella 7).
Tabella 7: variazione della frequenza delle crisi di caduta durante il periodo di trattamento nei pazienti con la sindrome di Lennox-Gastaut (Studio 3)
| Frequenza convulsiva per caduta (per 28 giorni) | Placebo | Fintepla 0,2 mg/kg/giorno | Fintepla 0,7 mg/kg/giorno |
| Studio 3 | N = 85* | N = 86* | N = 83* |
| Media del periodo di base Confisca Frequency | 55.0 | 77.8 | 80.0 |
| Variazione percentuale mediana dal basale durante il trattamento | -8,7% | -13,2% | -23,7% |
| valore p rispetto al placebo | 0.1917 | 0.0037 | |
| *Il numero totale di pazienti su cui si basava l'analisi di efficacia è inferiore al numero totale randomizzato nello studio in doppio cieco controllato con placebo perché i pazienti con dati mancanti sono stati esclusi dall'analisi di efficacia. |
La Figura 4 mostra la percentuale di pazienti per categoria di riduzione dalla linea di base nella frequenza convulsiva per 28 giorni durante il periodo di trattamento nello Studio 3.
Figura 4: proporzione di pazienti per categoria di risposta convulsiva per fintepla e placebo in pazienti con sindrome di Lennox.
| |
Miglioramenti numericamente maggiori sul CGI-I da parte dello studio sono stati osservati nei pazienti trattati con Fintepla rispetto al placebo.
Informazioni sul paziente per Fintepla
FinteplaR ®
(Fin-tep-la)
(fenfluramina) soluzione orale
Leggi questa guida ai farmaci prima di iniziare a prendere Fintepla e ogni volta che ricevi una ricarica. Potrebbero esserci nuove informazioni. Queste informazioni non prendono il posto di parlare con il proprio operatore sanitario sulla condizione medica o sul trattamento.
Quali sono le informazioni più importanti che dovrei sapere su Fintepla?
Fintepla can cause serious side effects including :
1. Problemi con le valvole nel cuore (cardiopatia valvolare) e la pressione alta nelle arterie dei polmoni (ipertensione arteriosa polmonare) sono stati associati a Fintepla. Il tuo operatore sanitario eseguirà un test chiamato ecocardiogramma per controllare il tuo cuore e per l'ipertensione nelle arterie dei polmoni prima di ricominciare a prendere la fintepla ogni 6 mesi durante il trattamento e una volta da 3 a 6 mesi dopo aver assunto la tua ultima dose di Fintepla.
Chiama subito il tuo operatore sanitario se si sviluppa uno di questi segni e sintomi di problemi cardiaci o polmonari durante il trattamento con Fintepla:
- fiato corto
- dolore al petto
- stanchezza o debolezza
- sensazioni di un battito cardiaco rapido svolazzante
- Soprattutto con una maggiore attività (palpitazioni)
- Accendino or svenimento
- impulso irregolare
- caviglie o piedi gonfi
- colore bluastro sulle labbra e la pelle (cianosi)
A causa del rischio di problemi della valvola cardiaca (cardiopatia valvolare) e dell'ipertensione nelle arterie dei polmoni (ipertensione arteriosa polmonare) Fintepla è disponibile solo attraverso un programma limitato chiamato Programma di valutazione del rischio di Fintepla e strategia di mitigazione (REMS). Prima che tu o tuo figlio riceva Fintepla, il tuo medico o il tuo farmacista ti assicurerai di capire come prendere la fintepla in sicurezza. In caso di domande su Fintepla, chiedi al tuo medico, visitare www.finteplarems.com o chiamare il numero 1-877-964-3649.
2. Riduzione dell'appetito e un peso ridotto. Diminuzione dell'appetito E Diminuzione del peso are both serious E common side effects of Fintepla in people with Dravet syndrome (DS) or Lennox-Gastaut syndrome (LGS).
- Il tuo peso deve essere controllato regolarmente durante il trattamento con Fintepla.
- Il tuo operatore sanitario potrebbe essere necessario apportare modifiche alla dose di fintepla se il peso diminuisce. In alcuni casi potrebbe essere necessario fermare Fintepla.
3. Sedazione sonnolenza e mancanza di energia (letargia). Questi sono effetti collaterali sia gravi che comuni della fintepla nelle persone con sindrome di Dravet (DS) o sindrome di Lennox-Gastaut (LGS). L'assunzione di fintepla con i depressivi del sistema nervoso centrale (SNC), incluso l'alcol, può aumentare la sonnolenza. Non guidare a funzionare macchinari pesanti o fare altre attività pericolose fino a quando non sai come ti colpisce la fintepla.
4. Come tutti gli altri farmaci antiepilettici, la fintapla può causare pensieri o azioni suicidarie in un numero molto piccolo di persone (circa 1 su 500).
Chiama subito il tuo operatore sanitario se hai uno di questi sintomi soprattutto se sono nuovi peggio o ti preoccupano:
- Pensieri sul suicidio o la morte
- ansia nuova o peggiore
- problemi a dormire (insonnia)
- agire su impulsi pericolosi
- tentativi di suicidarsi
- sentirsi agitato o irrequieto
- irritabilità nuova o peggiore
- Un estremo aumento dell'attività e parlare (mania)
- depressione nuova o peggiore
- attacchi di panico
- agire aggressivo essere arrabbiato o violento
- Altri cambiamenti insoliti nel comportamento o nell'umore
Come posso guardare per i primi sintomi di pensieri e azioni suicidari?
- Presta attenzione a eventuali cambiamenti in particolare improvvisi cambiamenti nei comportamenti dell'umore o ai sentimenti.
- Conserva tutte le visite di follow-up con il tuo medico come previsto.
I pensieri o le azioni suicidi possono essere causati da cose diverse dai medicinali. Se hai pensieri o azioni suicidarie, il tuo operatore sanitario può verificare altre cause.
5. Non smettere di prendere Fintepla senza prima parlare con il tuo operatore sanitario. L'arresto di una medicina convulsiva come la fintepla improvvisamente può farti avere convulsioni più spesso o convulsioni che non si fermano (stato epilettico).
Chiama il tuo operatore sanitario tra le visite secondo necessità, specialmente se sei preoccupato per i sintomi.
Cos'è Fintepla?
- Fintepla is a prescription medicine used to treat the seizures associated with Dravet syndrome (DS) E Lennox- Gastaut syndrome (LGS) in patients 2 years of age E older.
- Non è noto se la fintepla è sicura ed efficace nei bambini di età inferiore ai 2 anni.
Non prendere Fintepla se tu:
- sono allergici alla fenfluramina o a uno qualsiasi degli ingredienti nella fintepla. Vedi la fine di questa guida ai farmaci per un elenco completo di ingredienti nella fintepla.
- stanno assumendo o hanno smesso di assumere medicinali chiamati inibitori della monoamina ossidasi (MAOI) negli ultimi 14 giorni. Ciò può causare un problema grave o pericoloso per la vita chiamato sindrome della serotonina. Se non sei sicuro se stai prendendo o meno uno di questi medicinali contatta il tuo medico.
Prima di prendere Fintepla, racconta al tuo operatore sanitario su tutte le tue condizioni mediche, anche se tu:
- avere problemi cardiaci
- avere o avere una perdita di peso
- avere o avere o avere problemi dell'umore della depressione o pensieri o comportamenti suicidari
- avere problemi ai reni
- avere problemi epatici
- sono incinta o prevedono di rimanere incinta. Di 'subito al tuo operatore sanitario se rimani incinta mentre prendi la fintepla. Tu e il tuo operatore sanitario deciderete se dovresti prendere fintepla mentre siete incinta.
- Se rimani incinta mentre prendi la fintepla, parla con il tuo operatore sanitario sulla registrazione con il registro della gravidanza antiepilettica nordamericana. Puoi iscriverti a questo registro chiamando il numero 1-888-233-2334 o andare a www.
- aedpregnancyregistry.org. Lo scopo di questo registro è di raccogliere informazioni sulla sicurezza dei farmaci antiepilettici durante la gravidanza.
- stanno allattando o pianificano di allattare. Non è noto se Fintepla passa nel latte materno. Parla con il tuo operatore sanitario del modo migliore per nutrire il tuo bambino mentre prendi Fintepla.
Di 'al tuo operatore sanitario di tutte le medicine che prendi tra cui prescrizione e medicine da banco vitamine e integratori a base di erbe.
Conosci le medicine che prendi. Tienilo un elenco per mostrare il tuo medico o il tuo farmacista quando ottieni un nuovo medicinale.
Come dovrei prendere Fintepla?
- Leggi il Istruzioni per l'uso Alla fine di questa guida ai farmaci per informazioni sul modo giusto di utilizzare Fintepla.
- Prendi Fintepla esattamente come il tuo operatore sanitario ti dice di prenderlo.
- Il tuo operatore sanitario ti dirà quanta fintepla prendere e quando prenderlo.
- Fintepla may be taken with or without food.
- Misura la tua dose di fintepla usando la siringa dosata fornita dalla farmacia. Non utilizzare un cucchiaino o un cucchiaio domestico.
- Fintepla can be given through gastric E nasogastric feeding tubes
Cosa dovrei evitare mentre prendi la fintepla?
- Non farlo Guida azionare macchinari pesanti o svolgere altre attività pericolose fino a quando non sai come ti colpisce Fintepla. Fintepla può farti sentire assonnato.
Quali sono i possibili effetti collaterali della fintepla?
Fintepla may cause serious side effects including:
Chiama subito il tuo medico se si dispone dei seguenti sintomi della sindrome della serotonina.
- Vedi Quali sono le informazioni più importanti che dovrei sapere su Fintepla?
- serotonina syndrome. La sindrome di serotonin è un problema pericoloso per la vita che può accadere nelle persone che assumono fintepla soprattutto se viene presa la fintepla con determinati altri medicinali da includere:
- medicinali antidepressivi chiamati ssris snris tcas e maois
- ST. Johns Wort
- triptofano
- destrometorfano
- litio
- tramadolo
- antipsicotici
- Cambiamenti dello stato mentale come vedere cose che non ci sono (allucinazioni) agitazione o coma
- battito cardiaco veloce
- Diarrea di vomito di nausea
- Cambiamenti nella pressione sanguigna
- alta temperatura corporea
- muscoli stretti
- difficoltà a camminare
- Ipertensione (ipertensione). L'ipertensione è sia un effetto collaterale grave che comune. Fintepla può far aumentare la pressione sanguigna anche se non hai mai avuto la pressione alta prima. Il tuo operatore sanitario controllerà la pressione sanguigna mentre stai prendendo Fintepla.
- aumento della pressione negli occhi (glaucoma). I sintomi del glaucoma possono includere:
- occhi rossi
- Visione ridotta
- vedere aloni o colori vivaci attorno alle luci
- dolore agli occhi o disagio
- nausea o vomito
- visione sfocata
Se hai uno di questi sintomi, chiama subito il tuo operatore sanitario.
Gli effetti collaterali più comuni di Fintepla quando usati per trattare la sindrome di Dravet (DS) includono:
- diminuzione dell'appetito
- diarrea
- bassa energia
- sonnolenza
- Problemi con l'equilibrio del movimento e la camminata
- aumento sbavando
- infezione respiratoria
- aumento della pressione sanguigna
- Diminuzione del peso
- vomito
- febbre
- cadute
- stipsi
- convulsioni che non si fermano
- Ecocardiogramma anormale
- debolezza
Gli effetti collaterali più comuni di Fintepla se usati per trattare la sindrome di Lennox-Gastaut (LGS) includono:
- diarrea
- stanchezza
- vomito
- sonnolenza
- diminuzione dell'appetito
Questi non sono tutti i possibili effetti collaterali della fintepla. Per ulteriori informazioni chiedi al proprio medico o farmacista.
Di 'al tuo operatore sanitario se hai qualche effetto collaterale che ti disturba o che non scompare.
Chiama il medico per consigli medici sugli effetti collaterali. È possibile segnalare gli effetti collaterali alla FDA al numero 1-800-FDA-1088.
Come dovrei conservare la fintepla?
- Conservare la fintepla a temperatura ambiente compresa tra 68 ° F e 77 ° F (20 ° C e 25 ° C).
- Non farlo Refrigerare o congelare.
- Conservare insieme la bottiglia di fintepla e la siringa in un'area pulita.
- Getta via (scartare) qualsiasi fintepla inutilizzata 3 mesi dopo l'apertura della bottiglia o se il scarto dopo la data sulla confezione o sulla bottiglia è passato. Qualunque cosa venga prima.
Mantieni la fintapla e tutti i medicinali fuori dalla portata dei bambini.
Informazioni generali sull'uso sicuro ed efficace di Fintepla.
Le medicine sono talvolta prescritte a fini diversi da quelli elencati in una guida ai farmaci. Non utilizzare Fintepla per una condizione per la quale non è stata prescritta. Non dare fintepla ad altre persone anche se hanno gli stessi sintomi che hai. Potrebbe danneggiare loro.
Puoi chiedere al tuo farmacista o al fornitore di assistenza sanitaria informazioni su Fintepla scritta per gli operatori sanitari.
Quali sono gli ingredienti di Fintepla?
Ingrediente attivo: fenfluramina cloridrato
Ingredienti inattivi: Sapore ciliegia acido citrico etilparaben idrossietilcellulosio metilparaben potassio citrato sucralosio e acqua.
Fintepla contains no ingredient made from gluten-containing grain (wheat barley or rye) E contains not more than 0.1% of carboidrati che proviene dall'aroma di ciliegia.
Questa guida ai farmaci è stata approvata dalla Food and Drug Administration degli Stati Uniti.
Istruzioni per l'uso
Fintepla ®
(Fin-tep-la)
(fenfluramina) soluzione orale 2.2 mg/mL
Assicurati di leggere Comprendi e seguire queste istruzioni prima di iniziare a utilizzare la soluzione orale Fintepla e ogni volta che ottieni una ricarica. Potrebbero esserci nuove informazioni.
Queste istruzioni per l'uso contiene informazioni su come prendere Fintepla. Queste informazioni non prendono il posto di parlare con il proprio operatore sanitario sulla condizione medica o sul trattamento.
Cosa è incluso con Fintepla?
I seguenti elementi sono inclusi per prepararsi e dare una dose orale di fintepla:
- 1 bottiglia di soluzione orale Fintepla (NULL,2 mg/ml)
- 2 siringhe orali riutilizzabili
| |
Chiama il farmacista al numero 1-844-288-5007 se non hai ricevuto gli articoli sopra elencati o se hai bisogno di aiuto per usarli.
Informazioni importanti su Fintepla
- Fintepla is an oral medicine (taken by mouth) E is given 2 volte ogni giorno . Segui le istruzioni per gli operatori sanitari per assumere o dare dosi di fintepla.
- Se hai domande su come preparare o dare fintepla contatta il tuo medico o chiama il tuo farmacista.
- Usa sempre le siringhe orali fornite con fintepla per assicurarsi che venga data la dose giusta. Se hai bisogno di una nuova siringa, contatta il tuo farmacista. Non farlo Usa un cucchiaino o un cucchiaio domestico.
Siringhe orali fornite con fintepla dalla farmacia.
Con Fintepla riceverai 2 siringhe orali riutilizzabili.
2 siringhe orali che possono misurare fino a 3 ml
O
2 siringhe orali che possono misurare fino a 6 ml
| |
Chiama il farmacista al numero 1-844-288-5007 se hai domande sulle siringhe fornite con Fintepla.
Parti della siringa orale
| |
Preparare una dose
Passaggio 1 . Assicurati di avere:
- La bottiglia della soluzione orale di fintepla e
- Una siringa orale riutilizzabile a secco pulito che veniva fornita con fintepla.
Passaggio 2. Controlla lo scarto dopo la data (mm/dd/aaaa).
| |
- Non farlo Usa il medicinale se la data di lancio (scarto) è passata.
- Se la data è vicina, contatta la farmacia o il fornitore di assistenza sanitaria per ottenere una ricarica o una nuova prescrizione.
- Se la data è passata allo smaltimento di fintepla inutilizzata.
Passaggio 3. Premere verso il basso e girare il tappo a prova di bambino a sinistra (in senso antiorario) e rimuoverlo dalla bottiglia.
- Metti da parte il cappuccio (non buttare via).
| |
Passaggio 4. Assicurati che l'adattatore sia sulla bottiglia.
- Se la bottiglia non ha un adattatore contattare il farmacista.
- Lascia sempre l'adattatore in posizione Nella bottiglia della medicina.
| |
Passaggio 5. Rimuovere una siringa orale dalla sua confezione se necessario.
Utilizzare solo le siringhe orali fornite con fintepla.
Se una siringa orale è danneggiata o non è possibile leggere i segni della dose:
- Utilizzare l'altra siringa orale fornita o
- Contatta il farmacista per ottenerne uno nuovo.
| |
Passaggio 6. Assicurati che lo stantuffo sia spinto fino alla siringa orale.
| |
Passaggio 7. Tenere saldamente la bottiglia di medicina su una superficie piana dura.
Passaggio 8. Spingere la punta della siringa orale nell'apertura dell'adattatore fino a quando non può essere spinta ulteriormente.
| |
Passaggio 9. Tieni insieme la siringa orale e il bottiglia e capovolgi.
| |
Passaggio 10. Tirare lentamente lo stantuffo della siringa orale per ritirare la dose prescritta.
| |
| |
| |
Preparazione di una dose (continua)
Passaggio 11. Allinea la fine dello stantuffo con il segno per la dose prescritta sulla siringa orale.
Suggerimenti per ottenere la dose corretta
- Se tiri troppi medicine:
- Lasciare la siringa orale nell'adattatore.
- Spingere lentamente lo stantuffo nella siringa fino a raggiungere la dose prescritta.
- Se vedi bolle d'aria nel medicinale:
- Lasciare la siringa orale nell'adattatore.
- Abbattere lo stantuffo più in basso.
- Consenti alle bolle di salire sulla punta della siringa.
- Spingi lo stantuffo in tutto il mondo.
- Estrarre lentamente lo stantuffo sulla dose prescritta.
Nota: Le bolle molto piccole nel liquido sono normali.
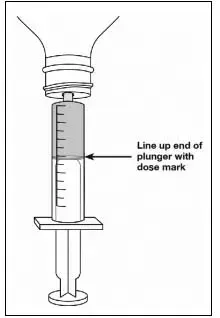
Passaggio 12. Tieni insieme la siringa orale e il bottiglia e quindi girare la bottiglia a destra verso l'alto.
| |
Passaggio 13. Tenendo la bottiglia fermamente estrarre delicatamente la siringa orale dall'adattatore della bottiglia.
| |
Passaggio 14. Assicurarsi che la dose nella siringa orale corrisponda ancora alla dose prescritta.
Se la dose non corrisponde:
- Rimetti la siringa in adattatore.
- Vedere i passaggi da 9 a 11 per regolare la dose secondo necessità.
Dare fintepla
Passaggio 15. Posizionare la punta della siringa orale contro l'interno della guancia.
Passaggio 16. Spingere delicatamente lo stantuffo fino a quando viene data tutta la medicina nella siringa orale.
| |
- Non farlo Spot o spingere con forza la medicina nella parte posteriore della gola. Questo può causare soffocamento.
Passaggio 17. Posizionare il cappuccio sulla bottiglia girando il tappo a destra (in senso orario) fino a quando non si ferma.
- Lascia sempre l'adattatore in posizione in the bottle
- Il cappuccio si adatterà su di esso.
| |
Pulire la siringa
- Sciacquare la siringa orale con acqua di rubinetto pulito e lasciarla asciugare all'aria dopo ogni utilizzo.
- Assicurati di sciacquare l'interno della siringa e dello stantuffo.
Suggerimenti per la pulizia:
- Tirare l'acqua del rubinetto pulito nella siringa con lo stantuffo e spingerla più volte per pulire la siringa.
- Rimuovere lo stantuffo dalla canna della siringa orale
- Risciacqua entrambe le parti sotto l'acqua del rubinetto
- Assicurarsi che la siringa e lo stantuffo siano completamente asciutti prima dell'uso successivo.
- La siringa è anche sicura da pulire nella lavastoviglie.
| |
Come dovrei conservare la fintepla?
- Conservare la fintepla a temperatura ambiente compresa tra 68 ° F e 77 ° F (da 20 ° C a 25 ° C).
- Non farlo Refrigerare o congelare.
- Tieni il tappo stretto e la bottiglia in posizione verticale.
- Conservare insieme la bottiglia di fintepla e la siringa in un'area pulita.
- Getta via (scartare) qualsiasi fintepla inutilizzata 3 mesi dopo l'apertura della bottiglia o se il scarto dopo la data sulla confezione o sulla bottiglia è passato. Qualunque cosa venga prima.
- Mantieni la fintapla e tutti i medicinali fuori dalla portata dei bambini.
Queste istruzioni per l'uso sono state approvate dalla Food and Drug Administration degli Stati Uniti.
