Le Informazioni Presenti Sul Sito Non Costituiscono Consulenza Medica. Non Vendiamo Nulla. L'Accuratezza Della Traduzione Non È Garantita. Disclaimer
Antibiotici, linosamideCleocin IV
Riepilogo della droga
Cos'è Cleocin?
La cleocina (clindamicina) è un antibiotico usato per il trattamento di gravi infezioni causate da batteri anaerobici sensibili. Cleocin è disponibile in forma generica.
Quali sono gli effetti collaterali di Cleocin?
Cleocin IV
- orticaria
- Difficoltà a respirare
- gonfiore della lingua o della gola
- Diarrea persistente
- Dolore addominale
- crampi
- Sangue o muco nelle feci
- dolore o gonfiore nel sito di iniezione
- urina scura
- Ingialcare la pelle o gli occhi (ittero)
- nausea o vomito persistente
- Modifica della quantità di urina
- Facile lividi o lividi
- Dolore articolare
- febbre
- mal di gola persistente
- battito cardiaco rapido lento o irregolare
- svenimento e
- Scrigette gravi
Ottieni subito assistenza medica se hai uno qualsiasi dei sintomi sopra elencati.
Gli effetti collaterali di cleocin includono:
a cosa serve i farmaci lisinopril
- Dolore addominale
- Colite pseudomembrane
- esofagite
- nausea
- vomito
- diarrea
- gusto spiacevole o metallico in bocca (se la cleocina viene iniettata in una vena)
- dolore e gonfiore nel sito di iniezione (se la cleocina viene iniettata in un muscolo)
- Reazioni di ipersensibilità (eruzione cutanea e orticaria)
- prurito
- infezione vaginale e
- Ingiallimento della pelle e degli occhi (ittero).
Di 'al medico se hai gravi effetti collaterali di Cleocin, incluso:
- dolore o gonfiore nel sito di iniezione (se questo farmaco viene iniettato in una vena)
- urina scura
- occhi ingialliti o pelle
- nausea o vomito persistente
- un cambiamento nella quantità di urina
- Facile lividi o sanguinanti
- dolore in diverse articolazioni
- Nuovi segni di infezione (ad es. Dolore persistente alla febbre)
- battito cardiaco rapido/lento/irregolare o
- svenimento.
Cerca cure mediche o chiama il 911 contemporaneamente se hai i seguenti gravi effetti collaterali:
- Sintomi di occhiali gravi come la perdita di visione improvvisa del tunnel della visione sfocata Dolore alla visione o gonfiore o vedere aloni attorno alle luci;
- Sintomi cardiaci gravi come battiti cardiaci irregolari o martellanti veloci; svolazzando nel petto; fiato corto; e improvviso vertigini giuria o svenuta;
- Grave mal di testa confusione Il braccio del linguaggio bloccato o la debolezza delle gambe problemi perdite perdita di coordinamento sentendoti instabili muscoli molto rigidi ad alta febbre abbondante sudorazione o tremori.
Questo documento non contiene tutti i possibili effetti collaterali e altri possono verificarsi. Verificare con il tuo medico ulteriori informazioni sugli effetti collaterali.
Dosaggio per cleocin
La dose raccomandata di cleocina per gli adulti è di 150-450 mg per via orale ogni 6 ore o dosi endovenose di 600-2700 mg al giorno in 2-4 dosi divise.
Quali sostanze o integratori di farmaci interagiscono con la cleocina?
La cleocina può interagire con altri agenti bloccanti neuromuscolari eritromicina e controllo ormonale. Dì al medico tutti i farmaci e gli integratori che usi.
Cleocina durante la gravidanza e l'allattamento
La cleocina non è stata adeguatamente valutata nelle donne in gravidanza. La cleocina dovrebbe essere usata durante la gravidanza solo se è chiaramente necessario. La cleocina passa nel latte materno e potrebbe avere effetti indesiderati su un bambino infermieristico. Consulta il medico prima dell'allattamento al seno.
Ulteriori informazioni
Il nostro centro farmacologico per effetti collaterali Cleocin fornisce una visione completa delle informazioni disponibili sui farmaci sui potenziali effetti collaterali quando si assume questo farmaco.
Informazioni sui farmaci FDA
- Descrizione del farmaco
- Indicazioni
- Dosaggio
- Effetti collaterali
- Interazioni farmacologiche
- Avvertimenti
- Precauzioni
- Overdose
- Farmacologia clinica
- Guida ai farmaci
AVVERTIMENTO
C Lostridium duro -Da diarrea associata (CDAD) è stata riportata con l'uso di quasi tutti gli agenti antibatterici tra cui la cleocina fosfato e può variare in gravità dalla diarrea lieve alla colite fatale. Il trattamento con agenti antibatterici altera la normale flora del colon che porta alla crescita eccessiva di C. difficile .
Poiché la terapia con fosfato di cleocina è stata associata a colite grave che può porre fine a fatalmente, dovrebbe essere riservato a gravi infezioni in cui agenti antimicrobici meno tossici sono inappropriati come descritto nelle indicazioni e nell'uso. Non dovrebbe essere usato in pazienti con infezioni non batteriche come la maggior parte delle infezioni del tratto respiratorio superiore. C. difficile produce tossine A e B che contribuiscono allo sviluppo di CDAD. Ipertoxina che produce ceppi di C. difficile causano un aumento della morbilità e della mortalità poiché queste infezioni possono essere refrattarie alla terapia antimicrobica e possono richiedere colectomia. Il CDAD deve essere considerato in tutti i pazienti che presentano diarrea a seguito di uso antibiotico. È stata necessaria un'attenta storia medica da quando è stato segnalato che il CDAD si verifica in due mesi dopo la somministrazione di agenti antibatterici.
Se il CDAD è sospettato o confermato l'uso di antibiotici in corso non diretto contro C. difficile Potrebbe essere necessario interrompere. Appropriato TRATTAMENTO ANTIbiotico di integrazione di proteine per la gestione dei fluidi ed elettroliti C. difficile e la valutazione chirurgica dovrebbe essere istituita come clinicamente indicata.
Descrizione per Cleocin I.V.
La soluzione sterile di cleocina fosfato in fiale contiene clindamicina fosfato Un estere solubile in acqua di clindamicina e acido fosforico. Ogni ML contiene l'equivalente di 150 mg di clindamicina da 0,5 mg di disodio edetato e 9,45 mg di alcool benzilico aggiunto come conservante in ciascun ml. La clindamicina è un antibiotico semisintetico prodotto da una sostituzione cloro 7 (S) del gruppo 7 (R)-idrossile del composto genitore linomicina.
Il nome chimico della clindamicina fosfato è l- direzione -a.D- Galacto -Octopyranoside metil-7-cloro-678-trideoxy-6-[[(1-metil-4-propil-2-pirrolidinil) carbonil] amino] -1-thio-2- (diidrogeno fosfato) (2S- trans )-.
La formula molecolare è C 18 H 34 Alimentazione 2 0 8 PS e il peso molecolare è 504,96.
La formula strutturale è rappresentata di seguito:
 |
Il fosfato di cleocina nella fiala aggiunta è destinata all'uso endovenoso solo dopo ulteriore diluizione con un volume adeguato di soluzione di base di diluenti aggiunte (Vedere Indicazioni per l'uso ).
La soluzione di cleocina fosfato IV nel contenitore di plastica di galassia per uso endovenoso è composta da clindamicina fosfato equivalente a 300 600 e 900 mg di clindamicina premiscela con destrosio al 5% come soluzione sterile. Il disodio edetato è stato aggiunto ad una concentrazione di 0,04 mg/mL. Il pH è stato regolato con idrossido di sodio e/o acido cloridrico.
Il contenitore di plastica è fabbricato da un multistrato di plastica multistrato appositamente progettato. Soluzioni a contatto con il contenitore di plastica possono lisciviarsi alcune delle sue componenti chimiche in quantità molto ridotte entro il periodo di scadenza. L'idoneità della plastica è stata confermata nei test negli animali secondo i test biologici USP per i contenitori di plastica e da studi di tossicità della coltura dei tessuti.
Usi per Cleocin I.V.
I prodotti cleocin fosfato sono indicati nel trattamento di gravi infezioni causate da batteri anaerobici sensibili.
I prodotti cleocin fosfato sono anche indicati nel trattamento di gravi infezioni a causa di ceppi sensibili di pneumococchi di streptococchi e stafilococchi. Il suo uso dovrebbe essere riservato ai pazienti allergici alla penicillina o ad altri pazienti per i quali nel giudizio del medico una penicillina è inappropriata. A causa del rischio di colite pseudomembranosa associata agli antibiotici come descritto nel Avvertenza in scatola Prima di selezionare la clindamicina, il medico dovrebbe considerare la natura dell'infezione e l'idoneità di alternative meno tossiche (ad es. Eritromicina).
Gli studi batteriologici dovrebbero essere condotti per determinare gli organismi causali e la loro suscettibilità alla clindamicina.
Le procedure chirurgiche indicate dovrebbero essere eseguite in combinazione con terapia antibiotica.
Cleocin fosfato è indicato nel trattamento di gravi infezioni causate da ceppi sensibili degli organismi designati nelle condizioni elencate di seguito:
Infezioni del tratto respiratorio inferiore tra cui la polmonite empiema e l'ascesso polmonare causato da anaerobi Streptococcus pneumoniae Altri streptococchi (tranne E. feecalis ) E Staphylococcus aureus.
Infezioni della struttura della pelle e della pelle causate da Streptococcus pyogenes Staphylococcus aureus e anaerobi.
Infezioni ginecologiche tra cui endometrite non angolate non cellulite pelvica tuboovariale e infezione post-chirurgica della cuffia vaginale causata da anaerobi sensibili.
Infezioni intra-addominali tra cui la peritonite e l'ascesso intra-addominale causato da organismi anaerobici sensibili.
Setticemia causata da Staphylococcus aureus streptococchi (tranne Enterococcus faecalis ) E susceptible anaerobes.
Infezioni ossee e articolari che comprendono l'osteomielite ematogena acuta causata da Staphylococcus aureus e come terapia aggiuntiva nel trattamento chirurgico di osso cronico e infezioni articolari dovute agli organismi sensibili.
Per ridurre lo sviluppo di batteri resistenti ai farmaci e mantenere l'efficacia del fosfato di cleocina e di altri farmaci antibatterici, la cleocina fosfato dovrebbe essere usata solo per trattare o prevenire infezioni provese o fortemente sospettate di essere causate da batteri sensibili. Quando sono disponibili informazioni sulla coltura e sulla suscettibilità, dovrebbero essere considerate nella selezione o nella modifica della terapia antibatterica. In assenza di tali dati di epidemiologia locale e modelli di suscettibilità possono contribuire alla selezione empirica della terapia.
Dosaggio per cleocin I.V.
Se si verifica la diarrea durante la terapia, questo antibiotico dovrebbe essere sospeso (vedi Avvertenza della scatola ).
La somministrazione IM di clindamicina fosfato deve essere usata non diluita.
è cymbalta e ssri o snri
La somministrazione di clindamicina fosfato IV deve essere diluita (Vedere Diluizione per uso IV e velocità di infusione endovenosa sotto).
Adulti
Parenterale (somministrazione IM o IV): gravi infezioni dovute a cocci aerobici gram-positivi e anaerobi più sensibili (non includono generalmente Bacteroides fragilis peptococcus specie e Clostridium specie diverse da Clostridium perfringens )
600.1200 mg/giorno in 2 3 o 4 dosi uguali.
Infezioni più gravi, in particolare quelle dovute a dimostrate o sospettate Bacteroides fragilis peptococcus specie o Clostridium species diverso da Clostridium perfringens:
1200.2700 mg/giorno in 2 3 o 4 dosi uguali.
Per infezioni più gravi, queste dosi potrebbero dover essere aumentate. Nelle situazioni potenzialmente letali dovute ad aerobi o anaerobi, queste dosi possono essere aumentate. Dosi di 4800 mg al giorno sono state somministrate per via endovenosa agli adulti. Vedere Diluizione per uso IV e velocità di infusione endovenosa sezione di seguito.
Non sono raccomandate iniezioni intramuscolari singole superiori a 600 mg.
In alternativa, il farmaco può essere somministrato sotto forma di una singola infusione rapida della prima dose seguita da infusione IV continua come segue:
| Per mantenere i livelli sierici di clindamicina | Tasso di infusione rapida | Tasso di infusione di manutenzione |
| Sopra 4 mcg/ml | 10 mg/min per 30 minuti | 0,75 mg/min |
| Sopra 5 mcg/ml | 15 mg/min per 30 minuti | 1,00 mg/min |
| Sopra 6 mcg/ml | 20 mg/min per 30 minuti | 1,25 mg/min |
Neonati (meno di 1 mese)
15-20 mg/kg/die in 3 a 4 dosi uguali. Il dosaggio inferiore può essere adeguato per le piccole premature.
Pazienti pediatrici da 1 mese a 16 anni
Garenteral (IM o IV) Somministrazione: da 20 a 40 mg/kg/giorno in 3 o 4 dosi uguali. Le dosi più elevate verrebbero utilizzate per infezioni più gravi. In alternativa al dosaggio su base corporeo, i pazienti pediatrici possono essere dosati sulla base della superficie corporea dei metri quadrati: 350 mg/m 2 /giorno per infezioni gravi e 450 mg/m 2 /giorno per infezioni più gravi.
La terapia parenterale può essere cambiata in cleocin pediatricr orale ® Granuli aromatizzati (clindamicina palmitato cloridrato) o cleocin hclr ® Capsule (clindamicina cloridrato) quando la condizione merita e a discrezione del medico.
In caso di infezione da streptococcici β-emolitici, il trattamento deve essere continuato per almeno 10 giorni.
Diluizione per uso IV e velocità di infusione endovenosa: The concentration of clindamycin in diluent for infusion should not exceed 18 mg per mL. Infusion rates should not exceed 30 mg per minute. Le solite diluizioni e tassi di infusione sono i seguenti:
| Dose | Diluente | Tempo |
| 300 mg | 50 ml | 10 min |
| 600 mg | 50 ml | 20 min |
| 900 mg | 50-100 ml | 30 min |
| 1200 mg | 100 ml | 40 min |
La somministrazione di oltre 1200 mg in una singola infusione di 1 ora non è raccomandata.
I prodotti farmaceutici parenterali devono essere ispezionati visivamente per il particolato e lo scolorimento prima della somministrazione ogni volta che la soluzione e il permesso del contenitore.
Diluizione e compatibilità
Gli studi di compatibilità fisica e biologica monitorati per 24 ore a temperatura ambiente non hanno dimostrato inattivazione o incompatibilità con l'uso di una soluzione sterile di cleocina fosfato (clindamicina fosfato) in soluzioni IV contenenti glucosio con cloruro di sodio calcio di glucosio o potassio e soluzioni contenenti il complesso di vitamina B nelle concentrazioni solitamente utilizzate clinicamente. Non è stata dimostrata alcuna incompatibilità con gli antibiotici cefalotina kanamicina per la penicillina o carbenicillina.
I seguenti farmaci sono fisicamente incompatibili con la clindamicina fosfato: l'ampicillina sodico fenitoina sodico barbiturisce l'aminofillina glucinato e il solfato di magnesio.
La compatibilità e la durata della stabilità delle miscele di droga varieranno a seconda della concentrazione e di altre condizioni. Per le informazioni attuali in merito alle compatibilità della clindamicina fosfato in condizioni specifiche, contattare l'unità di informazioni mediche e farmacologiche
Stabilità fisico-chimica di soluzioni diluite di temperatura ambiente fosfato di cleocina
6 9 e 12 mg/mL (equivalente alla base di clindamicina) in iniezione di destrosio iniezione di cloruro di sodio 5% 0,9% o iniezione di suonerie in latta in bottiglie di vetro o minibag ha dimostrato stabilità fisica e chimica per almeno 16 giorni a 25 ° C. Anche 18 mg/mL (equivalente alla base di clindamicina) nell'iniezione di destrosio il 5% in minibag ha dimostrato stabilità fisica e chimica per almeno 16 giorni a 25 ° C.
Refrigerazione
6 9 e 12 mg/mL (equivalente alla base di clindamicina) in iniezione di destrosio iniezione di cloruro di sodio 5% 0,9% o iniezione di suonerie in latta in bottiglie di vetro o minibag ha dimostrato stabilità fisica e chimica per almeno 32 giorni a 4 ° C.
IMPORTANTE: queste informazioni sulla stabilità chimica non indicano in alcun modo che sarebbe una pratica accettabile utilizzare questo prodotto ben dopo il tempo di preparazione. Una buona pratica professionale suggerisce che le miscele composte dovrebbero essere somministrate poco dopo la preparazione possibile.
Congelato
6 9 e 12 mg/mL (equivalente alla base di clindamicina) in iniezione di destrosio iniezione di cloruro di sodio 5% 0,9% o iniezione di suonerie in latta in minibags ha dimostrato stabilità fisica e chimica per almeno otto settimane a -10 ° C.
Congelato solutions should be thawed at room temperature and not refrozen.
Indicazioni per l'erogazione
Pacchetto di blocca della farmacia
Non per infusione diretta
Il pacchetto in blocco della farmacia è da utilizzare in un servizio di miscela di farmacia solo sotto un cappuccio di flusso laminare. L'ingresso nella fiala deve essere effettuato con un set di trasferimento sterile di piccolo diametro o un altro dispositivo di erogazione sterile di piccolo diametro e contenuti distribuiti in aliquote usando la tecnica asettica. Non sono consigliate voci più con ago e siringa. Dopo l'ingresso, usa prontamente l'intero contenuto di Fial. Qualsiasi porzione inutilizzata deve essere scartata entro 24 ore dall'ingresso iniziale.
Indicazioni per l'uso
Soluzione di cleocina fosfato IV nel contenitore di plastica di galassia
La soluzione di cleocina fosfato IV premiscelata è per la somministrazione endovenosa utilizzando apparecchiature sterili. Verificare le perdite minuti prima dell'uso stringendo saldamente la borsa. Se le perdite si trovano una soluzione di scarto poiché la sterilità può essere compromessa. Non aggiungere farmaci supplementari. I prodotti farmaceutici parenterali devono essere ispezionati visivamente per il particolato e lo scolorimento prima della somministrazione ogni volta che la soluzione e il permesso del contenitore. Non utilizzare a meno che la soluzione non sia chiara e il sigillo non sia intatto.
Attenzione
Non utilizzare contenitori di plastica nelle connessioni in serie. Tale uso potrebbe comportare l'embolia d'aria a causa dell'aria residua tratte dal contenitore primario prima che sia completata la somministrazione del fluido dal contenitore secondario.
Preparazione per l'amministrazione
- Sospendere il contenitore dal supporto per gli occhielli.
- Rimuovere il protettore dalla porta di uscita nella parte inferiore del contenitore.
- Set di amministrazione allega. Fare riferimento a indicazioni complete che accompagnano il set.
Preparazione di cleocin fosfato nel sistema aggiuntivo- .Per per l'uso solo. Cleocin fosfato 300 mg 600 mg e 900 mg possono essere ricostituiti in 50 mL (per 300 mg e 600 mg) o 100 mL (per 900 mg) di iniezione di destrosio 5% o iniezione di cloruro di sodio 0,9% nel contenitore aggiuntivo -diluente. Fare riferimento a istruzioni separate per il sistema aggiuntivo.
Come fornito
Ogni ml di Cleocin fosfato La soluzione sterile contiene fosfato di clindamicina equivalente a 150 mg di clindamicina 0,5 mg di disodio edetato 9,45 mg di alcool benzilico aggiunto come conservante. Quando necessario, il pH viene regolato con idrossido di sodio e/o acido cloridrico. Cleocin fosfato è disponibile nei seguenti pacchetti:
Viale da 25-2 ml Ndc 0009-0870-26
25-4 ml fiale Ndc 0009-0775-26
25-6 ml fiale Ndc 0009-0902-18
Pacchetto sfuso della farmacia da 5-60 ml Ndc 0009-0728-09
Cleocin fosfato viene fornito in fiale aggiunte come segue:
| Ndc | Dimensione della fiala | Clindamicina totale fosfato/fiala |
| 0009-6582-01 | Viale da 25-2 ml | 300 mg |
| 0009-3124-03 | 25-4 ml fiale | 600 mg |
| 0009-3447-03 | 25-6 ml fiale | 900 mg |
Conservare a temperatura ambiente controllata da 20 ° a 25 ° C (da 68 ° a 77 ° F) [vedi USP].
Cleocin fosfato IV Solution Nei contenitori in plastica di galassia è una soluzione sterile di clindamicina fosfato con destrosio al 5%. I contenitori di plastica a dose singola dose sono disponibili come segue:
24-300 mg/50 ml contenitori Ndc 0009-3381-02
24-600 mg/50 ml contenitori Ndc 0009-3375-02
24-900 mg/50 ml di contenitori Ndc 0009-3382-02
L'esposizione dei prodotti farmaceutici al calore dovrebbe essere ridotta al minimo. Si consiglia di conservare i contenitori di plastica di galassia a temperatura ambiente (25 ° C). Evitare temperature superiori a 30 ° C.
Distribuito da: Pfizer Pharmacia
Effetti collaterali for Cleocin I.V.
Sono state riportate le seguenti reazioni con l'uso della clindamicina.
Infezioni e infestazioni: Clostridium difficile colite
Gastrointestinale: Colite associata agli antibiotici (vedi AVVERTIMENTOS ) Nausea e vomito addominale pseudomembrane. L'inizio dei sintomi di colite pseudomembrana possono verificarsi durante o dopo il trattamento antibatterico (vedi AVVERTIMENTOS ). An unpleasant or metallic taste has been reported after intravenous administration of the higher doses of clindamycin phosphate.
Reazioni di ipersensibilità: Durante la terapia farmacologica sono state osservate eruzioni maculopapolari e orticaria. Le eruzioni cutanei da lieve a moderata generalizzate a morbilliforme sono le più frequentemente riportate di tutte le reazioni avverse.
Sono state riportate reazioni cutanee gravi come la necrolisi epidermica tossica alcune con esito fatale (vedi AVVERTIMENTOS ). Cases of Acute Generaleized Exanthematous Pustulosis (AGEP) erythema multiforme some resembling Stevens-Johnson syndrome have been associated with clindamycin. Anaphylactic shock anaphylactic reaction and hypersensitivity have also been reported (Vedere AVVERTIMENTOS ).
Pelle e mucose: Sono stati segnalati angoedema vaginite da prurito e rari casi di dermatite esfoliativa (vedi Reazioni di ipersensibilità ).
Fegato: L'ittero e le anomalie nei test di funzionalità epatica sono stati osservati durante la terapia con clindamicina.
Renale: Sebbene non sia stata osservata alcuna relazione diretta di clindamicina e danno renale, come evidenziato dall'azotemia oliguria e/o dalla proteinuria.
Ematopoietico: Sono stati segnalati neutropenia transitoria (leucopenia) ed eosinofilia. Sono state presentate segnalazioni di agranulocitosi e trombocitopenia. Nessuna relazione eziologica diretta con la terapia clindamicina concomitante potrebbe essere fatta in nessuno dei precedenti.
Sistema immunitario: Sono state riportate reazioni farmacologiche con eosinofilia e sintomi sistemici (abiti).
Reazioni locali: Sito di iniezione L'irritazione del dolore è stata riportata dopo l'iniezione intramuscolare e la tromboflebite intramuscolare dopo infusione endovenosa. Le reazioni possono essere minimizzate o evitate fornendo iniezioni intramuscolari profonde ed evitando l'uso prolungato di cateteri endovenosi permanenti.
Muscoloscheletrico: Sono stati riportati casi di poliartrosi.
Cardiovascolare: Sono stati segnalati arresti cardiopolmoni e ipotensione a seguito di una somministrazione endovenosa troppo rapida (vedi Dosaggio e amministrazione ).
Interazioni farmacologiche for Cleocin I.V.
È stato dimostrato che la clindamicina ha proprietà di blocco neuromuscolare che possono migliorare l'azione di altri agenti bloccanti neuromuscolari. Pertanto dovrebbe essere usato con cautela nei pazienti che ricevono tali agenti.
itinerario san franco
La clindamicina viene metabolizzata prevalentemente dal CYP3A4 e, in misura minore, dal CYP3A5 al principale metabolita clindamicina solfossido e minore metabolita N-desmetilcindamicina. Pertanto gli inibitori di CYP3A4 e CYP3A5 possono aumentare le concentrazioni plasmatiche di clindamicina e induttori di questi isoenzimi possono ridurre le concentrazioni plasmatiche di clindamicina. In presenza di forti inibitori del CYP3A4 monitorano le reazioni avverse. In presenza di forti induttori del CYP3A4 come la rifampicina monitor per la perdita di efficacia.
In vitro Gli studi indicano che la clindamicina non inibisce il CYP1A2 CYP2C9 CYP2C19 CYP2E1 o CYP2D6 e inibisce solo moderatamente CYP3A4.
L'antagonismo è stato dimostrato tra clindamicina ed eritromicina in vitro . A causa del possibile significato clinico, i due farmaci non dovrebbero essere somministrati contemporaneamente.
Avvertimenti for Cleocin I.V.
Vedere Avvertenza della scatola .
Clostridium Difficile Associated Diarrhea
Clostridium difficile La diarrea associata (CDAD) è stata riportata con l'uso di quasi tutti gli agenti antibatterici tra cui la cleocina fosfato e può variare in gravità dalla diarrea lieve alla colite fatale. Il trattamento con agenti antibatterici altera la normale flora del colon che porta alla crescita eccessiva di C. difficile .
C. difficile produce tossine A e B che contribuiscono allo sviluppo di CDAD. Ipertoxina che produce ceppi di C. difficile causano un aumento della morbilità e della mortalità poiché queste infezioni possono essere refrattarie alla terapia antimicrobica e possono richiedere colectomia. Il CDAD deve essere considerato in tutti i pazienti che presentano diarrea a seguito di uso antibiotico. È stata necessaria un'attenta storia medica da quando è stato segnalato che il CDAD si verifica in due mesi dopo la somministrazione di agenti antibatterici.
Se il CDAD è sospettato o confermato l'uso di antibiotici in corso non diretto contro C. difficile Potrebbe essere necessario interrompere. Appropriato TRATTAMENTO ANTIbiotico di integrazione di proteine per la gestione dei fluidi ed elettroliti C. difficile e la valutazione chirurgica dovrebbe essere istituita come clinicamente indicata.
Reazioni di ipersensibilità anafilattica e grave
Sono state riportate reazioni anafilattiche e anafilattiche (vedi Reazioni avverse ).
Reazioni di ipersensibilità gravi tra cui reazioni cutanee gravi come la necrolisi epidermica tossica (dieci) Reazione farmaco Reazioni avverse ).
In caso di una tale reazione di ipersensibilità anafilattica o grave interrompere permanentemente il trattamento e istituire una terapia appropriata.
Un'attenta indagine dovrebbe essere fatta riguardo alle precedenti sensibilità ai farmaci e ad altri allergeni.
Tossicità da alcol benzilico nei pazienti pediatrici (sindrome ansimante)
Questo prodotto contiene alcol benzilico come conservante. L'alcool benzilico conservante è stato associato a gravi eventi avversi tra cui la sindrome di GGASPING e la morte nei pazienti pediatrici. Sebbene le normali dosi terapeutiche di questo prodotto offrano normalmente quantità di alcol benzilico che sono sostanzialmente inferiori a quelle riportate in associazione con la sindrome di Asping, non è nota la quantità minima di alcool benzilico in cui la tossicità non può verificarsi.
Il rischio di tossicità da alcol benzilico dipende dalla quantità somministrata e dalla capacità del fegato e dei reni di disintossicare la sostanza chimica. I neonati prematuri e a basso peso alla nascita possono avere maggiori probabilità di sviluppare tossicità.
Utilizzo nella meningite
Poiché la clindamicina non si diffonde adeguatamente nel liquido cerebrospinale, il farmaco non dovrebbe essere usato nel trattamento della meningite.
Precauzioni for Cleocin I.V.
Generale
La revisione dell'esperienza fino ad oggi suggerisce che un sottogruppo di pazienti più anziani con malattia grave associata può tollerare la diarrea meno bene. Quando la clindamicina è indicata in questi pazienti, dovrebbero essere attentamente monitorati per il cambiamento nella frequenza intestinale.
Cleocin fosfato products should be prescribed with caution in individuals with a history of gastrointestinal disease particularly colite.
Cleocin fosfato should be prescribed with caution in atopic individuals.
Alcune infezioni possono richiedere incisione e drenaggio o altre procedure chirurgiche indicate oltre alla terapia antibiotica.
L'uso del fosfato di cleocina può provocare una crescita eccessiva di organismi non sensibili-particolari. Se si verificano superinfezioni, le misure appropriate dovrebbero essere prese come indicato dalla situazione clinica.
Cleocin fosfato should not be injected intravenously undiluted as a bolus but should be infused over at least 10-60 minutes as directed in the Dosaggio e amministrazione sezione.
La modifica del dosaggio di clindamicina potrebbe non essere necessaria nei pazienti con malattia renale. Nei pazienti con il prolungamento della malattia epatica da moderata a grave è stata trovata l'emivita di clindamicina. Tuttavia, è stato postulato da studi che quando si è verificato ogni otto ore di accumulo di raramente. Pertanto potrebbe non essere necessaria la modifica del dosaggio nei pazienti con malattia epatica. Tuttavia, si devono prendere determinazioni periodiche degli enzimi epatici durante il trattamento dei pazienti con grave malattia epatica.
È improbabile che prescrivere cleocin fosfato in assenza di un'infezione batterica comprovata o fortemente sospetta o un'indicazione profilattica fornisce benefici al paziente e aumenta il rischio di sviluppo di batteri resistenti ai farmaci.
Informazioni per i pazienti
I pazienti devono essere consigliati che i farmaci antibatterici tra cui la cleocina fosfato dovrebbero essere usati solo per trattare le infezioni batteriche. Non trattano le infezioni virali (ad esempio il raffreddore comune). Quando viene prescritto la cleocina fosfato per trattare, i pazienti con infezione batterica dovrebbero essere detto che sebbene sia comune sentirsi meglio nelle prime fasi della terapia, il farmaco dovrebbe essere assunto esattamente come indicato. Saltare le dosi o non completare l'intero corso della terapia può (1) ridurre l'efficacia del trattamento immediato e (2) aumentare la probabilità che i batteri sviluppino resistenza e non saranno curabili da cleocina fosfato o altri farmaci antibatterici in futuro.
La diarrea è un problema comune causato dagli antibiotici che di solito termina quando l'antibiotico viene interrotto. A volte dopo aver iniziato il trattamento con i pazienti con antibiotici possono sviluppare feci acquose e sanguinanti (con o senza crampi di stomaco e febbre) anche fino a due o più mesi dopo aver preso l'ultima dose dell'antibiotico. Se ciò si verifica, i pazienti devono contattare il proprio medico il più presto possibile.
Test di laboratorio
Durante la terapia prolungata dovrebbe essere eseguita test e contazioni ematiche periodiche e conteggi ematici.
Mutagenesi della carcinogenesi compromissione della fertilità
Studi a lungo termine sugli animali non sono stati condotti con clindamicina per valutare il potenziale cancerogeno. I test di genotossicità eseguiti includevano un test di micronucleo di ratto e un test di inversione di Salmonella Ames. Entrambi i test erano negativi.
Studi sulla fertilità nei ratti trattati per via orale con fino a 300 mg/kg/giorno (circa 1,1 volte la dose umana adulta più alta basata su mg/m 2 ) non ha rivelato effetti sulla fertilità o sull'abilità di accoppiamento.
Gravidanza
Effetti teratogeni
Negli studi clinici con donne in gravidanza la somministrazione sistemica di clindamicina durante il secondo e il terzo trimestre non è stata associata ad una maggiore frequenza di anomalie congenite.
La clindamicina dovrebbe essere usata durante il primo trimestre di gravidanza solo se chiaramente necessario. Non ci sono studi adeguati e ben controllati nelle donne in gravidanza durante il primo trimestre di gravidanza. Poiché gli studi sulla riproduzione degli animali non sono sempre predittivi della risposta umana, questo farmaco dovrebbe essere usato durante la gravidanza solo se chiaramente necessario.
Studi di riproduzione condotti su ratti e topi utilizzando dosi orali di clindamicina fino a 600 mg/kg/giorno (NULL,1 e 1,1 volte la dose umana adulta più consigliata basata su mg/m 2 Rispettiva 2 rispettivamente) non ha rivelato alcuna prova di teratogenicità.
Cleocin fosfato Sterile Solution contains benzyl alcohol. Benzyl alcohol can cross the placenta. see AVVERTIMENTOS .
Madri infermieristiche
È stato segnalato che la clindamicina appare nel latte materno nell'intervallo da 0,7 a 3,8 mcg/mL a dosaggi di 150 mg per via orale a 600 mg per via endovenosa. La clindamicina ha il potenziale per causare effetti avversi sulla flora gastrointestinale del bambino allattato al seno. Se la clindamicina orale o endovenosa è richiesta da una madre infermieristica, non è un motivo per interrompere l'allattamento al seno, ma si può preferire un farmaco alternativo. Monitorare il bambino per possibili effetti avversi sulla flora gastrointestinale come la diarrea candidosi (eruzione cutanea del pannolino di mughetto) o raramente il sangue nelle feci che indica una possibile colite associata agli antibiotici.
I benefici per lo sviluppo e la salute dell'allattamento dovrebbero essere considerati insieme alla necessità clinica della madre di clindamicina e a potenziali effetti avversi sul bambino allattato al seno dalla clindamicina o dalla condizione materna sottostante.
Brasov
Uso pediatrico
Quando la soluzione sterile di cleocina fosfato viene somministrata alla popolazione pediatrica (nascita a 16 anni) è auspicabile il monitoraggio appropriato delle funzioni del sistema di organi.
Utilizzo nei neonati e nei bambini
Questo prodotto contiene alcol benzilico come conservante. L'alcool benzilico è stato associato a una fatale sindrome ansimante nei neonati prematuri. Vedere AVVERTIMENTOS .
Non è stato valutato il potenziale per l'effetto tossico nella popolazione pediatrica da sostanze chimiche che possono lisciviazione dalla preparazione IV premiscelata a dose singola in plastica. Vedere AVVERTIMENTOS .
Uso geriatrico
Gli studi clinici sulla clindamicina non includevano un numero sufficiente di pazienti di età pari o superiore a 65 anni per determinare se rispondono in modo diverso dai pazienti più giovani. Tuttavia, altra esperienza clinica segnalata indica che la colite e la diarrea associate agli antibiotici (a causa di Clostridium difficile ) visto in associazione con la maggior parte degli antibiotici si verificano più frequentemente negli anziani (> 60 anni) e può essere più grave. Questi pazienti devono essere attentamente monitorati per lo sviluppo della diarrea.
Studi di farmacocinetica con clindamicina non hanno mostrato differenze clinicamente importanti tra soggetti giovani e anziani con normale funzione epatica e funzione renale normale (aggiustata per età) dopo somministrazione orale o endovenosa.
Informazioni per overdose per Cleocin I.V.
Una mortalità significativa è stata osservata nei topi a una dose endovenosa di 855 mg/kg e nei ratti a una dose orale o sottocutanea di circa 2618 mg/kg. Nei topi convulsioni e depressione sono state osservate.
L'emodialisi e la dialisi peritoneale non sono efficaci nel rimuovere la clindamicina dal siero.
Controindicazioni per Cleocin I.V.
Questo farmaco è controindicato negli individui con una storia di ipersensibilità ai preparazioni contenenti clindamicina o linomicina.
Farmacologia clinica for Cleocin I.V.
Distribuzione
La clindamicina biologicamente inattiva il fosfato viene convertito in clindamicina attiva. Alla fine dei livelli sierici di clindamicina attiva di clindamicina attivo di infusione endovenosa a breve termine.
Dopo l'iniezione intramuscolare di clindamicina fosfato i livelli di picco di clindamicina attiva sono raggiunti entro 3 ore negli adulti e 1 ora in pazienti pediatrici. Le curve a livello sierico possono essere costruite dai livelli sierici di picco IV come indicato nella Tabella 1 mediante l'applicazione di emivite di eliminazione (vedi Escrezione ).
I livelli sierici di clindamicina possono essere mantenuti sopra il in vitro Concentrazioni minime inibitorie per la maggior parte degli organismi indicati mediante somministrazione di clindamicina fosfato ogni 8-12 ore negli adulti e ogni 6-8 ore in pazienti pediatrici o mediante infusione endovenosa continua. Uno stato di equilibrio è raggiunto dalla terza dose.
Non sono raggiunti livelli significativi di clindamicina nel liquido cerebrospinale anche in presenza di meningi infiammati.
Metabolismo
In vitro Studi sui microsomi epatici e intestinali umani hanno indicato che la clindamicina è prevalentemente metabolizzata dal citocromo P450 3A4 (CYP3A4) con un contributo minore del CYP3A5 per formare clindamicina solfossido e un minore metabolite N-desmetilclindamicina.
Escrezione
La clindamicina biologicamente inattiva fosfato scompare rapidamente dal siero; L'emivita media di eliminazione è di 6 minuti; Tuttavia, l'emivita di eliminazione sierica della clindamicina attiva è di circa 3 ore negli adulti e 2 ore in pazienti pediatrici.
Popolazioni speciali
Compromissione renale/epatica
L'emivita di eliminazione della clindamicina è leggermente aumentata nei pazienti con funzione renale o epatica marcatamente ridotta. L'emodialisi e la dialisi peritoneale non sono efficaci nel rimuovere la clindamicina dal siero. I programmi di dosaggio non devono essere modificati in presenza di una malattia renale o epatica lieve o moderata.
Usa negli anziani
Studi di farmacocinetica nei volontari anziani (61-79 anni) e negli adulti più giovani (18-39 anni) indicano che l'età da sola non altera la clindamicina farmacocinetica (volume di emivita di emittenza di clearance di distribuzione e area sotto la curva del tempo di concentrazione del siero) dopo la somministrazione di Iv della clindamicina. Dopo la somministrazione orale di emivita di eliminazione dell'idrocloruro di clindamicina viene aumentata a circa 4,0 ore (intervallo 3,4-5,1 h) negli anziani rispetto a 3,2 ore (intervallo 2,1-4,2 h) negli adulti più giovani. L'entità dell'assorbimento non è tuttavia diversa tra le fasce di età e non è necessaria alcuna alterazione del dosaggio per gli anziani con normale funzione epatica e funzione renale normale (aggiustata per età) 1 .
I test sierici per la clindamicina attiva richiedono un inibitore per prevenire in vitro Idrolisi della clindamicina fosfato.
Tabella 1. Concentrazioni sieriche di picco e depressione di clindamicina attiva dopo dosaggio con clindamicina fosfato
| Dosaggio Regimen | Picco McG/ml | Trogolo McG/ml |
| Maschi adulti sani (post equilibrio) | ||
| 10.9 | 2.0 | |
| 10.8 | 1.1 | |
| 14.1 | 1.7 | |
| 9 | ||
| Pazienti pediatrici (prima dose)* | ||
| 5-7 mg/kg IV in 1 hour | 10 | |
| 5-7 mg/kg IM | 8 | |
| 3-5 mg/kg IM | 4 | |
| *Dati in questo gruppo da pazienti trattati per l'infezione. |
Microbiologia
Meccanismo d'azione
La clindamicina inibisce la sintesi della proteina batterica legandosi all'RNA 23S della subunità anni '50 del ribosoma. La clindamicina è batteriostatica.
La resistenza alla resistenza alla clindamicina è spesso causata dalla modifica di basi specifiche dell'RNA ribosomiale 23S. La resistenza incrociata tra clindamicina e linomicina è completa. Poiché i siti di legame per questi farmaci antibatterici si sovrappongono a resistenza incrociata tra i macrolidi delle linosamidi e la streptogramma di b.-macrolide-inducibile alla resistenza alla clindamicina si verifica in alcuni isolati di batteri resistenti al macrolide. Gli isolati resistenti ai macrolidi di stafilococchi e streptococchi beta-emolitici devono essere sottoposti a screening per l'induzione della resistenza alla clindamicina usando il test della zona D.
Attività antimicrobica
La clindamicina ha dimostrato di essere attiva contro la maggior parte degli isolati dei seguenti microrganismi in vitro e nelle infezioni cliniche come descritto in Indicazioni e utilizzo sezione.
Batteri gram-positivi
Staphylococcus aureus (ceppi sensibili alla meticillina)
Streptococcus pneumoniae (ceppi sensibili alla penicillina)
Streptococcus pyogenes
Batteri anaerobici
Clostridium perfringens
FUSOBACTERIM NECROPHORUM
Fusobacterium nucleatum
Peptostreptococcus anaerobius
Prevotella melaninogenica
Almeno il 90% dei microrganismi elencati di seguito in vitro Concentrazioni inibitorie minime (MIC) inferiori o uguali al punto di interruzione del MIC sensibile alla clindamicina per organismi di un tipo simile a quelli mostrati nella Tabella 2. Tuttavia, l'efficacia della clindamicina nel trattamento delle infezioni cliniche a causa di questi microrganismi non è stata stabilita in adeguate e ben controllate studi clinici.
Batteri gram-positivi
Staphylococcus epidermidis (ceppi sensibili alla meticillina)
Streptococcus agalactiae
Streptococcus gocciolante
Streptococcus lieve
Streptococcus orale
Batteri anaerobici
Actinomyces israelii
Clostridium clostridioforme
Eggerthella lenta
Finegoldia (peptostreptococcus) grande
Micromonas (peptostreptococcus) micros
Prevotella Bivia
Prevetella intermedia
Propionibacterium acnes
Metodi di test di suscettibilità
Se disponibile, il laboratorio di microbiologia clinica dovrebbe fornire cumulativo in vitro Risultati dei test di suscettibilità per i farmaci antimicrobici utilizzati negli ospedali locali e le aree di pratica del medico come rapporti periodici che descrivono il profilo di suscettibilità dei patogeni consumati e acquisiti dalla comunità. Questi rapporti dovrebbero aiutare il medico a selezionare un farmaco antibatterico per il trattamento.
Tecniche di diluizione
I metodi quantitativi vengono utilizzati per determinare le concentrazioni minime inibitorie antimicrobiche (MIC). Questi microfoni forniscono stime della suscettibilità dei batteri ai composti antimicrobici. I microfoni devono essere determinati utilizzando un metodo di prova standardizzato 23 (brodo e/o agar). I valori MIC devono essere interpretati in base ai criteri forniti nella Tabella 2.
Diffusione tecnica
I metodi quantitativi che richiedono la misurazione dei diametri delle zone possono anche fornire stime riproducibili della suscettibilità dei batteri ai composti antimicrobici. La dimensione della zona deve essere determinata utilizzando un metodo standardizzato 25 . Questa procedura utilizza dischi di carta impregnati di 2 mcg di clindamicina per testare la suscettibilità dei batteri alla clindamicina. I punti di interruzione della diffusione del disco sono forniti nella Tabella 2.
Tecniche anaerobiche
Per i batteri anaerobici la suscettibilità alla clindamicina può essere determinata con un metodo di prova standardizzato 24 . I valori MIC ottenuti devono essere interpretati in base ai criteri forniti nella Tabella 2.
Tabella 2. Criteri interpretativi del test di suscettibilità per la clindamicina
| Patogeno | Criteri interpretativi di suscettibilità | |||||
| Concentrazioni inibitorie minime (Microfono in MCG/mL) | Diffusione del disco (Diametri di zona in mm) | |||||
| S | I | R | S | I | R | |
| Staphylococcus spp. | ≤0,5 | 1-2 | ≥4 | ≥21 | 15–20 | ≤14 |
| Streptococcus pneumoniae e altro Streptococco spp. | ≤0,25 | 0.5 | ≥1 | ≥19 | 16–18 | ≤15 |
| Batteri anaerobici | ≤2 | 4 | ≥8 | N / a | N / a | N / a |
| N / a=not applicable |
Un rapporto di Suscettibile (S) Indica che è probabile che il farmaco antimicrobico inibisca la crescita del patogeno se il farmaco antimicrobico raggiunge la concentrazione di solito raggiungibile nel sito di infezione. Un rapporto di Intermedio (i) indica che il risultato dovrebbe essere considerato equivoco e se il microrganismo non è completamente suscettibile ai farmaci clinicamente fattibili alternativi, il test dovrebbe essere ripetuto. Questa categoria implica una possibile applicabilità clinica nei siti del corpo in cui il farmaco è concentrato fisiologicamente o in situazioni in cui è possibile utilizzare un elevato dosaggio di farmaco. Questa categoria fornisce anche una zona tampone che impedisce a piccoli fattori tecnici incontrollati di causare gravi discrepanze nell'interpretazione. Un rapporto di Resistente (R) indica che il farmaco antimicrobico non è probabile che inibisca la crescita del patogeno se il farmaco antimicrobico raggiunge la concentrazione di solito raggiungibile nel sito di infezione; Altra terapia dovrebbe essere selezionata.
Controllo di qualità
Le procedure di test di suscettibilità standardizzate richiedono l'uso di controlli di laboratorio per monitorare e garantire l'accuratezza e la precisione delle forniture e dei reagenti utilizzati nel test e le tecniche delle persone che eseguono il test 2345 . La polvere di clindamicina standard dovrebbe fornire gli intervalli di microfono nella Tabella 3. Per la tecnica di diffusione del disco utilizzando il disco di clindamicina da 2 mcg I criteri forniti nella Tabella 2 dovrebbero essere raggiunti.
Tabella 3. Intervalli di controllo di qualità accettabili per la clindamicina
| Ceppo QC | Intervalli di controllo di qualità accettabili | |
| Intervallo di concentrazione inibitoria minima (MCG/ML) | Diffusione del disco Range (Diametri di zona in mm) | |
| Enterococcus faecalis 1 ATCC 29212 | 4-16 | N / a |
| Staphylococcus aureus ATCC 29213 | 06-0.25 | N / a |
| Staphylococcus aureus ATCC 25923 | N / a | 24-30 |
| Streptococcus pneumoniae ATCC 49619 | 0,03-0,12 | 19-25 |
| Bacteroides fragilis ATCC 25285 | 0,5-2 | N / a |
| Bacteroides thetaiotaomicron ATCC 29741 | 2-8 | N / a |
| Clostridium difficile 2 ATCC 700057 | 2-8 | N / a |
| Eggerthella lenta ATCC 43055 | 06-0.25 | N / a |
| 1. Enterococcus faecalis è stato incluso in questa tabella solo a scopo di controllo di qualità. 2. Controllo di qualità per C. difficile viene eseguito utilizzando il metodo di diluizione dell'agar Solo tutti gli altri anaerobi obbligatori possono essere testati mediante microdiluizione del brodo o metodi di diluizione dell'agar. N / a=Not applicable ATCC ® è un marchio registrato dell'American Type Culture Collection |
Riferimenti
1. Smith RB Phillips JP: valutazione di Cleocin HCl e Cleocin fosfato in una popolazione anziana. Upjohn TR 8147-82-9122-021 dicembre 1982.
2. Clsi. Standard di prestazione per test di suscettibilità antimicrobica: 26 th ed. Supplemento CLSI M100S. Wayne PA: Istituto di standard clinici e di laboratorio; 2016.
3. Clsi. Metodi per la diluizione test di suscettibilità antimicrobica per i batteri che crescono aerobicamente; Standard approvato -Tente edizione. Documento CLSI M07-A10. Wayne PA: Istituto di standard clinici e di laboratorio; 2015.
4. Clsi. Metodi per test di suscettibilità antimicrobica di batteri anaerobici; Edizione standard-ottava approvata. Documento CLSI M11-A8. Wayne PA: Istituto di standard clinici e di laboratorio; 2012.
5. Clsi. Standard di prestazione per test di suscettibilità al disco antimicrobico; Edizione standard approvata -Twelfth. Documento CLSI M02-A12. Wayne PA: Istituto di standard clinici e di laboratorio; 2015.
Informazioni sul paziente per Cleocin I.V.
I pazienti devono essere consigliati che i farmaci antibatterici tra cui la cleocina fosfato dovrebbero essere usati solo per trattare le infezioni batteriche. Non trattano le infezioni virali (ad esempio il raffreddore comune). Quando viene prescritto la cleocina fosfato per trattare, i pazienti con infezione batterica dovrebbero essere detto che sebbene sia comune sentirsi meglio nelle prime fasi della terapia, il farmaco dovrebbe essere assunto esattamente come indicato. Saltare le dosi o non completare l'intero corso della terapia può (1) ridurre l'efficacia del trattamento immediato e (2) aumentare la probabilità che i batteri sviluppino resistenza e non saranno curabili da cleocina fosfato o altri farmaci antibatterici in futuro.
La diarrea è un problema comune causato dagli antibiotici che di solito termina quando l'antibiotico viene interrotto. A volte dopo aver iniziato il trattamento con i pazienti con antibiotici possono sviluppare feci acquose e sanguinanti (con o senza crampi di stomaco e febbre) anche fino a due o più mesi dopo aver preso l'ultima dose dell'antibiotico. Se ciò si verifica, i pazienti devono contattare il proprio medico il più presto possibile.
Istruzioni per l'uso per il sistema aggiuntivo.
Cleocin fosfato ®
Soluzione sterile di clindamicina per iniezione USP
in aggiunta ® Fial
Per aprire il contenitore diluente:
Scorciare il sovravamplare dall'angolo e rimuovere il contenitore. È possibile osservare una certa opacità della plastica dovuta all'assorbimento dell'umidità durante il processo di sterilizzazione. Questo è normale e non influisce sulla qualità della soluzione o sulla sicurezza. L'opacità diminuirà gradualmente.
Passa da Zoloft a Effexor XR
Per assemblare il contenitore di diluenti Fial e flessibile:
(Usa la tecnica asettica)
- Rimuovere i coperchi protettivi dalla parte superiore della fiala e la porta della fiala sul contenitore diluente come segue:
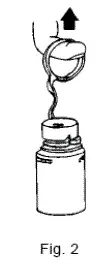
- Per rimuovere il cappuccio per fiala in fuga, oscillare l'anello di tiro sopra la parte superiore della fiala e tirare abbastanza lontano da iniziare l'apertura (vedere la Figura 1.), quindi tirare verso l'alto per rimuovere il tappo. (Vedi Figura 2.) NOTA: Una volta rimosso il cappuccio in fuga Non accedere alla fiala con la siringa.
- Per rimuovere il coperchio della porta della fiala afferrare la linguetta sull'anello di tiro verso l'alto per rompere le tre corde di cravatta, quindi tirare indietro per rimuovere il coperchio. (Vedi Figura 3.)

- Avvitare la fiala nella porta della fiala fino a quando non andrà più lontano. La fiala deve essere avvitata saldamente per garantire un sigillo. Ciò si verifica circa 1/2 turno (180 °) dopo il primo clic udibile. (Vedi Figura 4.) Il suono di clic non assicura un sigillo; La fiala deve essere girata fino in fondo. NOTA: Una volta che la fiala è seduta, non tentare di rimuoverla. (Vedi Figura 4.)
- Riconnettere la fiala per assicurarsi che sia stretto cercando di girarlo ulteriormente nella direzione dell'assemblaggio.
- Etichetta in modo appropriato.
 |
 |
Per preparare la miscela:
- Spremi delicatamente il fondo del contenitore diluente per gonfiare la porzione del contenitore che circonda l'estremità della fiala del farmaco.
- Con l'altra mano spingere la fiala di droga verso il basso nel contenitore che telescopi le pareti del contenitore. Afferrare il cappuccio interno della fiala attraverso le pareti del contenitore. (Vedi Figura 5.)
- Tirare il cappuccio interno dalla fiala di droga. (Vedi Figura 6.) Verificare che il tappo di gomma sia stato estratto permettendo al farmaco e al diluente di mescolare.
- Mescolare accuratamente il contenuto del contenitore e utilizzare entro il tempo specificato.
 |
 |
Preparazione per l'amministrazione: (Usa la tecnica asettica)
- Conferma l'attivazione e la miscela del contenuto di fiala.
- Verificare la presenza di perdite stringendo saldamente il contenitore. Se le perdite si trovano unità di scarto poiché la sterilità può essere compromessa.
- Closed Flow Control Bramp del set di somministrazione.
- Rimuovere il coperchio dalla porta di uscita nella parte inferiore del contenitore.
- Inserire il perforazione del perforazione dell'amministrazione impostata nella porta con un movimento di torsione fino a quando il perno è saldamente seduto. Nota: vedere le indicazioni complete sul cartone del set di amministrazione.
- Sollevare l'estremità libera del gancio sul fondo della fiala rompendo le due corde di cravatta. Piegare il ciclo verso l'esterno per bloccarlo in posizione verticale, quindi sospendere il contenitore dal gancio.
- Spremi e rilasciare la camera di gocciolamento per stabilire un livello di fluido adeguato in camera.
- Brampa di controllo a flusso aperto e aria trasparente dal set. Close morsetto.
- Collegamento set sul dispositivo venipuntura. Se il dispositivo non è PRIME permanente e crea venipuntura.
- Regolare il tasso di somministrazione con un morsetto di controllo del flusso.
AVVERTIMENTO: Do not use flexible container in series connections.


