Le Informazioni Presenti Sul Sito Non Costituiscono Consulenza Medica. Non Vendiamo Nulla. L'Accuratezza Della Traduzione Non È Garantita. Disclaimer
Derivati ErgotVerità
Riepilogo della droga
Cos'è Trudhesa?
Lo spray nasale di Trudhesa (diidroergotamina mesilato) è un derivato ergotamina usato per trattare l'emicrania con o senza aura negli adulti.
Quali sono gli effetti collaterali di Trudhesa?
Verità
- orticaria
- Difficoltà a respirare
- gonfiore della lingua o della gola
- battito cardiaco lento o veloce
- debolezza nelle gambe
- Dolore muscolare tra le braccia o le gambe
- formicolio o intorpidimento
- freddezza nelle mani e nei piedi
- dita blu e dita dei piedi
- forte mal di stomaco
- Mancella o dolore al braccio sinistro
- Dolore o pressione al torace
- Stanchezza improvvisa
- debolezza da un lato del corpo
- difficoltà a parlare
- Cambiamenti della visione
- Cambiamenti mentali o dell'umore
- confusione
- eruzione cutanea
- prurito e
- Scrigette gravi
Ottieni subito assistenza medica se hai uno qualsiasi dei sintomi sopra elencati.
Gli effetti collaterali di Trudhesa includono:
- rinorrea
- nausea
- alterato senso di gusto
- Reazioni del sito dell'applicazione
- vertigini
- vomito
- sonnolenza
- mal di gola E
- diarrea.
Cerca cure mediche o chiama il 911 contemporaneamente se hai i seguenti gravi effetti collaterali:
- Sintomi di occhiali gravi come la perdita di visione improvvisa del tunnel della visione sfocata Dolore alla visione o gonfiore o vedere aloni attorno alle luci;
- Sintomi cardiaci gravi come battiti cardiaci irregolari o martellanti veloci; svolazzando nel petto; fiato corto; e vertigini improvvise Accendino o svenire;
- Grave mal di testa confusione Il braccio del linguaggio bloccato o la debolezza delle gambe problemi perdite perdita di coordinamento sentendoti instabili muscoli molto rigidi ad alta febbre abbondante sudorazione o tremori.
Questo documento non contiene tutti i possibili effetti collaterali e altri possono verificarsi. Verificare con il tuo medico ulteriori informazioni sugli effetti collaterali.
Dosaggio per Trudhesa
La dose raccomandata di spray nasale Trudhesa è di 1,45 mg (somministrato come spruzzo a misura di 0,725 mg in ciascuna narice). La dose può essere ripetuta se necessario un minimo di 1 ora dopo la prima dose.
Trudhesa nei bambini
La sicurezza e l'efficacia dello spray nasale Trudhesa non sono state stabilite nei pazienti pediatrici.
Quali sostanze o integratori di farmaci interagiscono con Trudhesa?
Lo spray nasale di Trudhesa può interagire con altri medicinali come:
- beta-bloccanti
- nicotina
- inibitore del reuptake della serotonina selettiva ( Se ) antidepressivi (ad esempio fluoxetina fluvoxamina paroxetina sertralina)
- Inibitori della proteasi (ad es. Ritonavir Nelfinavir indinavir)
- macrolide Antibiotici (ad es. eritromicina claritromicina)
- Antifungini (ad esempio ketoconazole itraconazole)
- triptani e
- Vasocostrittori.
Dì al medico tutti i farmaci e gli integratori che usi.
Trudhesa durante la gravidanza e l'allattamento
Di 'al medico se sei incinta o hai intenzione di rimanere incinta prima di usare lo spray nasale Trudhesa. Può aumentare il rischio di consegna pretermine e può danneggiare un feto. Non è noto se lo spray nasale di Trudhesa passa nel latte materno; Tuttavia, nell'ergotamina è presente un farmaco correlato nel latte materno. A causa del potenziale per l'apporto di latte ridotto e degli eventi avversi gravi nel bambino allattato al seno, incluso il vomito di diarrea che vomina il impulso debole e l'allattamento al seno instabile non è raccomandato durante il trattamento con spray nasale Trudhesa e per 3 giorni dopo l'ultima dose. L'approvvigionamento di latte materno durante questo periodo deve essere pompato e scartato.
Ulteriori informazioni
Il nostro Centro farmaco droga di Trudhesa (Diidroergotamina mesilato) spray nasale fornisce una visione completa delle informazioni disponibili sui farmaci sui potenziali effetti collaterali quando si assume questo farmaco.
Questo non è un elenco completo di effetti collaterali e altri possono verificarsi. Chiama il medico per consigli medici sugli effetti collaterali. È possibile segnalare gli effetti collaterali alla FDA al numero 1-800-FDA-1088.
Informazioni sui farmaci FDA
- Descrizione del farmaco
- Indicazioni
- Effetti collaterali
- Interazioni farmacologiche
- Avvertimenti
- Overdose
- Controindicazioni
- Farmacologia clinica
- Guida ai farmaci
AVVERTIMENTO
Ischemia periferica a seguito della somministrazione di co -co -co -CYP3A4
L'ischemia periferica grave e/o potenzialmente letale è stata associata alla somministrazione di co -idroergotamina con forti inibitori del CYP3A4. Poiché l'inibizione del CYP3A4 eleva i livelli sierici di diidroergotamina, aumenta il rischio di vasospasmo che porta all'ischemia cerebrale e/o all'ischemia delle estremità. Quindi l'uso concomitante di Trudhesa con forti inibitori del CYP3A4 è controindicato [vedi Controindicazioni AVVERTIMENTOS AND PRECAUTIONS E Interazioni farmacologiche ].
Descrizione per Trudhesa
Lo spray nasale di Trudhesa (diidroergotamina mesilato) è un prodotto di combinazione di dispositivi di dispositivo a dosaggio monodosaggio contenente un componente di farmaco mesilato di diidroergotamina e un componente di dispositivo di spruzzo nasale.
Il nome chimico per la diidroergotamina mesilato è Ergotaman-3 '6' 18-Trione 910-Dihydro- 12'-Hydroxy-2'-metil-5'- (fenilmetil)-(5'a)-monometanesulfonato. Il suo peso molecolare è 679,78 e la sua formula molecolare è C 33 H 37 N 5 O 5 • Ch 4 O 3 S.
La struttura chimica è:
 |
Il componente del farmaco è una soluzione di mesilato di diidroergotamina. Ogni millilitro (ml) di soluzione contiene diidroergotamina mesilato 4,0 mg (equivalente a 3,43 mg diidroergotamina) e i seguenti ingredienti inattivi: caffeina (NULL,0 mg) di anidride carbonica (Q.s.) destrosio (NULL,0 mg) e acqua (q.s. a 1.0 ml).
Lo spray nasale di Trudhesa dopo l'assemblaggio e il innesco fornisce 0,725 mg diidroergotamina mesilato per spray. Una dose totale di 1,45 mg di mesilato di diidroergotamina viene erogata in 2 spray. Il dispositivo spray nasale contiene propellente Hydrofluoroalkane-134A (HFA).
Usi per Trudhesa
Trudhesa è indicato per il trattamento acuto dell'emicrania con o senza aura negli adulti.
Limiti di utilizzo
Trudhesa non è indicato per il trattamento preventivo dell'emicrania.
Trudhesa non è indicato per la gestione dell'emicrania emiplegica o basilare.
Dosaggio per Trudhesa
Informazioni sul dosaggio
La dose raccomandata di Trudhesa è somministrata 1,45 mg come due spray misurati nel naso (uno spruzzo di 0,725 mg in ogni narice).
La dose può essere ripetuta se necessario un minimo di 1 ora dopo la prima dose. Non utilizzare più di 2 dosi di Trudhesa in un periodo di 24 ore o 3 dosi in un periodo di 7 giorni.
Valutazione prima della prima dose
Prima dell'inizio di Trudhesa si raccomanda una valutazione cardiovascolare [vedi AVVERTIMENTOS AND PRECAUTIONS ]. For patients with risk factors predictive of coronary artery disease who are determined to have a satisfactory cardiovascular evaluation it is strongly recommended that administration of the first dose of TRUDHESA take place in the setting of an equipped healthcare facility.
Importanti istruzioni di amministrazione
Trudhesa è solo per la somministrazione nasale e non deve essere iniettata.
Trudhesa deve essere assemblato prima dell'uso (vedi Istruzioni per l'uso ). Utilizzare o scartare Trudhesa entro 8 ore una volta che la fiala è stata aperta o il prodotto è stato assemblato.
Adepisce il Trudhesa assemblato prima dell'uso iniziale rilasciando 4 spray. Usa Trudhesa immediatamente dopo l'invio. Scartare Trudhesa immediatamente dopo l'uso. Apri e prepara un nuovo Trudhesa se è necessaria una dose aggiuntiva.
Come fornito
Forme di dosaggio e punti di forza
Lo spray nasale di Trudhesa (diidroergotamina mesilato) è un prodotto di combinazione di dispositivi di dispositivo a dosaggio monodosaggio contenente una fiala di mesilato diidroergotamina con una soluzione chiara e incolore a giallo e un dispositivo di consegna intranasale. Ogni spray offre 0,725 mg di mesilato diidroergotamina.
Trudhesa (diidroergotamina mesilato) spray nasale (NULL,725 mg per spruzzo) viene fornito come un pacchetto di 4 unità a dosi monodose ( Ndc 77530-725-04). Ogni unità monodose contiene:
- Una fiala di vetro ambra ( Ndc 77530-725-01) contenente 4 mg di diidroergotamina mesilato in una soluzione trasparente da 1 ml di chiaro e incolore a debolmente giallo. Il tappo non è realizzato con lattice in gomma naturale.
- Un dispositivo spray nasale.
Archiviazione e maneggevolezza
Conservare Trudhesa a temperatura ambiente controllata da 20 ° C a 25 ° C (da 68 ° F a 77 ° F) con escursioni consentite tra 15 ° C a 30 ° C (da 59 ° F a 86 ° F). Non refrigerare o congelare.
Prodotto da: Mipharm S.P.A. Milano Italia. Revisionato: settembre 2021
Effetti collaterali for Trudhesa
Le seguenti reazioni avverse clinicamente significative sono descritte altrove nell'etichettatura:
- Ischemia periferica a seguito della somministrazione di co -co -co -inibitore del CYP3A4 [vedi Avvertenza della scatola E AVVERTIMENTOS AND PRECAUTIONS ]
- Ischemia miocardica e/o infarto altri eventi cardiaci avversi e vittime [vedi AVVERTIMENTOS AND PRECAUTIONS ]
- Reazioni avverse cerebrovascolari e vittime [vedi AVVERTIMENTOS AND PRECAUTIONS ]
- Altre reazioni avverse relative al vasospasmo [vedi AVVERTIMENTOS AND PRECAUTIONS ]
- Aumento della pressione sanguigna [vedi AVVERTIMENTOS AND PRECAUTIONS ]
- Mal di testa a uso eccessivo di farmaci [vedi AVVERTIMENTOS AND PRECAUTIONS ]
- Laburista pretermine [vedi AVVERTIMENTOS AND PRECAUTIONS ]
- Complicanze fibrotiche [vedi AVVERTIMENTOS AND PRECAUTIONS ]
- Irritazione locale [vedi AVVERTIMENTOS AND PRECAUTIONS ]
Esperienza di studi clinici
Poiché gli studi clinici sono condotti in condizioni di reazione avverse ampiamente variabili osservate negli studi clinici di un farmaco non possono essere paragonati direttamente ai tassi negli studi clinici di un altro farmaco e potrebbero non riflettere i tassi osservati nella pratica.
Reazioni avverse negli studi controllati con placebo con spray nasale mesilato di diidroergotamina (DHE) [vedi Studi clinici ]
Dei 1796 pazienti e soggetti trattati con dosi di spray nasale DHE 2 mg o meno negli Stati Uniti e studi clinici stranieri 26 (NULL,4%) interrotti a causa di eventi avversi. Gli eventi avversi associati alla discontinua sono stati in declino di frequenza: rinite (13) vertigini (2) edema facciale (2) e un paziente ciascuno a causa di sudori freddi per la depressione del trauma accidentale di chirurgia elettiva di sonnolenza vomito ipotensione e la paratestesia.
Puoi prendere Pepcid con gli antibiotici
La tabella 1 riassume i tassi di incidenza delle reazioni avverse riportate da almeno l'1% dei pazienti che hanno ricevuto spray nasale DHE per il trattamento dell'emicrania durante gli studi clinici a doppio cieco controllati con placebo e erano più frequenti rispetto a quei pazienti che ricevono placebo. Le reazioni avverse più comunemente riportate (superiori all'1% dei pazienti che hanno ricevuto spray nasale DHE) sono state la rinite nausea alterata del senso del gusto reazioni del sito reazioni vertigini vomito la sonnolenza faringite e diarrea. Nella maggior parte dei casi questi eventi sono stati transitori e auto -limitati e non hanno comportato l'interruzione del paziente da uno studio.
Tabella 1 Reazioni avverse riportate da almeno l'1% dei pazienti trattati con spray nasale DHE e si sono verificate più frequentemente rispetto al gruppo placebo negli studi controllati da placebo
| E spray nasale N = 597 % | Placebo N = 631 % | |
| Sistema respiratorio | ||
| Rhinitis | 26 | 7 |
| Pharyngitis | 3 | 1 |
| Sistema gastrointestinale | ||
| Nausea | 10 | 4 |
| Vomiting | 4 | 1 |
| Diarrhea | 2 | <1 |
| Sensi speciali altri | ||
| Altered Sense of Taste | 8 | 1 |
| Sito di applicazione | ||
| Sito di applicazione Reaction | 6 | 2 |
| Sistema nervoso centrale e periferico | ||
| Dizziness | 4 | 2 |
| Somnolence | 3 | 2 |
| Corpo nel suo intero generale | ||
| Hot Flashes | 1 | <1 |
| Asthenia | 1 | 0 |
| Sistema muscoloscheletrico | ||
| Stiffness | 1 | <1 |
Reazioni avverse negli studi con Trudhesa
È stato condotto uno studio in aperto sugli adulti (18-66 anni) per valutare la sicurezza e la tollerabilità del ripetuto Trudhesa che l'uso di Trudhesa è stato consentito nel corso di 6-12 mesi. Un totale di 354 pazienti con emicrania hanno ricevuto almeno una dose di Trudhesa. Centottantacinque pazienti trattati in media almeno due emicranie al mese per 6 mesi e 55 pazienti trattati in media almeno due emicranie al mese per 12 mesi. Dei pazienti che hanno ricevuto almeno una dose di pazienti Trudhesa 185 (NULL,3%) hanno avuto sintomi irritativi locali. Di questi i sintomi irritativi locali più comuni erano la rinite del prodotto di disagio nasale del prodotto anormale/disgeusia sinusale Sinusite Sinus Disagio Olfattivo Test di epistassi anormale Faringite Faringite Mucosal Disturbo della mucosa nasale Cambia AVVERTIMENTOS AND PRECAUTIONS ].
Esperienza post -marketing
Le seguenti reazioni avverse sono state identificate durante l'uso post -approvazione del mesilato di diidroergotamina. Poiché queste reazioni sono riportate volontariamente da una popolazione di dimensioni incerte, non è sempre possibile stimare in modo affidabile la loro frequenza o stabilire una relazione causale con l'esposizione ai farmaci:
Vasospasmo parestesia Ipertensione Vertigini ansia Dispnea mal di testa che scarica la diarrea eruzione ha aumentato la sudorazione e la fibrosi pleurica e retroperitoneale dopo uso a lungo termine di diidroergotamina. Casi di infarto del miocardio e ictus sono stati segnalati a seguito dell'uso di mesilato di diidroergotamina [vedi AVVERTIMENTOS AND PRECAUTIONS ].
Interazioni farmacologiche for Trudhesa
Inibitori del CYP3A4
Ci sono stati rari segnalazioni di gravi eventi avversi in relazione alla somministrazione di co -somministrazione endovenosa di diidroergotamina e forti inibitori del CYP3A4 come inibitori della proteasi (ad esempio ritonavir nelfinavir indinavir) macrolide (ad angolo di ketochingir) antibiotici (erycintomin) e antifungini (ad esempio antifungini) itraconazolo) con conseguente vasospasmo che ha portato all'ischemia cerebrale e/o all'ischemia delle estremità [vedi AVVERTIMENTOS AND PRECAUTIONS ]. The use of strong CYP3A4 inibitori with dihydroergotamine is contraindicated [see Controindicazioni ]. Administer moderate CYP3A4 inibitori (e.g. saquinavir nefazodone fluconazolo grapefruit juice fluoxetine fluvoxamine zileuton clotrimazole) with caution.
Triptani
Triptani (serotonin [5-HT] 1B/1D receptor agonists) have been reported to cause coronary artery vasospasm E its effect could be additive with TRUDHESA. Therefore triptani e TRUDHESA should not be taken within 24 ore of each other [see Controindicazioni ].
Beta bloccanti
È stato riferito che il propranololo può potenziare l'azione vasocostrittiva dell'ergotamina bloccando la proprietà vasodilata dell'epinefrina.
Vasocostrittori
Trudhesa è controindicato per l'uso con vasocostrittori periferici e centrali perché la combinazione può causare un elevazione sinergica della pressione sanguigna [vedi AVVERTIMENTOS AND PRECAUTIONS ].
Nicotina
Nicotina may provoke vasoconstriction in some patients predisposing to a greater ischemic response to ergot therapy [see AVVERTIMENTOS AND PRECAUTIONS ].
Inibitori selettivi di reuptake della serotonina
Debolezza iperreflessia e incoordinazione sono stati riportati raramente quando 5-HT 1 Gli agonisti sono stati somministrati con co -amministrazione con inibitori selettivi di reuptake della serotonina (ad esempio fluoxetina fluvoxamina paroxetina sertralina).
Abuso e dipendenza da droghe
Sostanza controllata
Trudhesa contiene diidroergotamina (come sale mesilato) che non è una sostanza controllata.
Abuso
Abuso is the intentional non-therapeutic use of a drug even once for its desirable psychological or physiological effects. Currently available data have not demonstrated drug abuse with dihydroergotamine. However cases of drug abuse in patients on other forms of ergot therapy have been reported.
Dipendenza
La dipendenza fisica è uno stato che si sviluppa a causa dell'adattamento fisiologico in risposta al ripetuto uso di droghe manifestato da segni di astinenza e sintomi dopo una brusca interruzione o una significativa riduzione della dose di un farmaco. I dati attualmente disponibili non hanno dimostrato la dipendenza fisica o psicologica con la diidroergotamina. Tuttavia, sono stati riportati casi di dipendenza psicologica nei pazienti da altre forme di terapia ERGOT.
Avvertimenti per Trudhesa
Incluso come parte del 'PRECAUZIONI' Sezione
Precauzioni per Trudhesa
Ischemia periferica a seguito della somministrazione di co -co -co -CYP3A4
L'ischemia periferica grave e/o potenzialmente letale è stata associata alla somministrazione di co-diidroergotamina con forti inibitori del CYP3A4, compresi gli inibitori della proteasi macrolide antibiotici e antifungini. Poiché l'inibizione del CYP3A4 eleva i livelli sierici di diidroergotamina, aumenta il rischio di vasospasmo che porta all'ischemia cerebrale e/o all'ischemia delle estremità. Quindi l'uso concomitante di Trudhesa con forti inibitori del CYP3A4 è controindicato [vedi Controindicazioni E Interazioni farmacologiche ].
Ischemia miocardica e/o infarto Altre reazioni avverse cardiache e vittime
Il potenziale di reazioni avverse cardiache avverse esiste con il trattamento con Trudhesa. Eventi cardiaci avversi gravi, tra cui alcuni che sono stati fatali si sono verificati dopo l'uso di mesilato di diidroergotamina. Questi eventi hanno incluso infarto miocardiale acuto disturbi del salotta di vita del ritmo cardiaco (ad esempio tachicardia ventricolare e fibrillazione ventricolare) vasospasmo coronarico e ischemia miocardica transitoria.
Prima dell'inizio di Trudhesa, si raccomanda una valutazione cardiovascolare per determinare se il paziente è privo di arteria coronarica e malattia miocardica ischemica o altre significative malattie cardiovascolari sottostanti. Se durante la valutazione cardiovascolare, la storia medica del paziente (compresi i fattori di rischio) o i risultati delle indagini elettrocardiografiche sono coerenti con il vasospasmo dell'arteria coronarica o l'ischemia miocardica non deve essere somministrato [vedi Controindicazioni ].
Per i pazienti con fattori di rischio predittivi della malattia coronarica (ad esempio ipertensione ipercolesterolemia fumatore di obesità Diabete Storia familiare forte di malattia coronarica femminile chirurgicamente o fisiologicamente in postmenopausa. L'impostazione di una struttura sanitaria attrezzata a meno che il paziente non abbia precedentemente ricevuto mesilato di diidroergotamina. Durante l'intervallo immediatamente successivo al primo uso di Trudhesa, è raccomandato un elettrocardiogramma in quei pazienti con fattori di rischio perché l'ischemia può verificarsi in assenza di sintomi clinici.
Reazioni avverse cerebrovascolari e vittime
Il potenziale per le reazioni avverse cerebrovascolari avverse esiste con il trattamento di Trudhesa. Emorragia cerebrale subaracnoidea ictus di emorragia e altri eventi cerebrovascolari sono stati riportati in pazienti trattati con diidroergotamina mesilato; E alcuni hanno provocato vittime. In un certo numero di casi sembra possibile che gli eventi cerebrovascolari fossero primari, il mesilato di diidroergotamina essendo stato somministrato nella convinzione errata che i sintomi vissuti fossero una conseguenza dell'emicrania quando non lo erano. Va notato che i pazienti con emicrania possono essere ad aumentato rischio di determinati eventi cerebrovascolari (ad es. Attacco ischemico transitorio di emorragia dell'ictus). Interrompere il trudhesa se si sospetta un evento cerebrovascolare.
Altre reazioni avverse relative al vasospasmo
Trudhesa come altri alcaloidi Ergot può causare reazioni vasospastiche diverse dal vasospasmo dell'arteria coronarica. L'ischemia vascolare periferica e colon periferica miocardica è stata segnalata con mesilato di diidroergotamina.
I fenomeni vasospastici associati a mesilato di diidroergotamina mesilato possono anche causare dolori muscolari intorpidimento pallore e cianosi delle cifre. Nei pazienti con circolazione compromessa il vasospasmo persistente può provocare cancrena o morte. Trudhesa dovrebbe essere sospeso immediatamente se si sviluppano segni o sintomi di vasocostrizione.
I pazienti che sperimentano altri sintomi o segni che suggeriscono una riduzione del flusso arterioso come la sindrome dell'intestino ischemico o la sindrome di Raynaud in seguito all'uso di qualsiasi agonista 5-HT incluso Trudhesa dovrebbe essere valutato da un operatore sanitario.
Aumento della pressione sanguigna
È stato riportato un aumento significativo della pressione sanguigna in rare occasioni in pazienti con e senza una storia di ipertensione trattata con mesilato di diidroergotamina. Trudhesa è controindicato nei pazienti con ipertensione non controllata [vedi Controindicazioni ].
Un aumento del 18% della pressione media dell'arteria polmonare è stato osservato a seguito di un dosaggio con un altro 5- ht 1 agonista in uno studio che valuta i soggetti sottoposti a cateterismo cardiaco.
Mal di testa a uso eccessivo di farmaci
L'uso eccessivo di droghe di emicrania acuta (ad esempio oppioidi di ergotaminine triptans o una combinazione di questi farmaci per 10 o più giorni al mese) può portare all'esacerbazione del mal di testa (cioè mal di testa a uso eccessivo di farmaci). Il mal di testa a uso eccessivo di farmaci può presentare come mal di testa quotidiano a forma di emicrania o come un marcato aumento della frequenza degli attacchi di emicrania. La disintossicazione dei pazienti incluso la sospensione dei farmaci abusati e il trattamento dei sintomi di astinenza (che spesso include un peggioramento transitorio del mal di testa) può essere necessaria.
Lavoro pretermine
Sulla base del meccanismo d'azione della diidroergotamina e i risultati della letteratura pubblicata Trudhesa possono causare lavoro pretermine. Evita l'uso di Trudhesa durante la gravidanza [vedi Utilizzare in popolazioni specifiche ]
Complicanze fibrotiche
Il potenziale per le complicanze fibrotiche esiste con il trattamento di Trudhesa. Sono stati segnalati segnalazioni di fibrosi pleurica e retroperitoneale in pazienti a seguito di un uso quotidiano prolungato di mesilato di diidroergotamina. L'uso quotidiano raramente prolungato di altri farmaci alcaloidi ERGOT è stato associato a fibrosi valvolare cardiaca. Sono stati anche riportati rari casi in associazione con l'uso di mesilato di diidroergotamina; Tuttavia, in questi casi i pazienti hanno anche ricevuto farmaci noti per essere associati alla fibrosi valvolare cardiaca.
La somministrazione di Trudhesa non deve superare le linee guida per il dosaggio e non dovrebbe essere utilizzata per la somministrazione quotidiana cronica [vedi Dosaggio e amministrazione ].
Irritazione locale
I sintomi irritativi locali sono stati riportati nel 52% dei pazienti trattati con almeno una dose di Trudhesa in uno studio con etichetta aperta che ha consentito un uso ripetuto di Trudhesa per 6-12 mesi. I sintomi irritativi locali più comuni (almeno l'1%dei pazienti) erano rinofaringite (21%) rinite (19%) disagio nasale (7%) gusto del prodotto anormale/disgeusia (6%) sinusite (5%) sinus Test (UPSIT)] (4%) epistassi (3%) faringite (3%) Disturbo della mucosa nasale (2%) variazione dell'odore (1%) Discusta dell'orecchio (1%) e rinorrea (1%). Se si verifica un grave evento di irritazione locale per nessun altro motivo attribuibile, Trudhesa dovrebbe essere temporaneamente sospeso fino a quando l'evento non si risolve. Se l'evento non si risolve o si ripresenta con la re-cocammata Trudhesa dovrebbe essere sospeso in modo permanente. La somministrazione di Trudhesa non deve superare le linee guida per il dosaggio e non dovrebbe essere utilizzata per la somministrazione quotidiana cronica [vedi Dosaggio e amministrazione ].
Il tessuto nasale negli animali trattati quotidianamente con diidroergotamina mesilato mostrava una lieve irritazione mucosa caratterizzata da iperplasia delle cellule mucose e di cellule di transizione e metaplasia delle cellule squamose. I cambiamenti nella mucosa nasale di ratto a 64 settimane erano meno gravi rispetto a 13 settimane. Non sono stati valutati effetti locali sul tessuto respiratorio dopo dosaggio intranasale cronico negli animali.
Informazioni sulla consulenza del paziente
Consiglia al paziente di leggere l'etichettatura del paziente approvato dalla FDA ( Guida ai farmaci E Istruzioni per l'uso ).
Quante volte puoi prendere Prometazina
Reazioni gravi e/o pericolose per la vita con co-somministrazione di inibitori del CYP3A4
Informare i pazienti che l'ischemia periferica grave e/o potenzialmente letale (ischemia cerebrale e/o ischemia delle estremità) è stata associata al co-amministrazione della diidroergotamina mesilato e dei forti inibitori del CYP3A4 come gli antibiotici macrolidi come gli inibitori dei macrolidi come macrolidi Controindicazioni AVVERTIMENTOS AND PRECAUTIONS E Interazioni farmacologiche ].
Ischemia miocardica e/o infarto Altri eventi cardiaci eventi e vittime cerebrovascolari
Informare i pazienti del rischio di eventi cerebrovascolari cardiaci gravi e di altri vasospasmo. Consiglia ai pazienti di avvisare il proprio operatore sanitario se sviluppano fattori di rischio o sintomi durante l'assunzione di Trudhesa. Informare i pazienti che la nicotina può provocare la vasocostrizione prevedendo a una maggiore risposta ischemica [vedi AVVERTIMENTOS AND PRECAUTIONS ].
Mal di testa a uso eccessivo di farmaci
Informare i pazienti che l'uso di farmaci per trattare gli attacchi di emicrania per 10 o più giorni al mese può portare a un'esacerbazione del mal di testa e incoraggiare i pazienti a registrare la frequenza del mal di testa e l'uso di droghe (ad esempio mantenendo un diario di mal di testa) [vedi AVVERTIMENTOS AND PRECAUTIONS ].
Irritazione locale
Consiglia ai pazienti di avvisare il proprio operatore sanitario se hanno fastidiose irritazioni locali [vedi AVVERTIMENTOS AND PRECAUTIONS ].
Interazioni farmacologiche
Consiglia ai pazienti di informare i loro operatori sanitari se stanno assumendo o pianificano di assumere farmaci da prescrizione o da banco poiché esiste un potenziale per le interazioni [vedi Interazioni farmacologiche ].
Gravidanza
Consiglia ai pazienti del rischio di nascita pretermine. Consiglia alle donne di informare il proprio operatore sanitario se sono incinte o intendono rimanere incinta [vedi AVVERTIMENTOS AND PRECAUTIONS Utilizzare in popolazioni specifiche ]
Lattazione
Consiglia ai pazienti di non allattare al seno durante il trattamento con Trudhesa [vedi Utilizzare in popolazioni specifiche ].
Importanti istruzioni di amministrazione
Consiglio ai pazienti che Trudhesa deve essere assemblato prima dell'uso e che prima della somministrazione del dispositivo deve essere innescato (cioè pompato 4 volte). Chiedere ai pazienti di utilizzare o scartare Trudhesa entro 8 ore una volta che la fiala è stata aperta o il prodotto è stato assemblato.
Tossicologia non clinica
Mutagenesi della carcinogenesi compromissione della fertilità
Carcinogenesi
Non è stata valutata la valutazione del potenziale cancerogeno della diidroergotamina mesilato nei topi e nei ratti.
Mutagenesi
La diidroergotamina il mesilato era negativo in un in vitro Mutagenicità (AMES) Assay e positivo in in vitro Aberrazione cromosomica (test delle cellule di criceto cinese V79 con attivazione metabolica e linfociti del sangue periferico umano). La diidroergotamina era negativa in in vivo Saggi di micronucleo nel topo e nel criceto.
Compromissione della fertilità
Non vi era alcuna prova di compromissione della fertilità nei ratti somministrati dosi intranasali di mesilato di diidroergotamina con mesilato fino a 1,6 mg/die, che era associato a esposizioni plasmatiche (AUC) circa 3 volte che nell'uomo alla massima dose umana raccomandata di 2,9 mg/giorno.
Utilizzare in popolazioni specifiche
Gravidanza
Riepilogo del rischio
I dati disponibili dalla letteratura pubblicata indicano un aumentato rischio di consegna pretermine con uso di Trudhesa durante la gravidanza. Evita l'uso di Trudhesa durante la gravidanza [vedi AVVERTIMENTOS AND PRECAUTIONS ]. Dati collected over decades have shown no increased risk of major birth defects or miscarriage with use of dihydroergotamine mesylate during pregnancy.
Negli studi sugli animali sono stati osservati effetti avversi sullo sviluppo dell'embriofetale in seguito alla somministrazione di mesilato di diidroergotamina durante la gravidanza (riduzione del peso corporeo fetale e/o dell'ossificazione scheletrica) nei ratti e nei conigli o durante la gravidanza e l'allattamento non sono stati associati con i ratti (ridotti alti moti -medie (riduciti dal corpo del corpo (non sono stati associati al peso corporeo (non sono stati associati al peso corporeo (riducendo il peso corporeo (alimentazione del corpo del corpo alterato (non sono stati associati a clinico (riduttori di clinico (diminuisce il peso corporeo (riduzione del corpo corporeo. Dati ).
Il tasso stimato dei principali difetti alla nascita (dal 2,2%al 2,9%) e l'aborto (17%) tra le consegne alle donne con emicrania sono simili ai tassi riportati nelle donne senza emicrania. Tutte le gravidanze hanno un rischio di fondo di perdita di difetti alla nascita o altri risultati avversi. Nella popolazione generale degli Stati Uniti il rischio di background stimato di importanti difetti alla nascita e aborti nelle gravidanze clinicamente riconosciute è rispettivamente dal 2% al 4% e dal 15% al 20%.
Dati
Dati sugli animali
La somministrazione intranasale di diidroergotamina mesilato a ratti in gravidanza durante il periodo di organogenesi ha comportato una riduzione del peso corporeo fetale e/o dell'ossificazione scheletrica a dosi di 0,16 mg/die (associate alle esposizioni plasmatiche [AUC] meno di quella nell'uomo al massimo dose umana raccomandata [MRHD] di 2.9 mg) o maggiore. Un livello senza effetto per la tossicità embriofetale non è stato identificato nei ratti. La somministrazione intranasale di mesilato di diidroergotamina a conigli incinta durante l'organogenesi ha comportato una ridotta ossificazione scheletrica a 3,6 mg/die. Alla dose senza effetto (NULL,2 mg/die) per gli effetti avversi sullo sviluppo dell'embriofetale nelle esposizioni al plasma dei conigli (AUC) erano inferiori a quello negli esseri umani al MRHD.
La somministrazione intranasale di diidroergotamina mesilato ai ratti femmine durante la gravidanza e l'allattamento ha comportato una riduzione del peso corporeo e la funzione riproduttiva compromessa (riduzione degli indici di accoppiamento) è stata osservata nella prole a dosi di 0,16 mg/die o maggiore. Non è stata stabilita una dose senza effetto per effetti di sviluppo avversi nei ratti.
Gli effetti sullo sviluppo si sono verificati a dosi inferiori a quelle che hanno prodotto prove di una significativa tossicità materna in questi studi.
Il ritardo della crescita intrauterina indotta dalla diidroergotamina è stata attribuita a una ridotta flusso sanguigno uteroplacentale derivante da vasocostrizione prolungata dei vasi uterini e/o aumento del tono miometriale.
Lattazione
Riepilogo del rischio
Non ci sono dati sulla presenza di diidroergotamina nel latte umano; Tuttavia ergotamina è presente un farmaco correlato nel latte umano. Ci sono segnalazioni di diarrea che vomito il impulso debole e la pressione sanguigna instabile nei neonati allattati al seno esposti all'ergotamina. Trudhesa può ridurre l'approvvigionamento di latte perché può ridurre i livelli di prolattina. A causa del potenziale per la riduzione dell'approvvigionamento di latte e degli eventi avversi gravi nel bambino allattato al seno, incluso la diarrea che vomina il impulso debole e la pressione arteriosa instabile consiglia ai pazienti di non allattare durante il trattamento con Trudhesa e per 3 giorni dopo l'ultima dose. L'approvvigionamento di latte materno durante questo periodo deve essere pompato e scartato.
Uso pediatrico
La sicurezza ed efficacia nei pazienti pediatrici non è stata stabilita.
Uso geriatrico
Studi clinici su Trudhesa e altri prodotti mesilati di diidroergotamina non includevano un numero sufficiente di soggetti di età pari o superiore a 65 anni per determinare se rispondono in modo diverso dai soggetti più giovani. In generale, la selezione della dose per un paziente anziano dovrebbe essere cauta di solito a partire dalla fascia bassa dell'intervallo di dosaggio che riflette la maggiore frequenza della ridotta funzione renale e cardiaca epatica e di malattia concomitante o altra terapia farmacologica.
Overdose Information for Trudhesa
Sintomi
Dosi eccessive di diidroergotamina possono provocare segni periferici e sintomi dell'ergotismo. In generale, i sintomi di un sovradosaggio acuto di Trudhesa sono simili a quelli di un sovradosaggio di ergotamina sebbene ci possa essere nausea e vomito meno pronunciati con Trudhesa. I sintomi di un sovradosaggio di ergotamina comprendono i seguenti: intorpidimento formicolio e cianosi delle estremità associate a impulsi periferici diminuiti o assenti; depressione respiratoria; un aumento e/o una diminuzione della pressione sanguigna di solito in quell'ordine; Confusion convulsioni e coma; e/o un certo grado di vomito di nausea e dolore addominale.
Negli animali da laboratorio la diidroergotamina era letale se somministrata a dosi per via endovenosa di 44 mg/kg in topi 130 mg/kg nei ratti e 37 mg/kg in conigli.
Trattamento
Trattamento includes discontinuance of the drug local application of warmth to the affected area the administration of vasodilators E nursing care to prevent tissue damage. Up-to-date information about the treatment of overdosage can often be obtained from a certified Regional Poison Control Center.
Controindicazioni for Trudhesa
Trudhesa è controindicato nei pazienti:
Kuta-Bali Indonesia
- Con un uso concomitante di forti inibitori del CYP3A4 come inibitori della proteasi (ad esempio ritonavir nelfinavir o indinavir) antibiotici macrolidi (ad esempio eritromicina o chiaritromicina) e antifungini (ketoconazolo o itraconazolo) [vedi AVVERTIMENTOS AND PRECAUTIONS E Interazioni farmacologiche ]
- con cardiopatia ischemica (Angina pectoris Storia dell'infarto miocardico o ischemia silenziosa documentata) o pazienti che hanno sintomi clinici o risultati coerenti con il vasospasmo dell'arteria coronarica, compresa l'angina variante di Prinzmetal [vedi AVVERTIMENTOS AND PRECAUTIONS ]
- con ipertensione incontrollata [vedi AVVERTIMENTOS AND PRECAUTIONS ]
- con malattia arteriosa periferica
- con sepsi
- seguendo la chirurgia vascolare
- con grave compromissione epatica
- con grave compromissione renale
- con ipersensibilità nota agli alcaloidi Ergot
- con un uso recente (cioè entro 24 ore) da altri 5-HT 1 Agonisti (ad es. Sumatriptan) o farmaci contenenti ergotamina o di tipo ERGOT [vedi Interazioni farmacologiche ]
- con un uso concomitante di vasocostrittori periferici e centrali perché la combinazione può provocare un aumento additivo o sinergico della pressione sanguigna [vedi AVVERTIMENTOS AND PRECAUTIONS ]
Farmacologia clinica for Trudhesa
Meccanismo d'azione
Diidroergotamina si lega ad alta affinità con 5-HT 1da E 5-HT 1db recettori. L'attività terapeutica della diidroergotamina nell'emicrania è generalmente attribuita agli effetti agonisti a 5-HT 1d recettori.
Farmacodinamica
È stato riportato un aumento significativo della pressione sanguigna in pazienti con e senza una storia di ipertensione [vedi AVVERTIMENTOS AND PRECAUTIONS ].
Diidroergotamina possiede proprietà ossitociche [vedi AVVERTIMENTOS AND PRECAUTIONS ].
Farmacocinetica
Assorbimento
Il tempo medio dal dosaggio alla massima concentrazione plasmatica dopo la somministrazione di Trudhesa era di circa 0,5 ore.
Distribuzione
La diidroergotamina mesilato è legata alla proteina plasmatica al 93%. L'apparente volume di distribuzione a stato stazionario è di circa 800 litri.
Eliminazione
Metabolismo
Quattro metaboliti mesilati di diidroergotamina sono stati identificati nel plasma umano dopo la somministrazione orale. La principale metabolita 8'-ß-idrossi diidroergotamina mostra un'affinità equivalente al suo genitore per i recettori adrenergici e 5-HT e dimostra una potenza equivalente in diversi modelli di attività venocostrittore in vivo E in vitro . Gli altri metaboliti, cioè acido diidrolisergico, l'ammide diidrolisergica e un metabolita formato dall'apertura ossidativa dell'anello di prolina sono di minore importanza. Dopo la somministrazione nasale i metaboliti totali rappresentano solo il 20% e il 30% di AUC al plasma. La clearance sistemica della diidroergotamina mesilata dopo la somministrazione endovenosa e intramuscolare è di 1,5 L/min. La caratterizzazione farmacocinetica quantitativa dei quattro metaboliti non è stata eseguita.
Escrezione
La principale via escretrice di diidroergotamina è attraverso la bile nelle feci. La clearance totale del corpo è di 1,5 L/min che riflette principalmente clearance epatica. Solo dal 6% al 7% della diidroergotamina invariata viene escreto nelle urine dopo l'iniezione intramuscolare. La clearance renale (NULL,1 L/min) non è influenzata dalla via della somministrazione di diidroergotamina.
L'emivita media apparente della somministrazione nasale di Trudhesa in soggetti sani è di circa 12 ore.
Popolazioni specifiche
Non sono stati condotti studi sull'effetto dell'etnia di razza di genere renale o epatica per la razza di genere sulla farmacocinetica di diidroergotamina [vedi Controindicazioni Utilizzare in popolazioni specifiche ].
Studi sull'interazione farmacologica
Inibitori del CYP3A4
Rapari segnalazioni di ergotismo sono state ottenute da pazienti trattati con antibiotici di diidroergotamina e macrolide (ad esempio claritromicina eritromicina) e da pazienti trattati con la diidroergotamina e inibitori della proteasi (ad esempio ritonavir) presumibilmente a causa di inibizione della cyp3a di ergisma [ergotamina [che Controindicazioni ].
Altre droghe
La farmacocinetica della diidroergotamina non sembrava essere significativamente influenzata dall'uso concomitante di un vasocostrittore locale.
Dosi multiple orali dell'antagonista dell'antagonista β-adrenoptor propranololo utilizzato per la profilassi dell'emicrania non hanno avuto alcuna influenza significativa sulle dosi di CMAX TMAX o AUC di dosi di diidroergotamina fino a 4 mg. Tuttavia il propranololo può potenziare l'azione vasocostrittiva dell'ergotamina [vedi Interazioni farmacologiche ].
L'effetto dei contraccettivi orali sulla farmacocinetica di Trudhesa non è stato studiato.
Studi clinici
L'efficacia di Trudhesa si basa sulla relativa biodisponibilità dello spray nasale Trudhesa rispetto allo spray nasale di diidroergotamina mesilato in soggetti sani.
Gli studi clinici descritti di seguito sono stati condotti utilizzando spray nasale mesilato di diidroergotamina.
L'efficacia dello spray nasale mesilato di diidroergotamina mesilato per il trattamento acuto del mal di testa è stata valutata in quattro studi randomizzati controllati in doppio cieco controllati negli Stati Uniti. La popolazione di pazienti per gli studi era prevalentemente femmina (87%) e caucasico (95%) con un'età media di 39 anni (intervallo 18-65 anni). I pazienti hanno trattato un singolo mal di testa da emicrania da moderata a grave con una singola dose di farmaco di studio e hanno valutato la gravità del dolore per le 24 ore successive al trattamento. La risposta al mal di testa è stata determinata 0,5 1 2 3 e 4 ore dopo il dosaggio ed è stata definita come una riduzione della gravità del mal di testa a dolore lieve o assente. Negli studi 1 e 2 è stata utilizzata una scala di intensità del dolore a quattro punti; Negli studi 3 e 4 una scala a cinque punti è stata utilizzata per registrare la risposta al dolore. Sebbene in tutti e quattro gli studi siano stati autorizzati i farmaci per il salvataggio sono stati istruiti a non usarli durante il periodo di osservazione di quattro ore. Negli studi 3 e 4 una dose totale di 2 mg è stata confrontata con il placebo. Negli studi 1 e 2 dosi di 2 e 3 mg sono stati valutati e non hanno mostrato alcun vantaggio della dose più elevata per un singolo trattamento. In tutti gli studi i pazienti hanno ricevuto un regime costituito da 0,5 mg in ciascuna narice ripetuta in 15 minuti (e di nuovo in altri 15 minuti per la dose di 3 mg negli studi 1 e 2).
La percentuale di pazienti che ha raggiunto la risposta al mal di testa 4 ore dopo il trattamento è stata significativamente maggiore nei pazienti che hanno ricevuto 2 mg di dosi di spray nasale mesilato di diidroergotamina rispetto a quelli che hanno ricevuto placebo in 3 dei 4 studi (vedere la Tabella 2 e la Tabella 3 e la Figura 1 e la Figura 2).
Tabella 2 Studi 1 e 2: percentuale di pazienti con risposta al mal di testa a 2 e 4 ore dopo un singolo trattamento del farmaco di studio (spray nasale di diidroergotamina mesilato o placebo)
| N | 2 ore | 4 ore | ||
| Studio 1 | Spray nasale mesilato di diidroergotamina | 105 | 61%** | 70%** |
| Placebo | 98 | 23% | 28% | |
| Differenza dal placebo | 37% | 42% | ||
| Studio 2 | Spray nasale mesilato di diidroergotamina | 103 | 47% | 56%* |
| Placebo | 102 | 33% | 35% | |
| Differenza dal placebo | 14% | 21% | ||
| a La risposta al mal di testa è stata definita come una riduzione della gravità del mal di testa a dolore lieve o assente. La risposta al mal di testa si basava sull'intensità del dolore interpretata dal paziente usando una scala di intensità del dolore a quattro punti. *valore p <0.01 ** Valore p <0.001 |
Tabella 3 Studi 3 e 4: percentuale di pazienti con risposta al mal di testa a 2 e 4 ore dopo un singolo trattamento del farmaco di studio (spray nasale di diidroergotamina mesilato o placebo)
| N | 2 ore | 4 ore | ||
| Studio 3 | Spray nasale mesilato di diidroergotamina | 50 | 32 | 48%* |
| Placebo | 50 | 20% | 22% | |
| Differenza dal placebo | 12% | 26% | ||
| Studio 4 | Spray nasale mesilato di diidroergotamina | 47 | 30% | 47% |
| Placebo | 50 | 20% | 30% | |
| Differenza dal placebo | 10% | 17% | ||
| a La risposta al mal di testa è stata definita come una riduzione della gravità del mal di testa a dolore lieve o assente. La risposta al mal di testa è stata valutata su una scala a cinque punti che includeva la risposta al dolore. *valore p <0.01 |
I grafici di Kaplan-Meier di seguito (Figura 1 e Figura 2) forniscono una stima della probabilità che un paziente abbia risposto a una singola dose di 2 mg di spray nasale mesilato di diidroergotamina mesilato in funzione del tempo trascorso dall'inizio del trattamento.
Figura 1 Probabilità stimata di un paziente che risponde durante le quattro ore successive a una singola dose di 2 mg di spray nasale mesilato di diidroergotamina in funzione in funzione del tempo trascorso dall'inizio del trattamento*
| *La figura mostra la probabilità nel tempo di ottenere una risposta dopo il trattamento con spray nasale mesilato di diidroergotamina. La risposta al mal di testa si basava sull'intensità del dolore interpretata dal paziente usando una scala di intensità del dolore a quattro punti. I pazienti che non hanno raggiunto la risposta entro 4 ore sono stati censurati a 4 ore. |
Figura 2 Probabilità stimata di un paziente che risponde allo spray nasale mesilato di diidroergotamina durante le quattro ore successive al dosaggio*
| *La figura mostra la probabilità nel tempo di ottenere una risposta dopo il trattamento con spray nasale mesilato di diidroergotamina. La risposta al mal di testa è stata valutata su una scala a cinque punti che includeva la risposta al dolore. I pazienti che non hanno raggiunto la risposta entro 4 ore sono stati censurati a 4 ore. |
Per i pazienti con fotofobia di nausea e fonofobia associata all'emicrania al basale, si è verificata una minore incidenza di questi sintomi a 2 e 4 ore dopo la somministrazione di spray nasale mesilato di diidroergotamina rispetto al placebo.
Ai pazienti non è stato permesso di utilizzare ulteriori trattamenti per 8 ore prima del dosaggio dei farmaci per lo studio e durante il periodo di osservazione di 4 ore dopo il trattamento dello studio. Dopo il periodo di osservazione di 4 ore, i pazienti sono stati autorizzati a utilizzare trattamenti aggiuntivi. Per tutti gli studi La probabilità stimata dei pazienti che utilizzano trattamenti aggiuntivi per le loro emicranie per le 24 ore successive alla singola dose di 2 mg di trattamento dello studio è riassunta nella Figura 3 di seguito.
Figura 3 Probabilità stimata di un paziente che utilizza trattamenti aggiuntivi per l'emicrania per le 24 ore successive a spruzzo nasale di diidroergotamina mesilato 2 mg (o placebo)*
| *Grafico Kaplan-Meier basato sui dati ottenuti da tutti gli studi con pazienti che non utilizzano trattamenti aggiuntivi censurati a 24 ore. Tutti i pazienti hanno ricevuto un singolo trattamento di farmaci per lo studio per il loro attacco di emicrania. La trama include anche pazienti che non hanno avuto risposta alla dose iniziale. |
Né l'età né il sesso sembrano influenzare la risposta del paziente allo spray nasale mesilato di diidroergotamina. La distribuzione razziale dei pazienti era insufficiente per determinare l'effetto della razza sull'efficacia dello spray nasale di diidroergotamina mesilato.
Informazioni sul paziente per Trudhesa
Trusta ™
(trae - deh - uno)
(diidroergotamina mesilato) spray nasale
Quali sono le informazioni più importanti che dovrei sapere su Trudhesa?
Trudhesa può causare gravi effetti collaterali tra cui:
- Gravi problemi con la circolazione sanguigna alle gambe e ai piedi (ischemia periferica). Trudhesa può causare ischemia periferica quando la prendi con determinati medicinali noti come inibitori del CYP3A4. L'ischemia periferica può portare a un ictus e morte. Smetti di prendere Trudhesa e ottenere subito assistenza medica di emergenza se hai uno dei seguenti sintomi:
- Crampi e dolore alle gambe o ai fianchi
- Sensazione di pesantezza o tenuta nei muscoli delle gambe
- bruciare o dolorare dolore ai piedi o ai piedi durante il riposo
- intorpidimento formicolio o debolezza nelle gambe
- La sensazione fredda o il colore cambiano in 1 o entrambe le gambe o i piedi
- discorso confuso
- debolezza improvvisa
Non assumere medicinali noti come forti inibitori del CYP3A4 come:
-
- Ritonavir
- eritromicina
- ketoconazolo
- Netfinavir
- Claritromicina
- itraconazolo
Queste non sono tutte le medicine che potrebbero influenzare il funzionamento di Trudhesa. Il tuo operatore sanitario può dirti se è sicuro prendere Trudhesa con altri medicinali.
Cos'è Trudhesa?
Trudhesa è un medicinale di prescrizione utilizzata per il trattamento acuto dell'emicrania con o senza aura negli adulti.
- Trudhesa non è usato per prevenire l'emicrania.
- Trudhesa non è usato per trattare altri tipi di mal di testa come emiplegico (che ti rendono incapace di muoverti su un lato del corpo) o basilare (rara forma di emicrania con aura).
Non è noto se Trudhesa è sicuro ed efficace nei bambini.
Non prendere Trudhesa se tu:
- stanno assumendo medicinali noti come forti inibitori del CYP3A4.
- Avere problemi cardiaci o una storia di problemi cardiaci.
- hanno una pressione arteriosa incontrollata.
- ha un restringimento dei vasi sanguigni nella pancia o nei reni delle gambe (malattia vascolare periferica).
- avere sepsi.
- hanno subito un intervento chirurgico vascolare.
- avere gravi problemi epatici.
- avere gravi problemi renali.
- sono allergici a alcaloidi Ergot mesilato di diidroergotamina o qualsiasi ingredienti a Trudhesa. Vedi la fine di questa guida ai farmaci per un elenco completo di ingredienti.
- hanno preso uno dei seguenti medicinali nelle ultime 24 ore:
- Sumatriptan
- Almotriptan
- Eletriptan
- frovatriptato
- Naratriptan
- Rizatriptan
- medicine di tipo ergotamina o ergotamina
- hanno assunto eventuali medicinali che restringono i vasi sanguigni o aumentano la pressione sanguigna.
Chiedi al tuo medico se non sei sicuro di prendere una di queste medicine. Il tuo operatore sanitario può dirti se è sicuro prendere Trudhesa con altri medicinali.
Prima di prendere Trudhesa, racconta al tuo operatore sanitario su tutte le tue condizioni mediche, anche se tu:
- avere la pressione alta.
- avere problemi epatici.
- avere problemi ai reni.
- fumo.
- sono incinta o prevedono di rimanere incinta. Trudhesa può causare manodopera pretermine. Trudhesa dovrebbe essere evitato durante la gravidanza. Parla immediatamente con il tuo operatore sanitario se sei incinta o vuoi rimanere incinta.
- stanno allattando o pianificano di allattare. Trudhesa può ridurre l'approvvigionamento di latte materno e passare nel latte materno. Trudhesa può essere dannoso per il tuo bambino. Non allattare il tuo bambino mentre prendi Trudhesa e per 3 giorni dopo aver usato Trudhesa. Parla con il tuo operatore sanitario del modo migliore per nutrire il tuo bambino se prendi Trudhesa.
Di 'al tuo operatore sanitario di tutte le medicine che prendi tra cui prescrizione e medicine da banco vitamine e integratori a base di erbe. Il tuo operatore sanitario deciderà se puoi prendere Trudhesa con le altre medicine.
Soprattutto dì al tuo operatore sanitario se prendi:
-
- Sumatriptan
- fluconazolo
- propranololo o altri medicinali che possono abbassare la frequenza cardiaca
- medicina di tipo ergot o succo di pompelmo o qualsiasi medicinali che possano aumentare la pressione sanguigna
- saqinavir o zileuton o serotonina selettiva Reuppake inibitori
- nefazodone
- nicotina
Queste non sono tutte le medicine che potrebbero influenzare il funzionamento di Trudhesa. Il tuo operatore sanitario può dirti se è sicuro prendere Trudhesa con altri medicinali.
Come dovrei prendere Trudhesa?
- Alcune persone dovrebbero prendere la loro prima dose di Trudhesa nell'ufficio del proprio medico o in un altro contesto medico. Chiedi al tuo medico se dovresti prendere la prima dose in un ambiente medico.
- Usa Trudhesa esattamente come il tuo operatore sanitario ti dice di usarlo. Leggere e seguire le istruzioni in Istruzioni per l'uso che è fornito con il pacchetto Trudhesa prima di utilizzare.
- Dovresti usare Trudhesa non appena iniziano i sintomi del mal di testa, ma può essere somministrato in qualsiasi momento durante un'emicrania.
- Dopo aver messo insieme Trudhesa e innescare lo spruzzo del dispositivo 1 volta in ogni narice (una dose completa).
- Se il tuo mal di testa torna dopo la prima dose completa o ricevi solo un po 'di rilievo dal mal di testa, puoi usare una seconda dose 1 ora dopo la prima dose completa. Utilizzare un nuovo dispositivo spray nasale Trudhesa per la seconda dose.
- Non utilizzare più di 2 dosi di Trudhesa in un periodo di 24 ore o 3 dosi in un periodo di 7 giorni.
- Se usi troppo Trudhesa, chiama subito il tuo medico o vai al pronto soccorso dell'ospedale più vicino.
- Prendere Trudhesa per 10 o più giorni in 1 mese può peggiorare il mal di testa. Dovresti scrivere quando hai mal di testa e quando prendi Trudhesa in modo da poter parlare con il tuo operatore sanitario su come Trudhesa funziona per te.
Quali sono i possibili effetti collaterali di Trudhesa?
Trudhesa può causare gravi effetti collaterali tra cui:
Vedere Quali sono le informazioni più importanti che dovrei sapere su Trudhesa?
- Attacco di cuore e altri problemi cardiaci. I problemi cardiaci possono portare alla morte. Smetti di prendere Trudhesa e ottenere subito assistenza medica di emergenza se hai uno dei seguenti sintomi di a attacco di cuore :
- disagio al centro del petto che dura più di qualche minuto o che scompare e torna indietro
- grave tenuta che pressione del dolore o pesantezza nella gola del petto o mascella
- dolore o disagio tra le braccia posteriori della mascella o dello stomaco
- mancanza di respiro con o senza disagio al torace
- scoppiare con un sudore freddo
- nausea or vomito
- sentirsi stordito
Trudhesa non è per le persone con fattori di rischio per le malattie cardiache a meno che non venga fatto un esame cardiaco e non mostra alcun problema. Hai un rischio più elevato per le malattie cardiache se tu:
-
- Avere la pressione alta
- hanno alti livelli di colesterolo
- fumo
- sono in sovrappeso
- avere il diabete
- avere una storia familiare di malattie cardiache
- Colpo. Smettila di prendere Trudhesa e ottenere subito assistenza medica di emergenza se hai uno dei seguenti sintomi di ictus:
- faccia a faccia
- debolezza insolita o intorpidimento
- discorso confuso
- Cambiamenti di colore o sensazione nelle dita delle dita e delle dita dei piedi (sindrome di Raynaud).
- Problemi di stomaco e intestinali (Eventi ischemici gastrointestinali e colonici). I sintomi di eventi ischemici gastrointestinali e colonici includono:
- Dolori allo stomaco improvviso o grave
- costipazione o diarrea
- Dolori allo stomaco dopo i pasti
- Diarrea sanguinosa
- perdita di peso
- febbre
- nausea or vomito
- Aumentare la pressione sanguigna.
- Medicinale eccessivo di mal di testa. Alcune persone che usano troppo Trudhesa possono peggiorare il mal di testa (medicina eccessivamente mal di testa). Se i tuoi mal di testa peggiorano il tuo operatore sanitario può decidere di fermare il trattamento con Trudhesa.
- Lavoro pretermine.
- Cambiamenti dei tessuti (complicanze fibrotiche). NFLAMMAZIONE E TESSUE SIBRO COMPLETO NON NORMARE (Fibrosi) può verificarsi attorno ai polmoni e allo stomaco.
- Bruciare sentimenti nella bocca e nella gola e nel gusto anormale.
Gli effetti collaterali più comuni di Trudhesa includono:
- rinorrea
- Reazioni del sito dell'applicazione
- sonnolenza
- nausea
- vertigini
- mal di gola
- gusto anormale
- vomito
- diarrea
Questi non sono tutti i possibili effetti collaterali Trudhesa.
Chiama il medico per consigli medici sugli effetti collaterali. È possibile segnalare gli effetti collaterali alla FDA al numero 1-800-FDA-1088.
Come dovrei conservare Trudhesa?
Tieni Trudhesa lontano dal calore e dalla luce.
- Conservare Trudhesa a temperatura ambiente compresa tra 68 ° F e 77 ° F (da 20 ° C a 25 ° C).
- Non refrigerare o congelare.
- Dopo che è stata aperta una fiala di Trudhesa, deve essere gettata via dopo 8 ore.
Mantieni Trudhesa e tutti i medicinali fuori dalla portata dei bambini.
Non gettare Trudhesa in fuoco o inceneritori poiché il contenitore all'interno del dispositivo può esplodere.
Informazioni generali sull'uso sicuro ed efficace di Trudhesa.
Le medicine sono talvolta prescritte a fini diversi da quelli elencati in una guida ai farmaci. Non usare Trudhesa per una condizione per la quale non è stata prescritta. Non dare Trudhesa ad altre persone anche se hanno gli stessi sintomi che hai. Potrebbe danneggiare loro. Puoi chiedere al tuo farmacista o operatore sanitario informazioni su Trudhesa che è scritto per gli operatori sanitari.
Quali sono gli ingredienti di Trudhesa?
Ingrediente attivo: Diidroergotamina mesilato
Ingredienti inattivi: Destrosio e acqua di anidride carbonica di caffeina. Il contenitore del dispositivo spray nasale contiene propellente Hydrofluoroalkane-134A (HFA). Il tappo della fiala non è realizzato con lattice in gomma naturale. Trudhesa è un marchio di Impel Neuropharma Inc.
Questa guida ai farmaci è stata approvata dalla Food and Drug Administration degli Stati Uniti.
Istruzioni per l'uso
Trusta ™
(Roe-SA)
(diidroergotamina mesilato)
spray nasale
Solo per uso nasale
Introduzione
Leggi queste istruzioni da utilizzare prima di iniziare a utilizzare Trudhesa e ogni volta che si ottiene una ricarica di prescrizione. Ci possono essere nuove informazioni.
Queste informazioni non prendono il posto di parlare con il proprio operatore sanitario sulla condizione medica o sul trattamento. Tu e il tuo operatore sanitario dovreste parlare di Trudhesa quando inizi a prenderlo e ai controlli regolari.
È importante seguire con precisione queste direzioni per ricevere la dose corretta. Contatti il tuo fornitore di assistenza sanitaria se hai domande su come utilizzare questo prodotto.
 |
Parti del dispositivo spray nasale
 |
Parti di fiala di vetro
 |
Informazioni importanti che devi sapere prima di dosarsi con Trudhesa
- Solo per uso nasale.
- Adepisce sempre il dispositivo spray nasale prima di dosarsi pompando le impugnature e la fiala di vetro insieme esattamente 4 volte
- Lo scopo del innesco è quello di portare la medicina sulla punta dell'ugello spray. Puoi o meno vedere liquido o spruzzo uscire dall'ugello durante ogni azione di innesco.
- Durante il primingmake sicuramente punta l'ugello spray lontano dal tuo viso e tutto ciò che non si desidera entrare in contatto con lo spruzzo della medicina.
- Una dose completa è di 2 spray; 1 spruzzo in ogni narice.
- Non farlo Prendi più di 2 dosi in un periodo di 24 ore. Non farlo Prendi più di 3 dosi in un periodo di 7 giorni.
- Tenere sempre il dispositivo spray nasale perfettamente in posizione verticale durante l'adempimento e durante il dosaggio.
- Non è necessario annusare durante il dosaggio. Tuttavia, non ti farà male né renderà la medicina meno efficace.
- Questo prodotto di dispositivo spray nasale è monodose (per una sola dose completa) e dovrebbe essere gettato via (scartato) dopo l'uso. Avrà bisogno di un nuovo kit per ogni dose.
- Mantieni il prodotto nel caso fino a quando non è pronto per l'uso.
- Dopo che una fiala di Trudhesa è stata aperta dopo 8 ore.
- Non farlo Apri la fiala di vetro ed esporre all'aria fino a quando non è pronto per l'uso.
- Conservare a temperatura ambiente in un'area asciutta pulita.
- Non farlo Utilizzare se il prodotto è danneggiato.
- Non farlo Utilizzare se il prodotto è scaduto.
- Ogni flitallo di vetro e dispositivo spray nasale può essere utilizzato solo 1 volta. Getta via l'intero dispositivo di spruzzo nasale dopo il dosaggio senza rimuovere la fiala di vetro.
- Puoi assumere un'altra dose completa almeno 1 ora dopo la prima dose se i sintomi persistono.
Memorizzando Trudhesa
- Conservare Trudhesa a temperatura ambiente compresa tra 68 ° F e 77 ° F (da 20 ° C a 25 ° C).
- Conservare Trudhesa nella confezione originale in una zona di pulizia lontano da calore e luce ( Figura A. ).
- Mantieni Trudhesa nella confezione originale fino a quando non sei pronto per l'uso.
- Non farlo Refrigerare o congelare Trudhesa.
- Mantieni Trudhesa e tutti i medicinali fuori dalla portata dei bambini.
 |
Prepararsi a dosare con Trudhesa
Passaggio 1: raccogliere e controllare le forniture
 |
 |
- Controlla per assicurarti di usare la medicina giusta per la tua emicrania (vedi Figura b ).
- Verifica assicurarsi che Trudhesa non sia scaduto (Exp) (vedi Figura c ).
- Se scatenato e prendi una nuova fiala di vetro.
- Controllare che il coperchio in plastica blu e blu di vetro non sembri danneggiati.
Passaggio 2: rimuovere il foglio di covermetale in plastica blu e tappo di gomma grigio da fiala di vetro
 |
 |
 |
- Rimuovere (capovolgere) il coperchio in plastica blu dalla fiala di vetro (vedi Figura d ).
- Usa il coperchio in plastica blu per staccare lentamente la lamina di metallo dal tappo di gomma grigio con un movimento circolare (vedi Figura E. ).

- Tirare il tappo di gomma grigio su e uscire dalla fiala di vetro ( Figura f E Figura g ).
- Getta via (scartare) il foglio e il tappo di gomma grigio nella spazzatura.
Passaggio 3: rimuovere il coperchio in plastica trasparente dal dispositivo spray nasale
- Tenere il dispositivo nasale SPPray in posizione verticale.
- Abbassare il coperchio in plastica trasparente e rimuoverlo dal dispositivo spray nasale ( Figura h ).
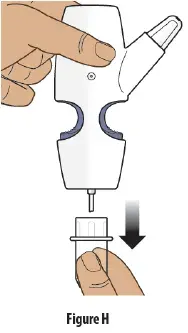
- Getta via la cara copertina di plastica.
Passaggio 4: avvitare la fiala di vetro nel dispositivo spray nasale
 |
 |
- Tenere il dispositivo spray nasale in posizione verticale.
- Spingere delicatamente la fiala di vetro nella parte inferiore del dispositivo nasale sparay (vedi Figura I. ) e avvitarlo fino a quando non viene fissato come mostrato in Figura j .
Passaggio 5: accompagnare il dispositivo spray nasale pompando quattro volte con le dita e il pollice
 |
- Tenere il dispositivo spray nasale in posizione verticale .
- Punta l'ugello spray lontano dal tuo viso.
- Posizionare il pollice sul fondo della fiala di vetro e posizionare il puntatore (indice) e le dita centrali sulle impugnature (vedi Figura k ).
- Pompare il dispositivo di spruzzo nasale esattamente 4 volte.
- Per pompare il dispositivo di spruzzo nasale premi saldamente le prese di dito e premi la fiala di vetro allo stesso tempo. Quindi rilascio (vedi Figura k )
- Potresti vedere alcuni medicinali spruzzare durante l'adescamento. Questo è normale. Va bene se non vedi la medicina spruzzata sulle prime pompe.
Suggerimento importante: Lo scopo del innesco è portare la medicina sulla punta dell'ugello di spruzzo. Se non si esegue il dispositivo spray nasale, non otterrai la dose corretta di medicina.
Adepisce sempre il dispositivo spray nasale prima dell'uso mediante pompaggio esattamente 4 volte.
Durante il priming assicurati di puntare l'ugello dal tuo viso e qualsiasi cosa tu non voglia entrare in contatto con lo spruzzo della medicina.
Usando Trudhesa
Passaggio 6: posizionare il dispositivo spray nasale
 |
- Ruota o ribadisci il dispositivo di grazia nasale in modo che l'ugello spray ti rivolga.
- Assicurati che la testa sia dritta e che il dispositivo spray nasale sia in posizione verticale.
- Inserisci l'ugello di Sparay nella tua prima narice per quanto riguarda la comodità (vedi Figura l ).
Passaggio 7: spruzzare il primo spray in 1 narice
- Premere saldamente le impugnature per le dita e premere la fiala di vetro allo stesso tempo per consegnare il primo spray (vedi Figura m ).Then release.
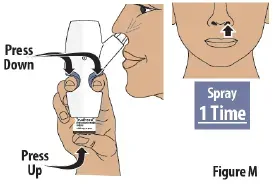
- Fornire solo 1 spruzzo in questa narice.
Passaggio 8: spruzzare il secondo spray in altra narice
- Sposta l'ugello di spruzzo nell'altra tua narice.
- Premere saldamente le impugnature per le dita e premere la fiala di vetro allo stesso tempo per consegnare il secondo spray (vedi Figura n ).Then release.
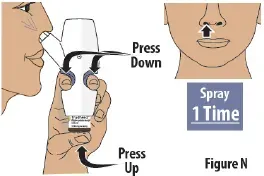
- Fornire solo 1 spruzzo in questa narice.
Suggerimento importante: Una dose completa è di 2 spray; 1 spruzzo in ogni narice.
puoi prendere l'ibuprofene con meclizina
Non farlo Prendi più di 2 dosi in un periodo di 24 ore. Non farlo Prendi più di 3 dosi in un periodo di 7 giorni.Please refer to the prescribing information for more information.
Non è necessario annusare mentre o dopo il dosaggio. Tuttavia, non ti farà male o renderà il medicinale meno efficace.
Importanti domande frequenti (FAQ)
Domanda: posso salvare la medicina saltando le 4 pompe in Passaggio 5: Primano il dispositivo spray nasale?
Risposta: Non saltare le 4 pompe per innescare il dispositivo di spruzzo nasale può comportare che non si ottiene la dose corretta di medicina.
Qestion: quando ho pompato per la prima volta il dispositivo spray nasale per innescare nulla sembrava accadere. Perché?
Risposta: Lo scopo dell'innesco è quello di portare la medicina sulla punta dell'ugello. Anche se potresti non vedere o ascoltare nulla sulla tua prima pompa o due, l'azione di pompaggio sposterà il medicinale dalla fiala di vetro attraverso l'interno del dispositivo spray nasale e nell'ugello. Dovresti vedere uno spray dal quarto tentativo di pompa. Prime solo pompando esattamente 4 volte prima del dosaggio.
Domanda: posso riutilizzare il dispositivo spray nasale con una nuova fiala di vetro?
Risposta: Il dispositivo spray nasale non è solo per uso una tantum e deve essere gettato via dopo aver chiuso (1 spruzzo in ogni narice). Questo è perché il dispositivo può ostruire. Dopo aver dosata la fiala di vetro avvitata sul dispositivo di spruzzo nasale e gettare via il dispositivo spray nasale assemblato nel cestino. Non riciclare nessuna parte del prodotto.
Domanda: posso usare la medicina che rimane nella fiala di vetro per una dose successiva?
Risposta: NOALTUA, sebbene sia nrmal che alcuni medicinali rimangano nella fiala di vetro, non può essere utilizzato per il successivo dosaggio. Qualsiasi medicina rimanente diventerà inefficace.
Domanda: cosa succede se spara più di una volta nella stessa narice?
Risposta: Una dose completa e corretta è uno spruzzo in ogni narice. Non dose in te Altro Nostril Se hai già spruzzato due volte in una narice. Rapido al tuo fornitore di assistenza sanitaria se hai l'irritale da moderato a grave nel naso o cambia di odore.
Domanda: quanto tempo posso prendere un'altra dose se non ricevo sollievo dalla mia emicrania?
Risposta: Puoi prendere un'altra dose almeno 1 ora dopo la prima dose di Youar se i sintomi persistono. Non farlo Prendi più di 2 dosi in un periodo di 24 ore. Non farlo Prendi più di 3 dosi in un periodo di 7 giorni.Please refer to the prescribing information for more information.
Queste istruzioni per l'uso sono state approvate dalla U.S.Food and Drug Administration.




