Le Informazioni Presenti Sul Sito Non Costituiscono Consulenza Medica. Non Vendiamo Nulla. L'Accuratezza Della Traduzione Non È Garantita. Disclaimer
AminoglicosidiArikayce
Riepilogo della droga
Cos'è Arikayce?
Arikayce (sospensione dell'inalazione del liposoma amikacina) è un aminoglicoside antibatterico Indicato negli adulti che hanno opzioni di trattamento alternative limitate o nessuna per il trattamento della malattia polmonare del complesso di Mycobacterium avium (MAC) come parte di un regime di farmaci antibatterici combinati in pazienti che non raggiungono colture di espettorato negativo dopo un minimo di 6 mesi consecutivi di una terapia di regime di fondo multidrug. Questo farmaco è indicato per l'uso in una popolazione limitata e specifica di pazienti.
Quali sono gli effetti collaterali di Arikayce?
Arikayce
- orticaria
- Difficoltà a respirare
- gonfiore della lingua o della gola
- tosse (specialmente durante il primo mese di utilizzo del farmaco)
- difficoltà a parlare
- squillando nelle orecchie
- cambiamenti nell'udito
- vertigini
- sensazione di rotazione
- Accendino
- tenuta toracica
- sibilante
- fiato corto
- tossire sangue
- poca o nessuna minzione
- gonfiore in piedi o caviglie e
- stanchezza
Ottieni subito assistenza medica se hai uno qualsiasi dei sintomi sopra elencati.
Gli effetti collaterali comuni di Arikayce includono:
- Difficoltà a parlare
- tosse
- broncospasmo
- tossire sangue
- danni all'orecchio interno
- Irritazione delle vie aeree superiori
- dolore muscoloscheletrico
- fatica
- debolezza
- peggioramento della malattia polmonare sottostante
- diarrea e
- nausea
Cerca cure mediche o chiama il 911 contemporaneamente se hai i seguenti gravi effetti collaterali:
- Sintomi di occhiali gravi come la perdita di visione improvvisa del tunnel della visione sfocata Dolore alla visione o gonfiore o vedere aloni attorno alle luci;
- Sintomi cardiaci gravi come battiti cardiaci irregolari o martellanti veloci; svolazzando nel petto; fiato corto; e improvviso vertigini giuria o svenuta;
- Grave mal di testa confusione Il braccio del linguaggio bloccato o la debolezza delle gambe problemi perdite perdita di coordinamento sentendoti instabili muscoli molto rigidi ad alta febbre abbondante sudorazione o tremori.
Questo documento non contiene tutti i possibili effetti collaterali e altri possono verificarsi. Verificare con il tuo medico ulteriori informazioni sugli effetti collaterali.
Dosaggio per Arikayce
Il dosaggio raccomandato di Arikayce negli adulti è una volta un'inalazione orale giornaliera del contenuto di una fiala Arikayce da 590 mg/8,4 ml. Usa i fiale di Arikayce solo con il sistema di nebulizzatore Lamira.
Quali sostanze o integratori di farmaci interagiscono con Arikayce?
Arikayce può interagire con l'acido etacrynico furosemide urea mannitolo endovenoso o farmaci associati alla nefrotossicità e all'ototossicità della neurotossicità. Dì al medico tutti i farmaci e gli integratori che usi.
Arikayce durante la gravidanza o l'allattamento
Di 'al medico se sei incinta o hai intenzione di rimanere incinta prima di usare Arikayce; Può danneggiare un feto. Non è noto se Arikayce passa nel latte materno. Consulta il medico prima dell'allattamento al seno.
Ulteriori informazioni
La nostra sospensione dell'inalazione di liposoma Arikayce (Arikacina) per inalazione orale utilizzato per gli effetti collaterali del Centro farmacologico fornisce una visione completa delle informazioni disponibili sui farmaci sui potenziali effetti collaterali durante l'assunzione di questo farmaco.
Informazioni sui farmaci FDA
- Descrizione del farmaco
- Indicazioni
- Dosaggio
- Effetti collaterali
- Avvertimenti
- Overdose
- Farmacologia clinica
- Guida ai farmaci
AVVERTIMENTO
Rischio di aumento delle reazioni avverse respiratorie
Arikayce è stato associato ad un aumentato rischio di reazioni avverse respiratorie, tra cui l'ipersensibilità alla polmonite emoptysi Broncospasmo esacerbazione di malattie polmonari sottostanti che hanno portato a ricoveri in alcuni casi [vedi AVVERTIMENTOS AND PRECAUZIONI ].
Descrizione per Arikayce
L'ingrediente attivo in Arikayce (sospensione dell'inalazione del liposoma amikacina) è l'amikacina solfato USP un antibatterico aminoglicosidico. Il suo nome chimico è D-streptamina O -3-ammino-3-deossi-α-dglucopiranosil- (1 → 6)- O -[6-ammino-6-deossi-α-d-glucopiranosil- (1 → 4)]- N 1 -(4-ammino-2-idrossi-1oxobutil) -2-deoxy- ( S )- solfato (1: 2) sale con una formula chimica di C 22 H 43 N 5 O 13 • 2h 2 COSÌ 4 con un peso molecolare di 781,76. La sua formula strutturale è:
 |
Arikayce è una sospensione latte bianca costituita da amikacina solfato incapsulata nei liposomi ed è fornita in una fiala di vetro trasparente da 10 ml di limpida unitaria contenente amikacina 590 mg/8,4 ml (equivalente all'amikacina solfato 623 mg/8,4 ml) come sospensione di difficoltà acquosa sterica per diffamazione. Arikayce è costituito da amikacina solfato incapsulato nei liposomi a una concentrazione mirata di 70 mg di amikacina/mL con l'intervallo di pH da 6,1 a 7,1 e un rapporto di peso lipidico -amikacina nell'intervallo da 0,60 a 0,79. Gli ingredienti inattivi sono il colesterolo dipalmitoilfosfatidilcolina (DPPC) cloruro di sodio idrossido di sodio (per regolazione del pH) e acqua per iniezione.
Arikayce viene somministrato solo usando un sistema di nebulizzatore Lamira [vedi Dosaggio e amministrazione ]. Like all other nebulized treatments the amount delivered to the lungs will depend upon patient factOs. Under stEardized in vitro Test per USP <1601> Pattern di respirazione per adulti (500 ml di volume di marea 15 respiri al minuto e inalazione: rapporto di espirazione di 1: 1) La dose media consegnata dal bocchino era di circa 312 mg di amikacin solfato (53% della rivendicazione dell'etichetta). Il diametro aerodinamico mediano di massa (MMAD) delle goccioline di aerosol nebulizzata è di circa 4,7 μm (NULL,1 - 5,3 μm) determinato usando il metodo di Impactorringor (NGI) di successiva generazione. Una percentuale di amikacina nel liposoma viene rilasciata dal processo di nebulizzazione, quindi Arikayce nebulizzato offre una combinazione di amikacina libera e liposomiale.
Usi per Arikayce
Popolazione limitata: Arikayce ® è indicato negli adulti che hanno opzioni di trattamento alternative o nessuna alternativa per il trattamento di Mycobacterium avium La malattia polmonare complessa (MAC) come parte di un regime di farmaci antibatterici combinati in pazienti che non ottengono colture di espettorato negative dopo almeno 6 mesi consecutivi di una terapia di regime di fondo multidrug. Dato che solo i dati limitati di sicurezza clinica ed efficacia per Arikayce sono attualmente disponibili Arikayce di riserva per l'uso negli adulti che hanno opzioni di trattamento limitate o non alternative. Questo farmaco è indicato per l'uso in una popolazione limitata e specifica di pazienti.
Questa indicazione è approvata in base all'approvazione accelerata in base al raggiungimento della conversione della coltura dell'espettorato (definita come 3 colture di espettorato mensile negativa consecutive) entro il mese 6. Il beneficio clinico non è stato ancora stabilito [vedi Studi clinici ]. Continued approval fO this indication may be contingent upon verification E description of clinical benefit in confirmatOy trials.
Limitazione dell'uso
Arikayce è stato studiato solo in pazienti con malattia polmonare Mac refrattaria definita come pazienti che non hanno raggiunto colture di espettorato negativo dopo un minimo di 6 mesi consecutivi di una terapia di regime di fondo multidrug. L'uso di Arikayce non è raccomandato per i pazienti con malattia polmonare MAC non refrattaria.
Dosaggio per Arikayce
Importanti istruzioni di amministrazione
Arikayce è solo per uso di inalazione orale. Somministrare solo mediante nebulizzazione con la lamira ® Sistema di nebulizzatore. Fare riferimento alle istruzioni per l'uso per informazioni sull'amministrazione completa sull'uso di Arikayce con il sistema di nebulizzatore Lamira.
Indiicare ai pazienti che usano un broncodilatatore (allevia) di utilizzare prima il broncodilatatore in seguito al volantino del broncodilatore per l'uso delle informazioni prima di utilizzare Arikayce.
Il pretrattamento con agonisti beta-2 selettivi a breve durata deve essere preso in considerazione per i pazienti con malattia delle vie aeree iperreattive note cronica ostruttiva asma o broncospasmo [vedi AVVERTIMENTOS AND PRECAUZIONI ].
Dosaggio consigliato
Il dosaggio raccomandato di Arikayce negli adulti è una volta l'inalazione quotidiana del contenuto di una fiala Arikayce da 590 mg/8,4 ml (590 mg di amikacina) usando il sistema di nebulizzatore Lamira [vedi Studi clinici ].
Amministrare Arikayce solo con il sistema di nebulizzatore Lamira. Arikayce dovrebbe essere a temperatura ambiente prima dell'uso. Prima di aprire Shake the Arikayce Fial Well per almeno 10-15 secondi fino a quando il contenuto appare uniforme e ben miscelato. La fiala di Arikayce viene aperta lanciando la parte superiore della plastica della fiala, quindi tirando verso il basso per allentare l'anello di metallo. L'anello di metallo e il tappo di gomma devono essere rimossi con cura. Il contenuto della fiala di Arikayce può quindi essere versato nel serbatoio del farmaco del portatile del nebulizzatore.
Se una dose giornaliera di Arikayce viene mandata, somministrare la dose successiva il giorno successivo. Non raddoppiare la dose per compensare la dose persa.
Come fornito
Dosaggio FOms And Strengths
Arikayce viene fornito come una sospensione di liposoma acquosa bianca bianca sterile per inalazione orale in una fiala di vetro a dosi unitaria contenente amikacina 590 mg/8,4 ml (equivalente all'amikacina solfato 623 mg/8,4 ml).
Arikayce (Sospensione per inalazione di liposoma amikacina) 590 mg/8,4 mL è fornito in una fiala di vetro da 10 ml di dose unile. Il prodotto viene erogato come un kit a 28 volte.
Ogni cartone contiene una fornitura di medicinali a 28 giorni (28 fiale). Oltre alle fiale di Arikayce nel portatile del nebulizzatore di Carton One Lamira e sono fornite quattro teste di aerosol Lamira.
Ndc 71558-590-28
Il sistema di nebulizzatore Lamira contiene un controller una testa di aerosol di riserva un cavo di alimentazione e accessori per ricevitori di riserva.
Archiviazione e maneggevolezza
Conservare le fiale di Arikayce refrigerate da 2 ° C a 8 ° C (da 36 ° F a 46 ° F) fino alla data di scadenza su Fial. Non congelare . Una volta scaduto, scartare qualsiasi farmaco inutilizzato.
Arikayce can be stOed at room temperature up to 25°C (77°F) fO up to 4 weeks. Once at room temperature any unused drug must be discarded at the end of 4 weeks.
Prodotto per: Insmed Incorporated 700 US Highway 202/206 Bridgewater NJ 08807-1704. Revisionato: febbraio 2023
Effetti collaterali per Arikayce
Le seguenti reazioni avverse clinicamente significative sono descritte in modo più dettagliato in altre sezioni di etichettatura:
- Pneumonite da ipersensibilità [vedi Avvertenza della scatola E AVVERTIMENTOS AND PRECAUZIONI ]
- Emoptysi [vedi Avvertenza della scatola E AVVERTIMENTOS AND PRECAUZIONI ]
- Bronchospasm [vedi Avvertenza della scatola E AVVERTIMENTOS AND PRECAUZIONI ]
- Esacerbazione della malattia polmonare sottostante [vedi Avvertenza della scatola E AVVERTIMENTOS AND PRECAUZIONI ]
- Reazioni di anafilassi e ipersensibilità [vedi AVVERTIMENTOS AND PRECAUZIONI ]
- Ototossicità [vedi AVVERTIMENTOS AND PRECAUZIONI ]
- Nefrotossicità [vedi AVVERTIMENTOS AND PRECAUZIONI ]
- Blocco neuromuscolare [vedi AVVERTIMENTOS AND PRECAUZIONI ]
Esperienza di studi clinici
Poiché gli studi clinici sono condotti in condizioni di reazione avverse ampiamente variabili osservate negli studi clinici di un farmaco non possono essere paragonati direttamente ai tassi negli studi clinici di un altro farmaco e potrebbero non riflettere i tassi osservati nella pratica.
Panoramica degli studi clinici per la valutazione della sicurezza
All'interno del programma clinico NTM refrattario 404 pazienti che hanno partecipato a tre studi clinici sono stati trattati con Arikayce alla dose di 590 mg/die (la durata mediana dell'esposizione ad Arikayce è stata di 236,5 giorni).
Prova 1 (NCT Mycobacterium avium Malattia polmonare complessa (MAC). I pazienti sono stati randomizzati a 8 mesi di Arikayce più un regime di fondo (n = 223) o solo regime di fondo (n = 112).
Prova 2 (NCT
Prova 3 (NCT Mycobacterium . I pazienti sono stati randomizzati nel regime di sfondo Arikayce più (n = 44) o un regime di sfondo di liposoma vuoto diluito inalato più regime di fondo (n = 45) per 84 giorni.
In tutti gli studi clinici di pazienti con e senza infezione polmonare NTM refrattaria 818 pazienti sono stati esposti a dosi multiple di Arikayce.
Reazioni avverse che portano alla sospensione del trattamento
Nei tre studi NTM c'è stata una maggiore incidenza di interruzione prematura di Arikayce. Nella sperimentazione 1 34,5% ha interrotto prematuramente Arikayce; La maggior parte erano dovute a reazioni avverse (NULL,8%) e ritiro per soggetto (NULL,9%). Nel braccio del comparatore il 10,7% dei soggetti ha interrotto il proprio regime di fondo con lo 0,9% a causa di reazioni avverse e il 5,4% a causa del ritiro per soggetto. Nella sperimentazione 2 (l'estensione a braccio singolo della sperimentazione 1) il 37,8% dei pazienti a partire da Arikayce si è interrotto prematuramente con il 24,4% che si è interrotto a causa di reazioni avverse. Nella sperimentazione 3 Tutti e 9 (NULL,5%) si sono verificati interruzioni premature nei pazienti trattati con il regime di fondo Arikayce più e non ci sono stati interruzioni premature nel braccio del regime di fondo placebo più.
Reazioni avverse gravi nelle prove 1 e 3
Nella sperimentazione 1 19,7% dei pazienti trattati con il regime di fondo Arikayce Plus ha riportato SAR rispetto al 16,1% dei pazienti trattati con il solo regime di fondo. Inoltre, nella sperimentazione 1 [2 a 1 randomizzazione arikayce più regime di fondo rispetto al solo regime di fondo] ci sono stati 80 ricoveri in ospedale in 41 pazienti (NULL,4%) trattati con il regime di fondo Arikayce Plus rispetto a 29 ricoveri in ospedale in 15 pazienti (NULL,4%) trattati con solo regime di fondo. Le SAR e le ragioni più comuni per il ricovero in ospedale nel braccio del regime di fondo Arikayce Plus erano correlate all'esacerbazione delle malattie polmonari sottostanti e alle infezioni del tratto respiratorio inferiore come la polmonite. Nello studio 3 18,2% dei pazienti trattati con il regime di fondo Arikayce Plus ha riportato SARS rispetto all'8,9% dei pazienti trattati con regime di fondo più placebo inalato.
Reazioni avverse comuni
L'incidenza delle reazioni avverse nella prova 1 sono visualizzate nella Tabella 1. Sono mostrate solo quelle reazioni avverse con un tasso di almeno il 5% nel gruppo di regime di sfondo Arikayce Plus e maggiore del gruppo di reggisimi di fondo da solo.
Tabella 1: reazioni avverse in ≥ 5% dei pazienti MAC trattati con Arikayce e più frequenti del solo regime di fondo nella sperimentazione 1
| Reazione avversa | Arikayce plus Background Regimen (N = 223) N (%) | Regime di fondo da solo (N = 112) N (%) |
| Disfonia a | 106 (48) | 2 (2) |
| Tosse b | 88 (40) | 19 (17) |
| Broncospasmo c | 64 (29) | 12 (11) |
| Emottisi | 41 (18) | 15 (13) |
| Dolore muscoloscheletrico d | 40 (18) | 10 (9) |
| Irritazione delle vie aeree superiori e | 39 (18) | 2 (2) |
| Elituità f | 38 (17) | 11 (10) |
| Affaticamento e astenia | 36 (16) | 11 (10) |
| Esacerbazione della malattia polmonare sottostante g | 34 (15) | 11 (10) |
| Diarrea | 28 (13) | 5 (5) |
| Nausea | 26 (12) | 4 (4) |
| Mal di testa | 22 (10) | 5 (5) |
| Polmonite h | 20 (9) | 10 (9) |
| Pyrexia | 17 (8) | 5 (5) |
| Il peso è diminuito | 16 (7) | 1 (1) |
| Vomito i | 15 (7) | 4 (4) |
| Eruzione cutanea j | 14 (6) | 1 (1) |
| Cambiamento nell'espettorato k | 13 (6) | 1 (1) |
| Disagio al torace | 12 (5) | 3 (3) |
| a Include afonia e disfonia b Include la tosse produttiva tosse e la sindrome della tosse delle vie aeree superiori c Include l'iperreattività bronchiale dell'asma Broncospasmo dispnea dispnea Dispnea Exerptional Exergence Expirazione Groat Luce e sibilante d Include il dolore alla schiena Artralgia Myalgia Dolore/Body Dolori Spasmo muscolare e dolore muscoloscheletrico e Include dolore orofaringeo a disagio orofaringeo Disagio gola irritazione faringea eritema superiore infiammazione delle vie aeree di infiammazione faringea edema vocale infiammazione del cavo vocale per infiammazione laringea eritema laringite f Include la sordità sordità nevosensoriale sordità vertigini unilaterale ipoacusis presincope acufene vertigini bilancia g Include la esacerbazione infettiva della BPCO di esacerbazione infettiva della BPCO della bronchiectasie h Include la polmonite atipica Empiema Infezione pleurica Effusione pleurica Infezione del tratto respiratorio inferiore infezione polmonare infezione polmonare pseudomonas polmonite polmonite aspirazione polmonite pseudomonas pseudomonas infezione da tratto respiratorio i Include vomito e vomito post-tussivo j Include l'eruzione e l'orticaria eruzione maculo-papolare eruzione cutanea k Include un aumento del espettorato espettorato purulento e espettorato scoloriti |
Reazioni di farmaco avverse selezionate che si sono verificate in <5% of patients E at higher frequency in Arikayce-treated patients in Trial 1 are presented in Table 2.
Tabella 2: reazioni avverse selezionate in <5% of Arikayce-treated MAC Patients E MOe Frequent than Regime di fondo da solo in Trial 1
| Reazione avversa | Arikayce plus Background Regimen N = 223 N (%) | Regime di fondo da solo N = 112 N (%) |
| Ansia a | 10 (5) | 0 (0) |
| Infezione fungina orale b | 9 (4) | 2 (2) |
| Bronchite | 8 (4) | 3 (3) |
| Dysgeusia | 7 (3) | 0 (0) |
| Pneumonite da ipersensibilità c | 7 (3) | 0 (0) |
| Bocca secca | 6 (3) | 0 (0) |
| Epistassi | 6 (3) | 1 (1) |
| Insufficienza respiratoria d | 6 (3) | 2 (2) |
| Pneumotorace e | 5 (2) | 1 (1) |
| La tolleranza all'esercizio è diminuita | 3 (1) | 0 (0) |
| Disturbo dell'equilibrio | 3 (1) | 0 (0) |
| Disturbo neuromuscolare f | 2 (1) | 0 (0) |
| a Include il disturbo d'ansia e ansia b Include candidosi orale e infezione fungina orale c Include la malattia polmonare interstiziale di alveolite allergica e la polmonite d Include insufficienza respiratoria acuta e insufficienza respiratoria e Include pneumotorax pneumotorace spontaneo e pneumomediastinum f Include la debolezza muscolare e la neuropatia periferica |
Fare riferimento alla tabella 1 e alla tabella 2 per il tasso di incidenza di ipersensibilità polmonite broncospasmo di broncospasmo della disfonia esacerbazione delle malattie sottostanti ototossicità ototossicità dell'irritazione delle vie aeree superiori e disturbi neuromuscolari [vedi AVVERTIMENTOS AND PRECAUZIONI ].
Esperienza post -marketing
Le seguenti reazioni avverse sono state identificate dalla sorveglianza post -marketing. Poiché queste reazioni avverse sono riportate volontariamente da una popolazione di stime precise di dimensioni sconosciute della frequenza e non è possibile stabilire una relazione causale con l'esposizione ai farmaci.
Disturbi del sistema immunitario: ipersensibilità anafilassi [vedi AVVERTIMENTOS AND PRECAUZIONI ]
Interazioni farmacologiche per Arikayce
Farmaci con potenziale nefrotossico o ototossico neurotossico
Evita l'uso concomitante di Arikayce con i farmaci associati alla nefrotossicità e all'ototossicità della neurotossicità.
Acido etacrynico furosemide urea o mannitolo
Alcuni diuretici possono migliorare la tossicità dell'aminoglicoside alterando le concentrazioni di aminoglicoside nel siero e nel tessuto. Evita l'uso concomitante di arikayce con furosemide dell'acido etacrynico urea o mannitolo per via endovenosa.
Avvertimenti per Arikayce
Incluso come parte del 'PRECAUZIONI' Sezione
Precauzioni per Arikayce
Pneumonite da ipersensibilità
Pneumonite da ipersensibilità has been repOted with the use of Arikayce in the clinical trials. Pneumonite da ipersensibilità (repOted as allergic alveolitis pneumonitis interstitial lung disease allergic reaction to Arikayce) was repOted at a higher frequency in patients treated with Arikayce plus a background regimen (3.1%) compared to patients treated with a background regimen alone (0%). Most patients with hypersensitivity pneumonitis discontinued treatment with Arikayce E received treatment with cOticosteroids [see Reazioni avverse ]. If hypersensitivity pneumonitis occurs discontinue Arikayce E manage the patient as medically appropriate.
Emottisi
Emottisi has been repOted with the use of Arikayce in the clinical trials. Emottisi was repOted at a higher frequency in patients treated with Arikayce plus a background regimen (18.4%) compared to patients treated with a background regimen alone (13.4%) [see Reazioni avverse ]. If hemoptysis occurs manage the patients as medically appropriate.
Broncospasmo
Broncospasmo has been repOted with the use of Arikayce in the clinical trials. Broncospasmo (repOted as asthma bronchial hyperreactivity broncospasmo dyspnea dyspnea exertional prolonged expiration throat tightness sibilante) was repOted at a higher frequency in patients treated with Arikayce plus a background regimen (28.7%) compared to patients treated with a background regimen alone (10.7%) [see Reazioni avverse ]. If broncospasmo occurs during the use of Arikayce treat the patients as medically appropriate.
Esacerbazione della malattia polmonare sottostante
Sono state riportate esacerbazioni di malattie polmonari sottostanti con l'uso di Arikayce negli studi clinici. Le esacerbazioni della malattia polmonare sottostante (riportate come esacerbazione infettiva cronica cronica di malattie polmonari ostruttive croniche di esacerbazione infettiva della bronchiectasi) sono state riportate a una frequenza più elevata nei pazienti trattati con Arikayce più un regime di fondo (NULL,2%) rispetto ai pazienti trattati con il solo reggimento (NULL,8%) Reazioni avverse ]. If exacerbations of underlying pulmonary disease occur during the use of Arikayce treat the patients as medically appropriate.
Anafilassi e reazioni di ipersensibilità
Le reazioni di ipersensibilità gravi e potenzialmente letali, incluso l'anafilassi, sono state riportate in pazienti che assumono Arikayce. Segni e sintomi includono insorgenza acuta della pelle e delle reazioni di ipersensibilità del tessuto mucosa (orticaria che prude le labbra gonfie/lingua/uvula) difficoltà respiratoria (mancanza di respiro sibilante e sintomi di sussulti e sintomi cardici) (Tachicardia bassa pressione sanguigna Sincope Incontinenza vertigini). Prima della terapia con Arikayce viene istituita valutare per le precedenti reazioni di ipersensibilità agli aminoglicosidi. Se l'anafilassi o una reazione di ipersensibilità si verificano interrompere Arikayce e istituire misure di supporto adeguate.
Elituità
Elituità With Use Of Arikayce
Elituità has been repOted with the use of Arikayce in the clinical trials. Elituità (including deafness vertigini presyncope tinnitus E vertigo) were repOted with a higher frequency in patients treated with Arikayce plus a background regimen (17%) compared to patients treated with background regimen alone (9.8%). This was primarily driven by tinnitus (8.1% in Arikayce plus background regimen vs. 0.9% in the background regimen alone arm) E vertigini (6.3% in Arikayce plus background regimen vs. 2.7% in the background regimen alone arm) [see Reazioni avverse ].
Monitorare attentamente i pazienti con disfunzione uditiva o vestibolare nota o sospetta durante il trattamento con Arikayce. Se si verifica l'ototossicità, gestisci il paziente come appropriato dal punto di vista medico, incluso la discontinzione potenzialmente di Arikayce.
Rischio di ototossicità a causa di varianti del DNA mitocondriale
Casi di ototossicità con aminoglicosidi sono stati osservati in pazienti con alcune varianti nel gene rRNA 12S mitocondrialmente codificato (MT-RNR1), in particolare la variante M.1555A> G. L'ototossicità si è verificata in alcuni pazienti anche quando i loro livelli sierici di aminoglicoside rientravano nell'intervallo raccomandato. Le varianti del DNA mitocondriale sono presenti in meno dell'1% della popolazione generale degli Stati Uniti e la proporzione dei vettori varianti che possono sviluppare l'ototossicità e la gravità dell'ototossicità non è nota. In caso di storia materna nota di ototossicità dovuta all'uso di aminoglicosidi o di una variante di DNA mitocondriale nota nel paziente, considerano trattamenti alternativi diversi dagli aminoglicosidi a meno che l'aumento del rischio di perdita dell'udito permanente non sia compensato dalla gravità dell'infezione e dalla mancanza di terapie alternative sicure ed efficaci.
Nefrotossicità
Nefrotossicità was observed during the clinical trials of Arikayce in patients with MAC lung disease but not at a higher frequency than the background regimen alone [see Reazioni avverse ]. Nefrotossicità has been associated with the aminoglycosides. Close monitOing of patients with known O suspected renal dysfunction may be needed when prescribing Arikayce.
Blocco neuromuscolare
I pazienti con disturbi neuromuscolari non sono stati arruolati negli studi clinici Arikayce. Gli aminoglicosidi possono aggravare la debolezza muscolare bloccando il rilascio di acetilcolina alle giunzioni neuromuscolari. Monitorare da vicino i pazienti con disturbi neuromuscolari noti o sospetti come la miastenia grave. Se si verifica un blocco neuromuscolare, può essere invertito dalla somministrazione di sali di calcio, ma può essere necessaria l'assistenza respiratoria meccanica.
Tossicità dell'embrione-fetale
Gli aminoglicosidi possono causare danni fetali quando somministrati a una donna incinta. Gli aminoglicosidi incluso Arikayce possono essere associati a una sordità congenita bilaterale totale irreversibile nei pazienti pediatrici esposti in utero . I pazienti che usano Arikayce durante la gravidanza o rimangono incinta durante l'assunzione di arikayce dovrebbero essere informati del potenziale pericolo per il feto [vedi Utilizzare in popolazioni specifiche ].
Informazioni sulla consulenza del paziente
Consiglia al paziente di leggere l'etichettatura del paziente approvato dalla FDA ( Guida ai farmaci E Patient Instructions fO Use ).
Istruzioni importanti per l'amministrazione di Arikayce
Chiedere ai pazienti di leggere le istruzioni per l'uso prima di iniziare Arikayce. Istruire i pazienti a usare solo la lamira ® Sistema di nebulizzatore per amministrare Arikayce. Consiglia al paziente o al caregiver di non utilizzare il sistema di nebulizzatore Lamira con nessun altro medicinale.
Pneumonite da ipersensibilità And Broncospasmo (Difficulty Breathing)
Consiglia ai pazienti di informare il proprio operatore sanitario se sperimentano la mancanza di respiro o il respiro sibilante dopo la somministrazione di Arikayce. Consiglia ai pazienti con una storia di malattia reattiva delle malattie delle vie aeree o broncospasmo per somministrare Arikayce dopo aver usato un broncodilatatore a breve durata [vedi AVVERTIMENTOS AND PRECAUZIONI ].
Emottisi Or Tosse
Consiglia ai pazienti di informare il proprio operatore sanitario se tossiscono sangue o sperimentano la tosse episodica durante o dopo la somministrazione di Arikayce, in particolare nel primo mese dopo aver iniziato Arikayce [vedi AVVERTIMENTOS AND PRECAUZIONI E Reazioni avverse ].
Esacerbazioni della malattia polmonare sottostante
Consiglia ai pazienti di informare il proprio operatore sanitario se sperimentano il peggioramento della malattia polmonare dopo aver iniziato Arikayce [vedi AVVERTIMENTOS AND PRECAUZIONI ].
Disfonia Or Difficulty Speaking
Consiglia ai pazienti di informare il proprio operatore sanitario se hanno difficoltà a parlare. Difficoltà a parlare o perdita di capacità di parlare è stata segnalata con Arikayce [vedi Reazioni avverse ].
Anafilassi e reazioni di ipersensibilità
Consiglia ai pazienti e ai caregiver che potrebbero verificarsi reazioni di ipersensibilità gravi e potenzialmente potenzialmente letali che richiedono un trattamento immediato. Consigliare al paziente di interrompere l'Arikayce e di cercare immediatamente cure mediche se si verificano segni o sintomi di una reazione di ipersensibilità [vedi AVVERTIMENTOS AND PRECAUZIONI ].
Elituità (Ringing In The Ears)
Consiglia ai pazienti di informare il proprio operatore sanitario se sperimentano suonando le vertigini delle orecchie o eventuali cambiamenti nell'udito perché Arikayce è stato associato alla perdita dell'udito [vedi AVVERTIMENTOS AND PRECAUZIONI ].
Consiglia al paziente di non utilizzare macchinari pesanti o svolgere attività pericolose durante l'inalazione di Arikayce attraverso il sistema di nebulizzatore Lamira perché Arikayce può causare sintomi come vertigini o sintomi respiratori.
Nefrotossicità Or Kidney Damage
Consiglia ai pazienti di informare il proprio medico se hanno problemi renali perché sono stati segnalati danni ai reni con aminoglicosidi [vedi AVVERTIMENTOS AND PRECAUZIONI ]. Blocco neuromuscolare Advise patients to infOm their healthcare provider of known neuromuscular disease (e.g. myasthenia gravis) [see AVVERTIMENTOS AND PRECAUZIONI ].
Tossicità dell'embrione-fetale
Consiglia alle donne in gravidanza che gli aminoglicosidi, incluso Arikayce, possono causare sordità congenita irreversibile quando somministrata durante la gravidanza [vedi AVVERTIMENTOS AND PRECAUZIONI E Utilizzare in popolazioni specifiche ].
Tossicologia non clinica
Mutagenesi della carcinogenesi compromissione della fertilità
In uno studio di carcinogenicità per inalazione di 2 anni i ratti sono stati esposti ad Arikayce per 15-25 50-70 o 155170 minuti al giorno per 96-104 settimane. Questi hanno fornito dosi approssimative per inalazione di 5 15 e 45 mg/kg/giorno. Il carcinoma a cellule squamose è stato osservato nei polmoni di 2 su 120 ratti somministrati la dose più alta testata. I livelli di amikacina sierica massimi di amikacina nei ratti allo stato stazionario erano circa 1,3 2,8 e 7,6 mcg · HR/mL rispettivamente a medie e alte basse rispetto all'uomo. I carcinomi a cellule squamose possono essere il risultato di un elevato carico polmonare di particolati da Arikayce nel polmone di ratto. La rilevanza dei risultati del tumore polmonare per quanto riguarda gli umani che ricevono Arikayce è sconosciuta.
Non sono state osservate prove di mutagenicità o genotossicità in una batteria di in vitro E in vivo Studi di genotossicità con una formulazione di amikacina incapsulata da liposomi simile ad Arikayce ( in vitro Test di mutagenesi microbica in vitro Test di mutazione del linfoma del topo in vitro studio di aberrazione cromosomica e un in vivo Studio di micronucleo nei ratti).
Non sono stati condotti studi sulla fertilità con Arikayce. La somministrazione intraperitoneale di amikacina a ratti maschi e femmine a dosi fino a 200 mg/kg/giorno prima dell'accoppiamento fino al giorno 7 della gestazione non era associata alla compromissione della fertilità o degli effetti avversi sullo sviluppo embrionale precoce.
Utilizzare in popolazioni specifiche
Gravidanza
Riepilogo del rischio
Non ci sono dati sull'uso di Arikayce nelle donne in gravidanza per valutare eventuali rischi associati ai farmaci di gravi difetti alla nascita o risultati avversi materni o fetali. Sebbene l'assorbimento sistemico dell'amikacina dopo l'inalazione orale dovrebbe essere basso [vedi Farmacologia clinica ] L'esposizione sistemica a farmaci antibatterici aminoglicosidici, incluso Arikayce, può essere associata a una sordità congenita bilaterale totale irreversibile quando somministrata alle donne in gravidanza [vedi AVVERTIMENTOS AND PRECAUZIONI ]. Advise pregnant women of the potential risk to a fetus.
Studi di tossicologia riproduttiva degli animali non sono stati condotti con amikacina inalata. La somministrazione sottocutanea di amikacina a ratti in gravidanza (fino a 100 mg/kg/die) e topi (fino a 400 mg/kg/giorno) durante l'organogenesi non era associata a malformazioni fetali. L'ototossicità non è stata adeguatamente valutata nella prole negli studi sugli animali.
Non è noto il rischio di background stimato di principali difetti alla nascita e aborto per le popolazioni indicate. Tutte le gravidanze hanno un rischio di fondo di perdita di difetti alla nascita o altri risultati avversi. Nella popolazione generale degli Stati Uniti il rischio di background stimato di gravi difetti alla nascita e aborto in gravidanza clinicamente riconosciuta è rispettivamente del 2-4% e del 15-20%.
Dati
Dati sugli animali
Non sono stati condotti studi di tossicologia riproduttiva animale con Arikayce o amikacina non liposomiale somministrata per inalazione.
L'amikacina è stata somministrata per via sottocutanea a ratti in gravidanza (giorni di gestazione 8-14) e topi (giorni di gestazione 7-13) a dosi di 25 100 o 400 mg/kg per valutare la tossicità dello sviluppo. Queste dosi non hanno causato malformazioni fetali viscerali o scheletriche nei topi. L'elevata dose è stata eccessivamente tossica maternamente nei ratti (nefrotossicità e mortalità) precludendo la valutazione della prole a questa dose. Le malformazioni fetali non sono state osservate alla dose bassa o media nei ratti. Sviluppo post -natale dei ratti e dei topi esposti a queste dosi di amikacina in utero non differiva significativamente dal controllo.
Elituità was not adequately evaluated in offspring in animal developmental toxicology studies.
Lattazione
Riepilogo del rischio
Non ci sono informazioni sulla presenza di Arikayce nel latte umano gli effetti sul bambino allattato al seno o sugli effetti sulla produzione di latte dopo la somministrazione di arikayce per inalazione. Sebbene i dati pubblicati limitati su altri percorsi di somministrazione di amikacina indicano che l'amikacina è presente nell'assorbimento sistemico del latte umano di Arikayce a seguito della somministrazione inalata dovrebbe essere bassa [vedi Farmacologia clinica ]. The developmental E health benefits of breastfeeding should be considered along with the mother’s clinical need fO Arikayce E any potential adverse effects on the breastfed child from Arikayce O from the underlying maternal condition.
Uso pediatrico
Non sono state stabilite sicurezza ed efficacia di Arikayce nei pazienti pediatrici di età inferiore ai 18 anni.
Uso geriatrico
Negli studi clinici NTM del numero totale di pazienti che ricevevano Arikayce 208 (NULL,5%) erano ≥ 65 anni e 59 (NULL,6%) erano ≥ 75 anni. Non sono state osservate differenze complessive nella sicurezza ed efficacia tra soggetti anziani e soggetti più giovani. Poiché i pazienti anziani hanno maggiori probabilità di avere una riduzione della funzione renale, può essere utile monitorare la funzione renale [vedi AVVERTIMENTOS AND PRECAUZIONI ].
Compromissione epatica
Arikayce has not been studied in patients with hepatic impairment. No dose adjustments based on hepatic impairment are required since amikacin is not hepatically metabolized [see Farmacologia clinica ].
Effetti collaterali del vaccino HEP B
Compromissione renale
Arikayce has not been studied in patients with renal impairment. Given the low systemic exposure to amikacin following administration of Arikayce clinically relevant accumulation of amikacin is unlikely to occur in patients with renal impairment. However renal function should be monitOed in patients with known O suspected renal impairment including elderly patients with potential age-related decreases in renal function [see AVVERTIMENTOS AND PRECAUZIONI Uso geriatrico ].
Informazioni per overdose per Arikayce
Le reazioni avverse specificamente associate al sovradosaggio di Arikayce non sono state identificate. La tossicità acuta deve essere trattata con immediato ritiro di Arikayce e dovrebbero essere effettuati test di funzionalità renale.
L'emodialisi può essere utile per rimuovere l'amikacina dal corpo.
In tutti i casi di sospetti medici di sovradosaggio dovrebbero contattare il Centro di controllo del veleno regionale per informazioni sul trattamento efficace. Nel caso di qualsiasi sovradosaggio dovrebbe essere presa in considerazione la possibilità di interazioni farmacologiche con alterazioni nella disposizione dei farmaci.
Controindicazioni per Arikayce
Arikayce is contraindicated in patients with a known hypersensitivity to any aminoglycoside.
Farmacologia clinica fO Arikayce
Meccanismo d'azione
Arikayce is an antibatterico drug [see Microbiologia ].
Farmacodinamica
Arikayce exposure-response relationships E the time course of pharmacodynamic response are unknown.
Farmacocinetica
Concentrazioni di espettorato
Dopo l'inalazione una volta al giorno di 590 mg di Arikayce in Mycobacterium avium Le concentrazioni di espettorato complesse (MAC) a 1-4 ore dopo l'inlaborazione erano 1720 884 e 1300 mcg/g rispettivamente a 1 3 e 6 mesi. È stata osservata un'elevata variabilità nelle concentrazioni di amikacina (CV%> 100%). Dopo 48-72 ore dopo l'inlaborazione delle concentrazioni di amikacina sono diminuite a circa il 5% di quelle da 1 a 4 ore dopo l'inclusione.
Concentrazioni sieriche
Dopo 3 mesi di inalazione un tempo giornaliera di 590 mg di Arikayce in pazienti MAC il siero medio AUC0-24 era 23,5 mcg*hr/ml (intervallo: da 8,0 a 46,5 mcg*hr/ml; n = 12) e il siero medio CMAX era 2,8 mcg/ml (intervallo: da 1,0 a 4,4 μg/ml; n = 12). Il massimo CMAX e AUC0-24 erano al di sotto del CMAX medio di circa 76 mcg/ml e AUC0-24 di 154 mcg*hr/ml osservati per la somministrazione endovenosa di amikacina solfato per iniezione al dosaggio approvato di 15 mg/kg una volta al giorno negli adulti sani.
Assorbimento
La biodisponibilità di Arikayce dovrebbe variare principalmente dalle differenze individuali nell'efficienza del nebulizzatore e nella patologia delle vie aeree.
Distribuzione
Il legame proteico di amikacina nel siero è ≤ 10%.
Eliminazione
Dopo l'inalazione di Arikayce nei pazienti con Mac l'apparente emivita sierica di amikacina variava da circa 5,9 a 19,5 ore.
Metabolismo
L'amikacin non subisce un metabolismo apprezzabile.
Escrezione
L'amikacina assorbita sistematicamente dopo la somministrazione di Arikayce viene eliminata principalmente tramite filtrazione glomerulare. In media il 7,42% (che varia da 0,72 al 22,60%; n = 14) della dose totale di Arikayce è stato escreto nelle urine come farmaco invariato rispetto al 94% a seguito della somministrazione endovenosa di amikacina solfato per iniezione. L'amikacina non assorbita dopo l'inalazione di Arikayce viene probabilmente eliminata principalmente dal turnover cellulare e dall'espesa.
Studi sull'interazione farmacologica
Non sono stati condotti studi di interazione farmacologica clinica con Arikayce [vedi Interazioni farmacologiche ].
Microbiologia
Meccanismo d'azione
L'amikacina è un aminoglicoside battericida semisintetico polycazionale. L'amikacina entra nella cellula batterica legandosi a componenti caricati negativamente della parete cellulare batterica che interrompono l'architettura generale della parete cellulare. Il principale meccanismo d'azione è l'interruzione e l'inibizione della sintesi proteica nei batteri bersaglio legandosi alla subunità ribosomiale 30S.
Resistenza
Il meccanismo di resistenza all'amikacina nei micobatteri è stato collegato alle mutazioni nel gene RRS dell'RRNA 16S. Negli studi clinici MAC isolati che sviluppano un microfono di amikacina di> 64 mcg/ml dopo la linea di base sono stati osservati in una percentuale più elevata di soggetti trattati con arikayce [vedi Studi clinici ].
Interazione con altri antimicrobici
Non c'è stato no in vitro signal for antagonism between amikacin and other antimicrobials against MAC based on fractional inhibitory concentration (FIC) and macrophage survival assays. In select instances some degree of synergy between amikacin and other agents has been observed as for example synergy between aminoglycosides including amikacin and the beta-lactam class has been documented.
Tossicologia animale e farmacologia
Per fornire informazioni sul dosaggio cronico di Arikayce a un'altra specie animale è stato condotto uno studio di tossicologia per inalazione di 9 mesi. I macrofagi alveolari schiumosi associati alla clearance del prodotto inalato erano presenti all'incidenza e alla gravità correlati alla dose, ma non erano associati all'iperplasia del tessuto infiammato o alla presenza di cambiamenti preneoplastici o neoplastici. I cani sono stati esposti ad Arikayce per un massimo di 90 minuti al giorno fornendo dosi di amikacina per inalazione di circa 5 10 e 30 mg/kg/giorno.
Studi clinici
Prova 1 (NCT Mycobacterium avium Malattia polmonare complessa (MAC) confermata da almeno 2 risultati della coltura dell'espettorato. I pazienti sono stati considerati avere una malattia polmonare Mac refrattaria se non hanno raggiunto colture di espettorato negative dopo una durata minima di 6 mesi consecutivi di terapia di regime di fondo che è stata in corso o fermata non più di 12 mesi prima della visita di screening. I pazienti sono stati randomizzati a Arikayce più un regime di fondo o un regime di fondo da solo. L'endpoint surrogato per la valutazione dell'efficacia si basava sul raggiungimento della conversione della cultura (3 culture di espettorato negativa mensile consecutive) entro il mese 6. La data di conversione è stata definita come la data della prima delle 3 culture mensili negative che dovevano essere raggiunte entro il mese 4 al fine del mese per soddisfare i reggiseni di background o per i reggisimi di background al fine del mese. randomizzazione) per un totale di 12 mesi dopo la prima coltura di espettorato negativo.
Un totale di 336 pazienti sono stati randomizzati (Arikayce Plus Regimen di fondo N = 224; Regime di fondo da solo n = 112) (popolazione ITT) con un'età media di 64,7 anni e c'era una percentuale più elevata di femmine (NULL,3%) rispetto ai maschi (NULL,7%) nello studio. Al momento dell'iscrizione ai 336 soggetti nella popolazione ITT 302 (NULL,9%) erano su un regime basato sulle linee guida per MAC o OFF basato su terapia basata sulle linee guida per Mac per meno di 3 mesi, mentre 34 (NULL,1%) erano fuori da 3 a 12 mesi prima dell'iscrizione. Al momento dello screening i pazienti sono stati stratificati dallo stato del fumo (fumatore attuale o meno) e per se i pazienti erano in trattamento o fuori dal trattamento per almeno 3 mesi. La maggior parte dei pazienti allo screening non erano attuali fumatori (NULL,3%) e aveva bronchiectasie sottostanti (NULL,5%). Al basale 329 pazienti si trovavano su un regime di sfondo multidrug che includeva un macrolide (NULL,3%) una rifamicina (NULL,3%) o etambutolo (NULL,4%). Complessivamente il 55,6% dei soggetti stava ricevendo un regime di fondo a tripla farmaco composto da un macrolide a rifamicina ed etambutolo.
La percentuale di pazienti che raggiungeva la conversione della coltura (3 colture di espettorato negativa mensile consecutive) entro il mese 6 era significativamente (p <0.0001) greater fO Arikayce plus background regimen (65/224 29.0%) compared to background regimen alone (10/112 8.9%). Of those receiving Arikayce plus background regimen 18.3% (41/224) achieved culture conversion by Month 6 E sustained sputum culture conversion (defined as consecutive negative sputum cultures with no positive culture on solid media O no mOe than 2 consecutive positive cultures on liquid media following culture conversion) fO up to 12 months of treatment after the first culture that defined culture conversion compared to 2.7% (3/112) of patients receiving background regimen alone (p <0.0001). At 3 months after the completion of treatment 16.1% (36/224) of patients who had received Arikayce plus background regimen maintained durable culture conversion compared to 0% of patients who had received background regimen alone (p <0.0001).
Proporzione cumulativa di soggetti che raggiungono la conversione della cultura mostrata dal primo mese di conversione intenzione di trattare la popolazione (ITT)
 |
Nella sperimentazione 1 23/224 (NULL,3%) dei pazienti presentava isolati MAC che sviluppavano MIC di> 64 mcg/mL mentre ricevevano un trattamento con Arikayce. Nel solo regime di fondo il braccio 4/112 (NULL,6%) dei pazienti presentava isolati MAC che sviluppavano MIC di amikacina di> 64 mcg/mL.
Ulteriori endpoint per valutare il beneficio clinico di Arikayce, ad esempio il cambiamento dal basale nella distanza di test di sei minuti e il questionario respiratorio di Saint George non ha dimostrato il beneficio clinico entro il mese 6.
Informazioni sul paziente per Arikayce
Arikayce
(Ar 'i kase)
Popolazione limitata
(sospensione dell'inalazione del liposoma amikacina) per uso di inalazione orale
Importante: solo per inalazione orale.
Quali sono le informazioni più importanti che dovrei sapere su Arikayce?
Arikayce can cause serious side effects including:
- Infiammazione allergica dei polmoni: Questi problemi respiratori possono essere sintomi di infiammazione allergica dei polmoni e spesso arrivano con:
- febbre
- sibilante
- tosseing
- fiato corto
- respirazione rapida
- tosseing up of blood (hemoptysis): Tosseing up blood is a serious E common side effect of Arikayce.
- Gravi problemi di respirazione: Gravi problemi di respirazione possono essere sintomi del broncospasmo. Il broncospasmo è un effetto collaterale grave e comune di Arikayce. I sintomi del broncospasmo includono:
- fiato corto
- Respirazione difficile o lavorata
- sibilante
- tosseing O tenuta toracica
- peggioramento della malattia polmonare ostruttiva cronica (BPCO): Questo è un effetto collaterale grave e comune di Arikayce.
- Reazioni allergiche gravi: Le gravi reazioni allergiche che possono portare alla morte sono accadute alle persone che prendono Arikayce. Smetti di prendere subito Arikayce e ottenere assistenza medica di emergenza se si dispone dei seguenti sintomi di una grave reazione allergica:
- orticaria
- rumoroso acuto
- Respirazione a frequenza cardiaca veloce (Stridor)
- prurito
- tosse
- Sentirsi leggeri
- arrossamento o arrossimento di
- nausea
- Sentirsi svenire la pelle (arrossamento)
- lingua di labbra gonfie o
- vomito
- Perdita del controllo della gola o della vescica (incontinenza)
- difficoltà a respirare o
- diarrea
- vertigini sibilante
- fiato corto
- Senti i crampi nella zona dello stomaco
Mentre usando Arikayce questi effetti collaterali possono diventare abbastanza gravi che il trattamento in un ospedale è necessario.
Chiama il tuo medico o ottieni subito assistenza medica se Hai uno di questi gravi effetti collaterali mentre prendi Arikayce. Il tuo operatore sanitario potrebbe chiederti di smettere di usare Arikayce per un breve periodo di tempo o smettere completamente di usare Arikayce.
Cos'è Arikayce?
Arikayce is a prescription medicine used to treat adults with refractOy (difficult to treat) Mycobacterium avium Malattia polmonare complessa (MAC) come parte di un piano di trattamento farmacologico antibatterico combinato (regime).
Non è noto se Arikayce è sicuro ed efficace nei bambini di età inferiore ai 18 anni. Questo prodotto è stato approvato dalla FDA utilizzando il percorso limitato della popolazione.
Ciò significa che la FDA ha approvato questo farmaco per una popolazione di pazienti limitata e specifica e gli studi sul farmaco potrebbero aver risposto solo a domande focalizzate sulla sua sicurezza e efficacia.
Non usare Arikayce se tu:
- sono allergici a qualsiasi aminoglicoside o qualsiasi degli ingredienti di Arikayce. Vedere Quali sono gli ingredienti di Arikayce? Alla fine di questo opuscolo per un elenco completo di ingredienti in Arikayce.
Prima di usare Arikayce, racconta al tuo operatore sanitario su tutte le condizioni mediche, anche se tu:
- Avere la malattia polmonare ostruttiva cronica dell'asma (BPCO) mancanza di respiro o respiro sibilante (broncospasmo).
- Ti è stato detto che hai una scarsa funzione polmonare.
- Hai o hanno avuto problemi di udito (inclusi rumori nelle orecchie come squillo o sibilo) perdita dell'udito o tua madre ha avuto problemi di udito dopo aver assunto un aminoglicoside.
- Ti è stato detto che hai alcune varianti geniche (un cambiamento nel gene) relative alle anomalie dell'udito ereditate da tua madre.
- avere vertigini o senso della stanza che gira.
- avere problemi ai reni.
- Avere malattie neuromuscolari come la miastenia grave.
- are pregnant or plan to become pregnant. It is not known if ARIKAYCE can harm your unborn baby. ARIKAYCE is in a class of medicines that may be connected with complete deafness in babies at birth. The deafness affects both ears and cannot be changed.
- stanno allattando o pianificano di allattare. Non è noto se la medicina in Arikayce passa nel latte materno e se può danneggiare il tuo bambino. Parla con il tuo operatore sanitario del modo migliore per nutrire il tuo bambino durante il trattamento con Arikayce.
Di 'al tuo operatore sanitario di tutte le medicine che prendi, incluso medicinali da prescrizione e medicine da banco vitamine e integratori a base di erbe.
Come dovrei usare Arikayce?
- Leggi le istruzioni passo-passo per l'utilizzo di Arikayce alla fine della guida ai farmaci e le istruzioni complete per l'uso fornite nel kit. Le istruzioni del produttore per l'uso forniscono informazioni complete su come mettere insieme (assemblare) Preparare l'uso e disinfettare la tua lamira ® Sistema di nebulizzatore.
- Non farlo Usa Arikayce a meno che tu non capisca le indicazioni fornite. Se hai domande, parla con il tuo medico o chiama il supporto Arikares al numero 1-833-Arikare (1-833-274-5273).
- Usa Arikayce esattamente come il tuo operatore sanitario ti dice di usarlo. Non usare Arikayce più spesso di quanto prescritto per te.
- Usa solo Arikayce con il sistema di nebulizzatore Lamira.
- Inspira ogni dose giornaliera di Arikayce 1 volta ogni giorno attraverso il ricevitore di nebulizzatore Lamira. Non usare più di 1 fiala di Arikayce in un giorno.
- Non farlo use Arikayce after the expiration date on the vial. If you fOget to take your daily dose of Arikayce take your next dose at your usual time the next day.
- Non farlo Raddoppia la dose per compensare la dose mancata.
- Non farlo Smetti di usare Arikayce o altri medicinali per curare la malattia polmonare MAC se non dirlo di farlo dal tuo operatore sanitario.
- Se usi troppo Arikayce, chiama il tuo medico o vai subito al pronto soccorso più vicino.
Quali sono i possibili effetti collaterali di Arikayce?
Arikayce may cause serious side effects including:
- Guarda quali sono le informazioni più importanti che dovrei sapere su Arikayce?
- Perdita dell'udito o squillo nelle orecchie (ototossicità) . L'ototossicità è un effetto collaterale grave e comune di Arikayce. Di 'subito al tuo operatore sanitario se hai una perdita dell'udito o senti rumori nelle orecchie come squillare o sibilare. Di 'al tuo operatore sanitario se inizi ad avere problemi con l'equilibrio o le vertigini (vertigini).
- peggioramento dei problemi renali (nefrotossicità). Arikayce is in a class of medicines which may cause wOsening kidney problems. Your healthcare provider may do a blood test to check how well your kidneys are wOking during your treatment with Arikayce.
- peggioramento della debolezza muscolare (blocco neuromuscolare). Arikayce is in a class of medicines which can cause muscle debolezza to get wOse in people who already have problems with muscle debolezza (myasthenia gravis).
Gli effetti collaterali più comuni di Arikayce includono:
- cambia nella tua voce e
- mal di gola
- raucessità del dolore muscolare (disfonia)
- diarrea
- nausea
- stanchezza (fatica)
- febbre
- vomito
- mal di testa
- Diminuzione del peso
- aumento dell'espettorato
- eruzione cutanea
- disagio al torace
- tosse during O after a dose of Arikayce especially in the first month after starting treatment.
Questi non sono tutti i possibili effetti collaterali di Arikayce.
posso prendere zyrtec e pseudoefedrina
Chiama il medico o il farmacista per consigli medici sugli effetti collaterali. È possibile segnalare gli effetti collaterali alla FDA al numero 1-800-FDA-1088
Come dovrei conservare Arikayce?
- Conservare i fiale di Arikayce refrigerati da 36 ° F a 46 ° F (da 2 ° C a 8 ° C) fino alla data di scadenza sulla fiala. Non congelare.
- Dopo che Arikayce è stato immagazzinato nel frigorifero, qualsiasi medicina non utilizzata deve essere gettata via (eliminata) dopo la data di scadenza sulla fiala.
- Conservare le fiale di Arikayce a temperatura ambiente compresa tra 68 ° F e 77 ° F (da 20 ° C a 25 ° C) per un massimo di 4 settimane
- Dopo che Arikayce è stato immagazzinato a temperatura ambiente, qualsiasi medicina non utilizzata deve essere gettata via (smaltita) alla fine di 4 settimane.
- Usa subito una fiala Arikayce aperta.
- Getta via subito la fiala di Arikayce dopo l'uso.
Mantieni Arikayce e tutti i medicinali fuori dalla portata dei bambini.
Informazioni generali sull'uso sicuro ed efficace di Arikayce
Le medicine sono talvolta prescritte a fini diversi da quelli elencati in una guida ai farmaci. Non usare Arikayce per una condizione per la quale non è stata prescritta. Non dare arikayce ad altre persone anche se hanno gli stessi sintomi che hai. Potrebbe danneggiare loro. Puoi chiedere al tuo farmacista o al fornitore di assistenza sanitaria informazioni su Arikayce scritta per gli operatori sanitari.
Quali sono gli ingredienti di Arikayce?
Ingrediente attivo: Amikacina solfato
Ingredienti inattivi: Dipalmitoilfosfatidilcolina (DPPC) cloruro di sodio di sodio idrossido di sodio di sodio (per regolazione del pH) e acqua per iniezione
Questa guida ai farmaci è stata approvata dalla Food and Drug Administration degli Stati Uniti.
Istruzioni per l'uso
Arikayce ®
Popolazione limitata
(sospensione dell'inalazione del liposoma amikacina) per uso di inalazione orale
Lamira ®
Sistema di nebulizzatore
Prima di utilizzare il sistema di nebulizzatore Lamira, assicurati di leggere e comprendere le informazioni dettagliate nelle istruzioni complete per l'uso fornite con il sistema di nebulizzatore Lamira. Ciò fornirà informazioni più complete su come mettere insieme (assemblare) preparare l'uso e disinfettare il sistema di nebulizzatore Lamira. Se non si capisce alcuna parte del contatto delle istruzioni Supporto Arikares al numero 1-833-Arikare (1-833-274-5273) Prima di utilizzare il sistema di nebulizzatore Lamira.
Raccogli la tua medicina Arikayce. Il kit a 28 giorni Arikayce contiene:
- 1 Guida ad avvio rapido Arikayce
- 1 istruzioni per l'uso Insert
- 1 inserto per informazioni sulla prescrizione completa
- 1 portatile di nebulizzatore Lamira
- 4 teste di aerosol Lamira (1 in ogni scatola settimanale)
- 28 fiale (1 fiala ogni giorno) di Arikayce (7 in ogni scatola settimanale)
Controlla per assicurarti di avere tutte le parti necessarie per il sistema di nebulizzatore Lamira:
- Case di trasporto
- Cavo di connessione
- Controller
- Alimentazione A/C.
- Batterie AA
 |
Ricevitore di nebulizzatore Lamira di riserva:
- Capo e sigilla medica
- Serbatoio di farmaci
- Valvola blu
- Camera aerosol
- Boccaglio
- Testa di aerosol di riserva
 |
Avrai anche bisogno delle seguenti forniture che non sono disponibili nel tuo kit Arikayce a 28 giorni che ti aiuteranno a prenderti cura del tuo sistema di nebulizzatore Lamira:
- Cancella sapone liquido per pulire il telefono e la testa di aerosol
- Acqua distillata per disinfettare il portatile e la testa di aerosol
Scegli il tuo alimentatore e preparalo.
UN. 4 batterie AA
 |
B. Alimentazione A/C.
- Collegare l'alimentazione A/C al controller.
- Collegare l'alimentazione A/C all'uscita del muro.
Non farlo insert the A/C Power into thefront of the Controller.
 |
Pulizia e disinfezione
Prima di usare il risciacquo e disinfettare il telefono e la testa di aerosol. Spostando il risciacquo pulito e disinfetta il portatile, inclusa la testa di aerosol dopo ogni utilizzo.
Quando ricevi il telefono e la testa di aerosol non saranno sterili. La pulizia e la disinfezione del portatile e della testa di aerosol è importante per ridurre il rischio di malattie e contaminazione delle infezioni.
- Pulizia del ricordo del telefono e della testa di aerosol: Prima di usare il risciacquo e pulire il telefono e la testa di aerosol. Spostando il risciacquo in avanti e pulire il telefono, compresa la testa di aerosol subito dopo ogni utilizzo.
Usa solo semplici papertowel o salviette. Non farlo use towels O wipes that have any chemicals added to them such as alcohol lotion O baby wipes.
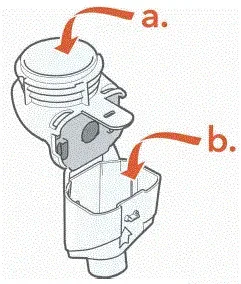
Fai attenzione a non danneggiare le parti. Non pulire la testa di aerosol.
Getta gli asciugamani di carta smaltindoti con rifiuti solidi.

- Smontare (smontare) il telefono per la pulizia
- Spazzare delicatamente eventuali gocce della medicina dal serbatoio del farmaco (A) Camera di aerosol (B) e bocconcino (C) prima del risciacquo per ridurre gli antibiotici aggiunti ai sistemi idrici.
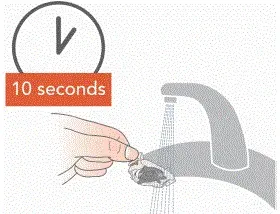
- Risciacquare ciascuna delle parti sotto acqua di rubine 10 secondi. Risciacquare la testa di aerosol per 10 secondi su ogni lato.
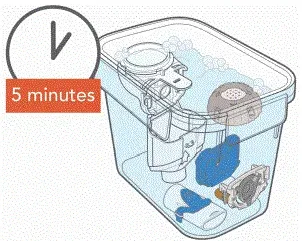
- Pulisci tutte le parti del portatile aggiungendo alcune gocce di sapone per piatti liquidi trasparenti e acqua calda a rubinetto a una vasca o una ciotola pulita. Coprire le parti del portatile nell'acqua calda insaponata e immergersi per 5 minuti scuoterli periodicamente. Quindi sciacquarli accuratamente sotto acqua di rubinetto che corre calda.
- Disinfezione del portatile e della testa di aerosol prima del ricordo di prima utilizzo: disinfettare il portatile e la testa di aerosol prima di primo utilizzo.

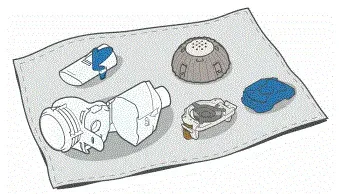
- Assicurati che il portatile e la testa di aerosol siano puliti prima di disinfettare.
- Assicurati che la pentola abbia abbastanza acqua distillata per coprire completamente tutte le parti del portatile, inclusa la testa di aerosol.
- Scaldare l'acqua a ebollizione in una pentola pulita.
- Posizionare le parti del portatile, compresa la testa di aerosol nell'acqua bollente.
- Fai bollire per un pieno 5 minuti . Nota: può essere utile utilizzare un timer.
- Aria asciutta su a senza lanugine asciugamano. Se completamente asciutto avvolgi le parti in un asciugamano senza lanugine per lo stoccaggio. Puoi rimetterli insieme appena prima di prendere il tuo prossimo trattamento.
Assemblaggio del telefono
Passaggio 1: lavarsi le mani con sapone e acqua E dry them well.
 |
Passaggio 2: inserire la valvola blu.
Apri il portatile tirandolo delicatamente sulla scheda del serbatoio del farmaco.
Inserire la valvola blu in modo che poggia sulla parte superiore della camera di aerosol con le alette della valvola rivolte verso il basso (lembi della valvola non piegate).
 |
Aer Osol C Hamber Val Flaps Valve Flap Valvola blu
Passaggio 3: inserire la testa di aerosol.
Afferrare la testa di aerosol dalle 2 linguette di plastica flessibili su ciascun lato. Assicurati che il testo Lamira ® è rivolto verso di te ed è in cima alla testa di aerosol.
Sprema le 2 linguette di plastica flessibili insieme inserendo la testa di aerosol nel serbatoio dei farmaci.
Chiudi il portatile quando si è finita (nessun vuoto lungo il bordo della valvola blu).
 |
Non farlo touch the silver part of theAerosol Head at any time.
Dopo che la testa di aerosol è stata utilizzata 7 volte di distanza (dispone) e sostituire con un nuovo processo di pulizia. Il telefono Lamira deve essere utilizzato per 28 giorni.
 |
Passaggio 4: attaccare il portafoglio giocattolo del bocchino con la falda blu.
 |
Passaggio 5: infine collegare il portatile al controller.
UN. Collegare il cavo di connessione al telefono. A1. Adeguarsi la parte inferiore del connettore con il fondo del portatile.
A2. Spingi verso l'alto contro il portatile fino a quando non senti i pezzi che si agganciano insieme. B. Collegare il cavo di connessione al controller.
 |
Prendendo Arikayce
Il tuo Arikayce dovrebbe essere a temperatura ambiente prima di utilizzare per assicurarsi che il sistema di nebulizzatore Lamira funzioni correttamente. Non farlo use other medicines in your HEset.
Porta Arikayce a temperatura ambiente rimuovendolo dal frigorifero Almeno 45 minuti prima dell'uso. Non farlo use if your Arikayce has been frozen.
Passaggio 1: preparare il tuo arikayce.
- Posizionare il telefono su una superficie stabile piatta pulita.
- Agita la fiala di Arikayce per un minimo di 10-15 secondi E fino a quando la medicina non appare uguale per tutto e ben miscelato.
 |
Come aprire la fiala di Arikayce
 |
 |
 |
 |
- Sollevare il cappuccio arancione dalla fiala.
- Afferra l'anello di metallo In cima alla fiala e tiralo giù delicatamente fino a quando 1 late si rompe dalla fiala ma non tira completamente la linguetta.
- Tira la fascia metallica From Around Fial Top con un movimento circolare fino a quando non si stacca completamente.
- Rimuovere con cura il tappo di gomma.
UN. Apri la fiala e versa l'Arikayce nel serbatoio del farmaco.
B. Attaccare il cappuccio del farmaco.
 |
Passaggio 2: siediti in una posizione verticale rilassata.
- Premere e tenere premuto il pulsante ON/OFF per alcuni secondi per accendere la Lamira.
- La nebbia inizierà a fluire.
 |
Passaggio 3: inserire il bocchino (ma non coprire il lembo blu) e fare respiri profondi lenti.
- Quindi respira normalmente dentro e fuori attraverso il bocchino fino al completamento del trattamento.
- Il trattamento dovrebbe richiedere circa 14 minuti ma potrebbe richiedere fino a 20 minuti.
Assicurati di tenere il livello del telefono durante il trattamento.
 |
Passaggio 4: verificare che il trattamento sia terminato.
- La Lamira emetterà un segnale acustico 2 volte.
- Un segno di spunta apparirà brevemente sullo schermo.
- Il controller si spegne automaticamente.
- Rimuovere il tappo del farmaco e Controlla il serbatoio del farmaco per assicurarsi che non più di qualche goccia di Arikayce rimanga. Se Arikayce rimane sostituire il tappo del farmaco, premere il pulsante ON/OFF e completare la dose.
 |
Per eventuali problemi che potresti avere con il tuo sistema di nebulizzatore Lamira, consultare la sezione J -.
Pulire il telefono e la testa di aerosol Lamira dopo l'uso
- Risciacquare subito il ricevitore pulito e disinfetto dopo ogni utilizzo per ridurre la malattia e la contaminazione delle infezioni.
- Disinfetta il portatile e la testa di aerosol dopo ogni utilizzo.
- Vedi la pulizia e la disinfezione all'inizio delle istruzioni per l'uso su come pulire e disinfettare correttamente il portatile e la testa di aerosol.
Queste istruzioni per l'uso sono state approvate dalla Food and Drug Administration degli Stati Uniti.






